苯并噻嗪酮类GSK-3β 非ATP 竞争型抑制剂的设计、合成与生物活性评价
鹿文博,张 鹏,黄 科,楚 勇,2* ,叶德泳*
(1. 复旦大学 药学院 药物化学教研室,上海201203;2. 中国科学院 上海药物研究所新药研究国家重点实验室,上海201203)
糖原合成酶激酶-3β(glycogen synthase kinase-3β,GSK-3β)是一个多功能的丝氨酸/苏氨酸蛋白激酶[1],在哺乳动物中广泛存在。它参与调节体内多种生理过程,通过磷酸化作用影响一系列的细胞功能,包括代谢、分化、增殖,还有细胞凋亡等[2-4]。研究表明,GSK-3β 抑制剂可应用于治疗糖尿病、阿尔茨海默病(Alzheimer's disease,AD)、癌症等多种复杂性疾病,尤其是在治疗阿尔茨海默病方面。
人体大脑内GSK-3β 的分布很广泛[5],其高活性或高表达会导致微管相关蛋白—tau 蛋白的过度磷酸化[6],过度磷酸化的tau 蛋白与微管结合能力降低,从而导致其从微管上脱落,在细胞内形成神经元纤维缠结,这也是AD 公认的发病机制之一。因此抑制GSK-3β 是治疗AD 的一个很好的途径。目前临床上应用的药物只能缓解AD的某些症状,而无法阻止AD 的发病。因此,研究新型的选择性较好的GSK-3β 抑制剂在治疗AD方面有着很好的应用前景。
过去20 年里,关于GSK-3β 抑制剂的报道已有很多,但是这些抑制剂大多是ATP 竞争型的。该类抑制剂作用于GSK-3β 的ATP 结合位点,体外活性一般较好(纳摩尔级)。但是由于该ATP结合位点在500 多种激酶中具有高度的保守性,因而ATP 竞争型抑制剂的选择性往往较差。当前,GSK-3β 非ATP 竞争型抑制剂的研究引起了人们越来越多的关注,正在成为一个新的研究热点。该类抑制剂作用于GSK-3β 所特有的底物结合位点或变构位点,与ATP 竞争型抑制剂相比,该类抑制剂选择性较好。
尽管目前已知的GSK-3β 非ATP 竞争型抑制剂还不多,而且体外酶抑制活性还不高,即使活性最好的TDZDs(thiadiazolidinones)类化合物IC50值也仅有2 ~10 μmol·L-1[7],但其中一个化合物NP031112 已在欧洲临床试验ⅡB 期中用于治疗AD,表明GSK-3β 非ATP 竞争型抑制剂具有开发研究的可能性。
作为一个与多种疾病相关的靶点,GSK-3β抑制剂的研究,尤其是非ATP 竞争型抑制剂,有着更好的开发和应用前景。一方面,非ATP 竞争型抑制剂选择性较好,并且其活性还有很大的提升空间;另一方面,该类抑制剂的开发进展迅速,具有比较明确的应用前景。因此致力于此类抑制剂的开发,有望找到活性和选择性都较好的治疗相关疾病的药物,尤其是在治疗阿尔茨海默病方面。
1 目标化合物的设计及合成方法
Palomo 等[8]最近报道的一个GSK-3β 非ATP竞争型抑制剂VP 0.7(图1,IC50=3 μmol·L-1)引起了作者极大的兴趣。该化合物含有一个较长的疏水侧链和一个特异性的母核,计算机模拟推测其可能作用于GSK-3β 的变构位点[8]。本课题组在前期活性筛选中发现了另外一个GSK-3β 非ATP竞争型抑制剂HZjb(图1,IC50=100 μmol·L-1),尽管活性不高,但结构比较新颖。该化合物含有的苯并噻嗪酮母核与VP 0.7 的母核结构非常相似,因此作者综合两个化合物的结构特点,运用分子杂交(molecular hybridization)的概念[9],设计合成了一系列以苯并噻嗪酮为母核的化合物,以期找到活性较好、结构新颖的GSK-3β 非ATP 竞争抑制剂。另外,对于长疏水侧链的设计,首先考虑引入单纯的疏水侧链,以验证疏水侧链的作用;然后考察侧链的长度对活性的影响;最后对侧链做初步的修饰。
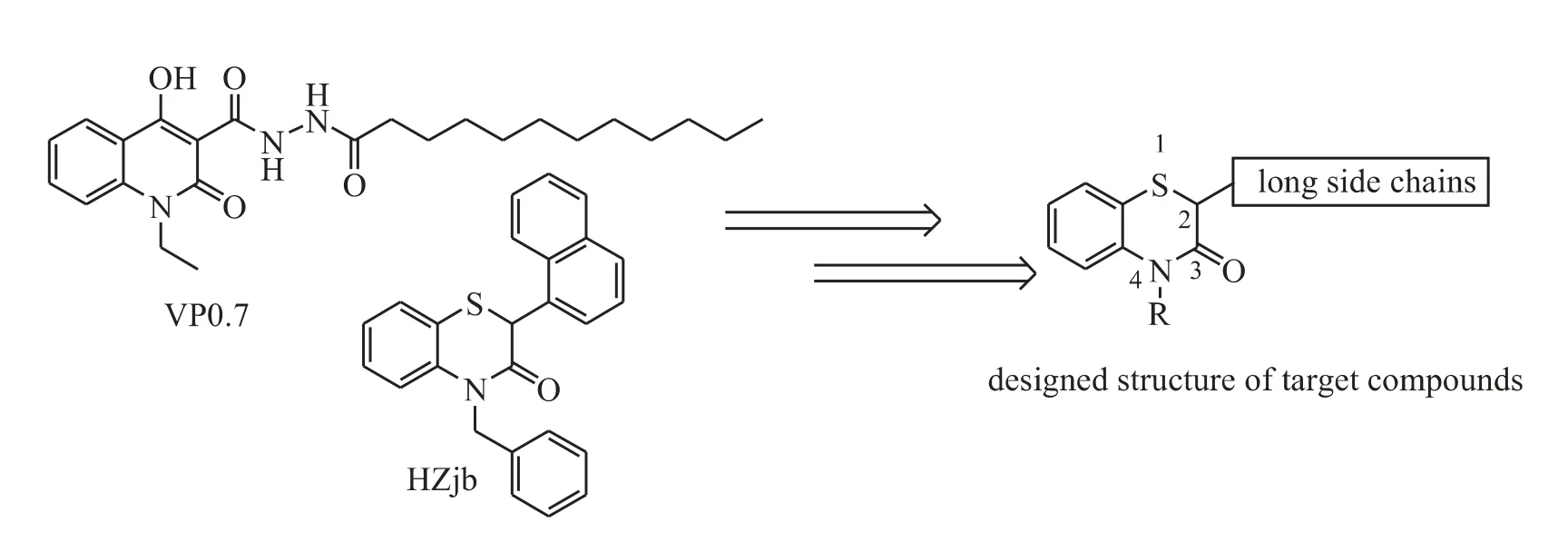
Figure 1 The structures of VP 0.7,HZjb and target compounds
目标化合物的合成路线如图2 所示:原料1在碳酸钾的的作用下,经过氮烷基化反应得到化合物2a ~2d;然后在氢化钠的作用下(氮气保护),经过酰基化反应得到化合物3a ~3d 及目标化合物3e;化合物3a ~3d 可不经分离纯化,直接与水合肼发生肼解反应得到相应的酰肼4a ~4d;在缩合剂HOBT/EDCI 的作用下,酰肼化合物4a ~4d 与不同的有机酸在室温下缩合即得到目标产物5a ~5u。
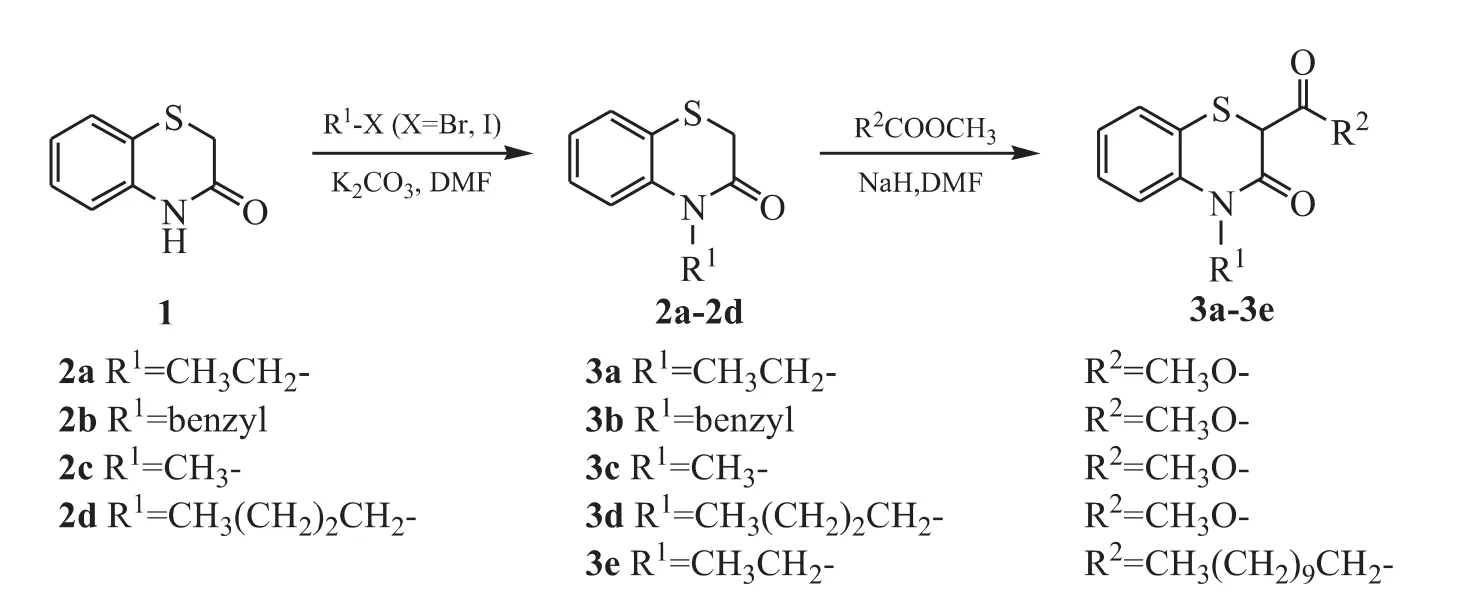
Figure 2 The synthetic route to the target compounds
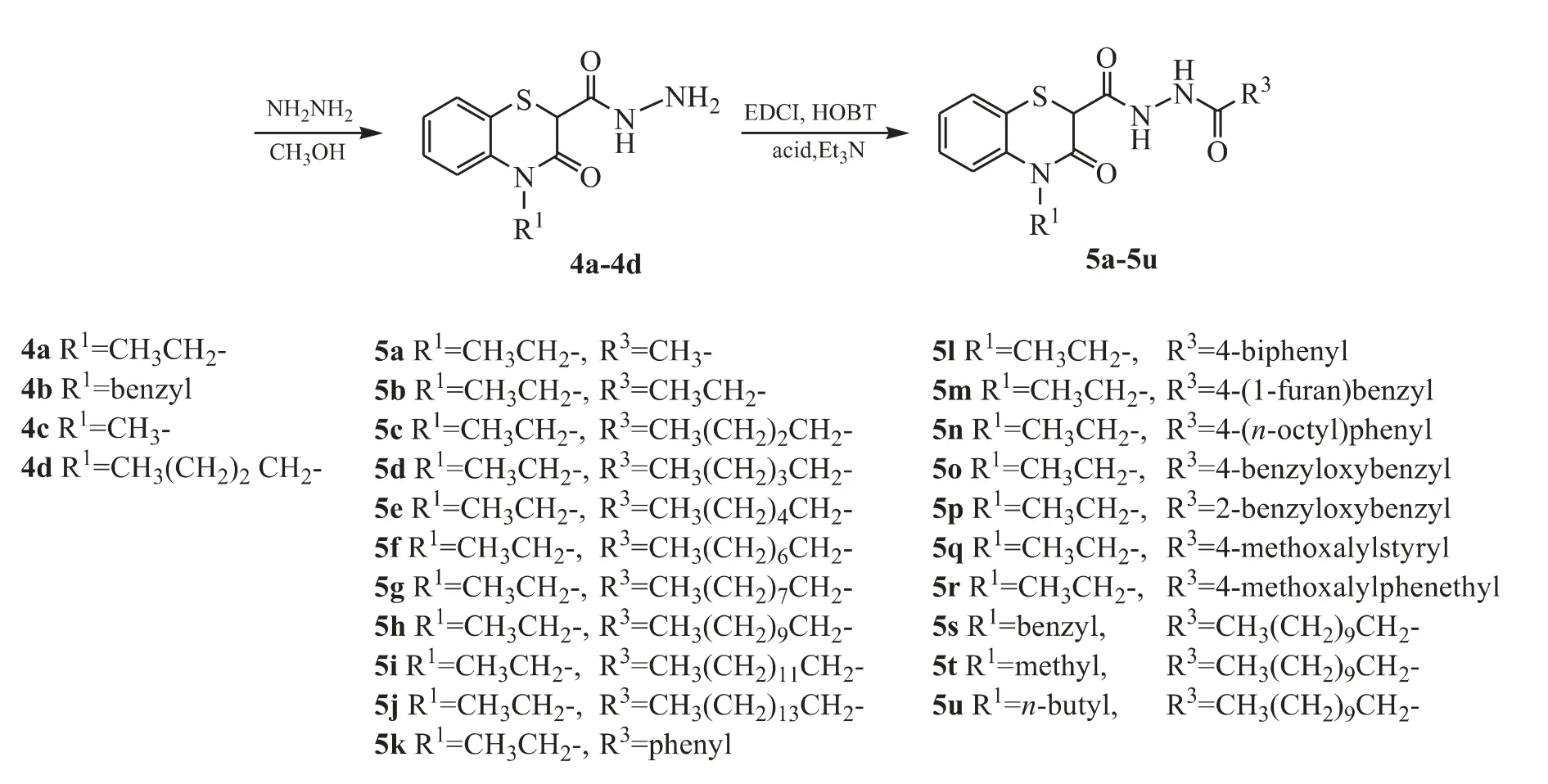
Continued Figure 2
2 合成实验
化合物熔点由上海精密科学仪器有限公司生产的SGWX -4 型熔点仪测定,温度未经校正;质谱由Agilent 1100s 质谱仪测定;核磁共振谱由Bruker AMX -400 型核磁共振仪测定,TMS 为内标,工作频率400 MHz。柱色谱用51 ~70 μm 硅胶由上海上邦实业有限公司生产;TLC 硅胶板由烟台市芝罘黄务硅胶开发试验厂生产。实验所用溶剂均为化学纯或分析纯。
2.1 2a ~2d 的通用制备方法
5.0 g(30.3 mmol)化合物1 和12.5 g (90.9 mmol)碳酸钾溶于250 mL 无水N,N-二甲基甲酰胺(DMF)中,搅拌下加入相应卤代物36.3 mmol,室温搅拌过夜,TLC 检测原料1 基本消失,停止反应。加等体积的水,乙酸乙酯(200 mL ×3)萃取,合并有机层,饱和食盐水洗涤3 次,无水硫酸钠干燥,硅胶柱色谱分离(石油醚-乙酸乙酯),得微黄色晶体或油状物2a ~2d,收率68% ~78%。
2.2 3a ~3e 的通用制备方法
将3.9 mmol 化合物2a ~2d 和质量分数60%的氢化钠0.44 g(7.8 mmol)加入到100 mL三颈瓶中,氮气保护,放置冰浴中搅拌下加入无水N,N-二甲基甲酰胺(DMF)100 mL,冰浴下继续搅拌0.5 h,反应液由微黄色变为玫红色,然后加入碳酸二甲酯(DMC)7.8 mmol,之后撤去冰浴,室温下反应约5 h,停止反应。滴加饱和氯化铵水溶液除去未反应的氢化钠,然后加等体积水,乙酸乙酯(100 mL ×3)萃取,合并有机层,饱和食盐水洗涤3 次,无水硫酸钠干燥,硅胶柱色谱分离(石油醚-乙酸乙酯),得油状物3a ~3e,收率55% ~78%。
2.3 4a ~4d 的通用制备方法
将3.2 mmol 中间体3a ~3d 溶于25 mL 甲醇中,然后加入质量分数85% 水合肼2.48 mL(64 mmol),回流过夜。蒸干溶剂,适量甲醇洗涤,得白色固体4a ~4d,收率71% ~88%。
2.4 5a ~5u 的通用制备方法
将477.5 μmol 羧酸溶于10 mL 乙腈,然后加入1-羟基苯并三唑(HOBT)477.5 μmol,搅拌15 min 后依次加入1-乙基-3-(3-二甲胺丙基)碳二亚胺盐酸盐(EDCI)65 mg(477.5 μmol)、三乙胺(Et3N)110 μL(795 μmol)及中间体4a ~4d 100 mg(398 μmol),室温搅拌24 h。停止反应后,减压蒸馏除去溶剂,残留物用饱和碳酸钠水溶液超声洗涤,过滤,干燥后用乙腈洗涤,再干燥即得相应目标产物,收率10% ~80%(对于溶解度较好的产物则用石油醚-乙酸乙酯硅胶柱色谱分离)。
合成的22 个目标化合物的理化常数及波谱数据见表1。
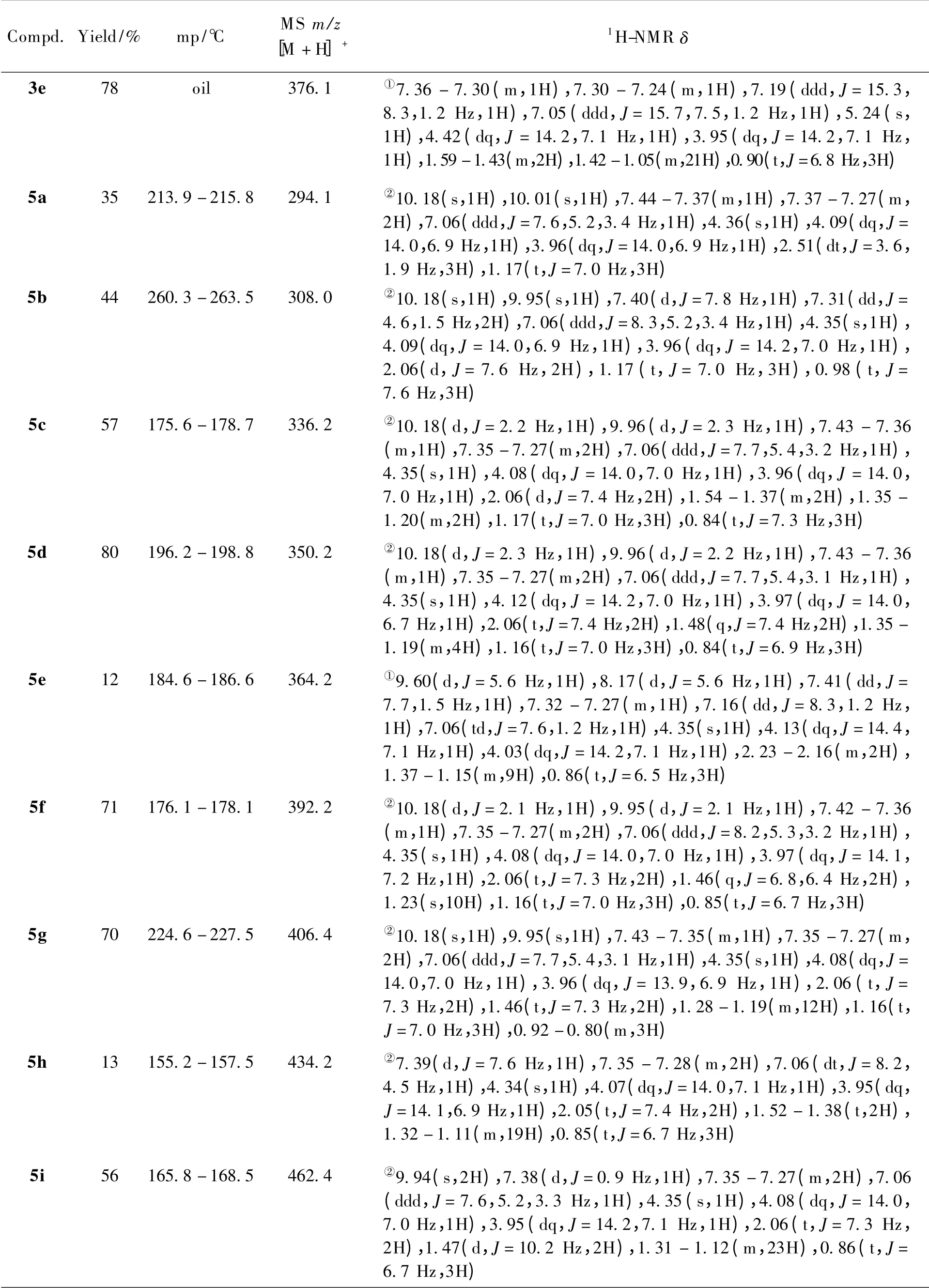
Table 1 The yield,melting point,MS and NMR data of the target compounds

Continued Table 1
3 活性实验
3.1 基于化学发光法的体外酶抑制活性测试
化合物的GSK-3β 抑制活性的测试是基于Baki 的Kinase-Glo 测试方法,用96 孔板在缓冲溶液中进行测试[10]:4 μL 不同浓度化合物的DMSO 溶液用14 μL 缓冲溶液稀释,然后在每孔中加入2 μL(20 ng)酶溶液,之后再加入含有12.5 μmol·L-1底物和4 μmol·L-1ATP 的缓冲溶液。30 ℃下孵育30 min,然后用40 μL Kinase-Glo 试剂终止酶反应。10 min 后记录其化学发光强度。根据ATP 总量和消耗ATP 量的比例计算出抑制活性。空白对照不加化合物,其抑制活性为100%。IC50是与空白对照相比,降低酶活性50%时的化合物浓度。所有目标化合物的IC50值见表2 所示。

Table 2 GSK 3β inhibitory activities of target compounds
3.2 化合物作用模式
化合物的抑制作用模式通过酶动力学实验确证,同样基于化学发光法进行测试,测试化合物与ATP 的相关性时,待测化合物浓度选择为其IC50的2 ~3 倍,同时保持酶底物GS-2(糖原合成酶-2)的浓度不变(6.25 μmol·L-1),分别测试在不同ATP 浓度(0.5、2、4、8 μmol·L-1)下化合物的酶抑制活性,然后采用Lineweaver-Burk 作图法,根据直线的相交点来确定化合物的作用类型。直线交于y轴,抑制剂为ATP 竞争型;直线交于x轴,则抑制剂为非ATP 竞争型。同理,在测试化合物和底物GS-2 的关系时,ATP 浓度保持不变(2 μmol·L-1),而底物GS-2 的浓度分别为0.78、1.56、3.13、6.25 μmol·L-1。
活性最好的化合物5h 的酶动力学测试结果如图3 所示(图中v代表酶促反应速率)。研究表明5h 的抑制作用既不与ATP 竞争,也不与底物竞争,因此推测5h 可能与VP 0.7 一样是作用于GSK-3β 的变构位点。
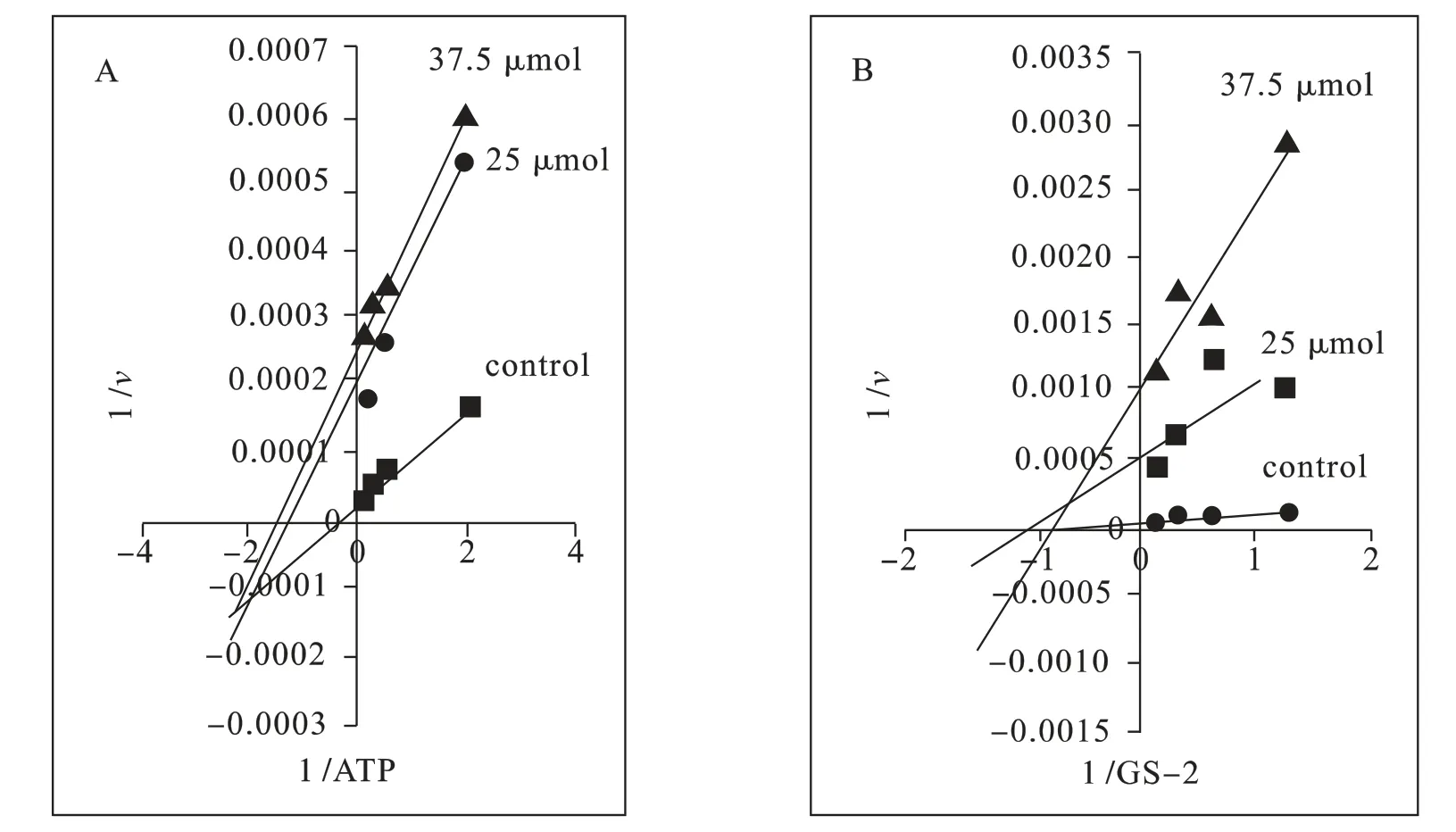
Figure 3 Kinetic data determined for the compound 5h
4 结果与讨论
4.1 GSK 3β 体外酶抑制活性
本文首先在苯并噻嗪酮骨架2 位上引入一个与VP 0.7 相同的疏水侧链(正十二酰基)得到目标化合物3e,该化合物与HZjb 相比IC50明显提高,达到了34.6 μmol·L-1,这初步表明长疏水侧链对化合物活性具有比较重要的影响。
随后,在化合物3e 中插入具有氢键给体和受体的酰肼基团,得到化合物5h,该化合物活性又提高了约3 倍,IC50达到了11.9 μmol·L-1。鉴于长疏水侧链对活性的重要影响,本文还考察了疏水侧链长度与化合物活性之间的相关性,以期找到最佳长度的侧链。因此设计合成了化合物5a ~5j,侧链长度在n=0 ~14。从活性数据可以看出,该类化合物的活性与疏水侧链长度之间的确有一定的相关性,如图4 所示,侧链长度约为11,即n=10 时,化合物活性最好。

Figure 4 The relationship between the length of side chain and inhibitory activities
考虑到长烷基疏水侧链的代谢不稳定性,因而以疏水芳杂环取代部分或全部疏水侧链进行初步的优化,以改善化合物的代谢性质。以苯基取代疏水侧链得到的化合物5k 活性消失,再增加一个芳杂环得到的化合物5l、5m 依然没有活性。但是在5k 苯基对位引入正辛基得到的化合物5n活性与5k、5l 及5m 相比明显提高,IC50值为25.9 μmol·L-1,这说明化合物侧链的长度和柔性对活性的影响都很大。化合物5o 的取代基由对位变为邻位得到的化合物5p 活性有所提高,说明活性化合物的疏水侧链很可能是以弯曲折叠的方式作用于特定的疏水空腔。化合物5q 含有一个柔性较差的较长共轭侧链,但没有活性。将该侧链的双键还原之后增加了化合物的柔性,活性也明显提高(IC50=72.0 μmol·L-1),表明侧链的柔性对化合物活性也有重要影响。
R1取代基对化合物活性也有一定影响。从活性数据可以看出,无论是较小的基团甲基取代(5t),还是较大的基团苄基(5s)、正丁基(5u)取代,化合物活性都会有所下降,R1为乙基时化合物活性最好。
4.2 化合物的动力学作用模式
对于化合物5h,首先是考察化合物的抑制活性与ATP 浓度的关系:从其双倒数图(图3A)可以看出各浓度直线相交于y轴之外,由此可知化合物5h 为非ATP 竞争型抑制剂,这符合作者的设计初衷。进一步考察化合物活性与酶底物GS-2 浓度的关系:从其双倒数图(图3B)可以看出,各浓度直线相交于x轴,由此可知化合物5h 是非底物竞争型抑制剂,这刚好初步印证了作者最初的设计思路,即该类含有长链的化合物很有可能作用于ATP 结合位点和底物结合位点之外的特异性变构位点。
综上所述,酶促动力学结果反映出5h 既不是作用于ATP 结合位点,也不是作用于底物结合位点,而是有可能作用于这二者之外的变构结合位点。但是这个推测有待进一步用计算化学方法和化学生物学方法验证。2 位长脂烃取代的苯并噻嗪酮类化合物作为一类新的GSK-3β 非ATP 竞争型抑制剂,值得进一步研究与开发。
[1] COHEN P,YELLOWLEES D,AITKEN A,et al.Separation and characterisation of glycogen synthase kinase 3,glycogen synthase kinase 4 and glycogen synthase kinase 5 from rabbit skeletal muscle[J].Eur J Biochem,1982,124(1):21 -35.
[2] WELSH G I,MILLER C M,LOUGHLIN A J,et al.Regulation of eukaryotic initiation factor eIF2B:glycogen synthase kinase-3 phosphorylates a conserved serine which undergoes dephosphorylation in response to insulin[J]. FEBS Lett,1998,421(2):125 -130.
[3] WELSH G I,PROUD C G. Glycogen synthase kinase-3 is rapidly inactivated in response to insulin and phosphorylates eukaryotic initiation factor eIF-2B[J].Biochem J,1993,294(3):625 -629.
[4] KAKU S,CHAKI S,MURAMATSU M. GSK-3 inhibitors:recent developments and therapeutic potential[J]. Curr Signal Transduct Ther,2008,3(3):195 -205.
[5] PEI J J,BRAAK E,BRAAK H,et al.Distribution of active glycogen synthase kinase 3β(GSK 3β)in brains staged for Alzheimer disease neurofibrillary changes[J]. J Neuropathol Exp Neurol,1999,58(9):1010 -1019.
[6] FERREIRA A,LU Q,ORECCHIO L. Selective phosphorylation of adult tau isoforms in mature hippocampal neurons exposed to fibrillar Aβ[J]. Mol Cell Neurosci,1997,9(3):220 -234.
[7] MARTINEZ A,ALONSO M,CASTRO,et al. First non-ATP competitive glycogen synthase kinase 3β(GSK-3β)inhibitors:thiadiazolidinones(TDZDs)as potential drugs for the treatment of Alzheimer's disease[J].J Med Chem,2002(45):1292 -1299.
[8] PALOMO V,CAMPILLO N E,MARTINZE A,et al.Exploring the binding sites of glycogen synthase kinase 3.Identification and characterization of allosteric modulation cavities[J].J Med Chem,2011,54(24):8461 -8470.
[9] VIEGAS-JUNIOR C,DANUELLO A,BARREIRO E J,et al. Molecular hybridization:a useful tool in the design of new drug prototypes[J].Curr Med Chem,2007,14(17):1829 -1852.
[10] BAKI A,BIELIK A,MOLNAR L,et al. A high throughput luminescent assay for glycogen synthase kinase-3β inhibitors[J]. Assay Drug Dev Technol,2007(5):75 -83.
——从偶然发现到合理设计