罗红霉素晶型分析及与溶解速率、溶出度的关系
王建,曾红霞,陈悦
(1.浙江工业大学,杭州 310014;2.浙江省食品药品检验研究院,杭州 310004)
罗红霉素晶型分析及与溶解速率、溶出度的关系
王建1,2,曾红霞1,陈悦2*
(1.浙江工业大学,杭州 310014;2.浙江省食品药品检验研究院,杭州 310004)
目的 对罗红霉素的晶型进行分析,并探讨不同晶型对罗红霉素溶解速率、溶出度的影响。方法 晶型分析采用X射线粉末衍射法和红外光谱法,溶解速率和溶出度测定采用转篮法,转速为100 r·min-1。结果 3种罗红霉素的结晶为3种不同的晶型,不同晶型的罗红霉素溶解速率和溶出度有一定差异。结论 为罗红霉素用药的有效性提供了科学依据。
罗红霉素;晶型;溶解速率;溶出度;X射线粉末衍射法;红外光谱法
药物晶型是影响药品溶解、溶出和吸收的重要因素[1-3],因此选择罗红霉素晶型分析及与溶解速率、胶囊溶出度的关系开展探索性研究。罗红霉素结晶工艺中,重结晶溶剂有甲醇、丙酮。按中国药典2010年版起草红外光谱测定时,发现上海现代哈森(商丘)药业有限公司和天津太平洋制药有限公司的样品与主流产品的晶型不一致。本次国评用X射线粉末衍射法和红外光谱法,分析并比较罗红霉素3种结晶,并探讨不同晶型对罗红霉素原料药溶解速率、胶囊溶出度的影响[4-8],为确保罗红霉素有效用药提供科学依据。
1 仪器与试药
X’Pert PRO型X射线衍射仪[XRD,荷兰PANalytical(帕纳科)公司];Tensor 27 傅立叶红外光谱仪(德国Bruker光谱仪器公司);天津大学ZRS智能型药物溶出仪(天津市天大天发科技有限公司);罗红霉素溶解速率测定用100目转蓝(自制)。
样品来源:浙江震元制药有限公司,罗红霉素(甲醇结晶),批号:12041641;上海现代哈森(商丘)药业有限公司,罗红霉素(甲醇结晶),批号:120315;上海现代哈森(商丘)药业有限公司,罗红霉素(丙酮结晶),批号:111205。按上海现代哈森(商丘)药业有限公司罗红霉素胶囊处方,制备罗红霉素胶囊。罗红霉素对照品(中国食品药品检定研究院,批号:130557-201103,纯度:74.7%)。
2 方法与结果
2.1 3种罗红霉素结晶X射线粉末衍射法和红外光谱法研究
2.1.1 3种罗红霉素结晶红外光谱图测定 取浙江震元制药有限公司生产的罗红霉素(甲醇结晶)、上海现代哈森(商丘)药业有限公司生产的罗红霉素(甲醇结晶)和提供的非生产工艺罗红霉素(丙酮结晶),测定红外光谱图,结果显示同为甲醇结晶但工艺有差别的两家公司生产的罗红霉素,在3 500 cm-1位置红外光谱图有差异,提示为2种不同的晶型,结果见图1。
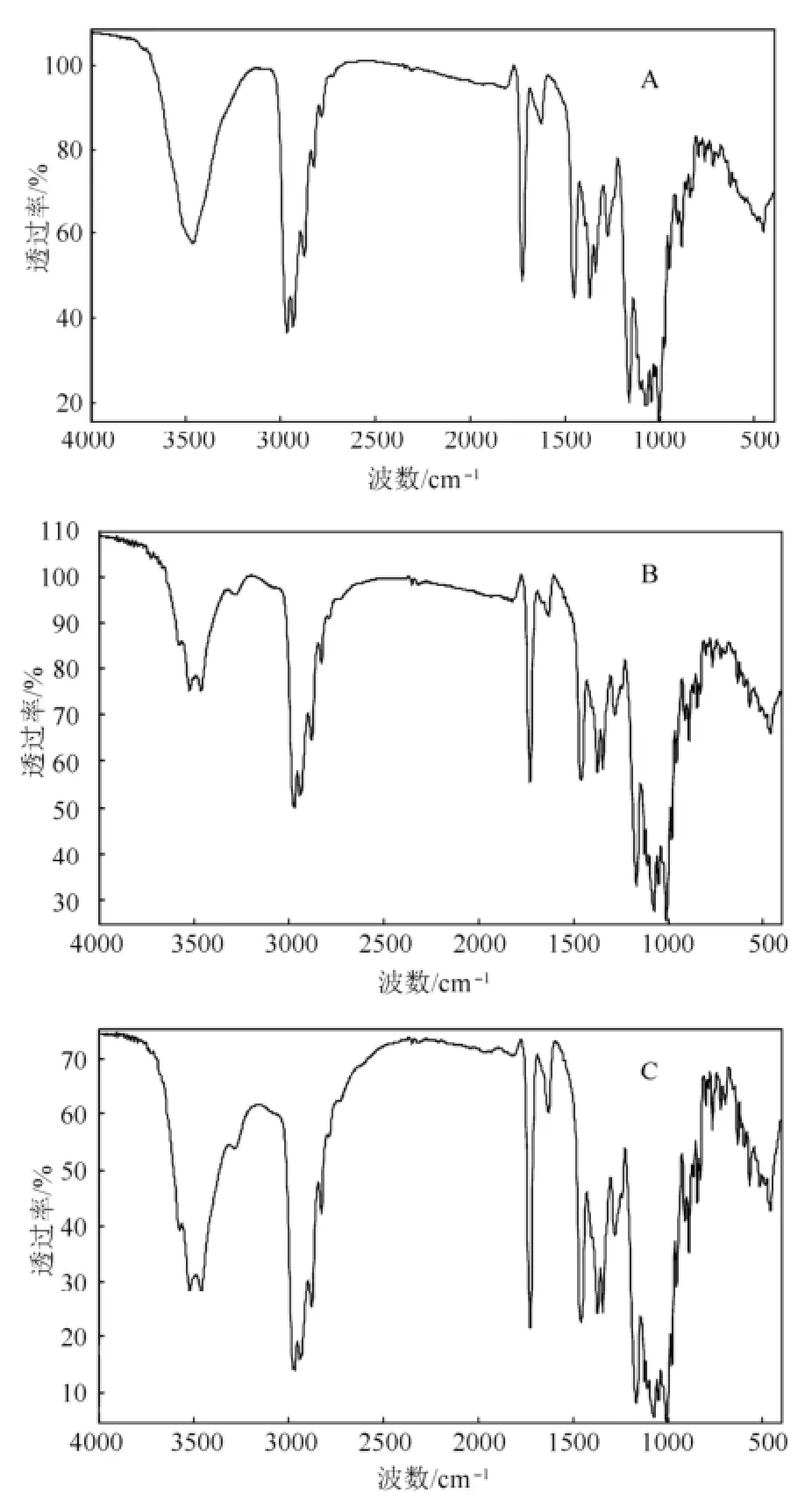
图1 罗红霉素3种结晶红外光谱图A-上海现代哈森(商丘)药业有限公司生产的罗红霉素(甲醇结晶);B-浙江震元制药有限公司生产的罗红霉素(甲醇结晶);C-上海现代哈森(商丘)药业有限公司提供的罗红霉素(丙酮结晶)Fig 1 Roxithromycin infrared spectra of 3 kinds of crystallization A-roxithromycin made by Shanghai Modern Hasen(Shangqiu) Pharmaceutical Company Limited through methanol; B-roxithromycin made by Zhejiang Zhenyuan Pharmaceutical Corporation through methanol; C-roxithromycin made by Shanghai Modern Hasen(Shangqiu) Pharmaceutical Company Limited through acetone
2.1.2 3种罗红霉素结晶X射线粉末衍射法测定取浙江震元制药有限公司生产的罗红霉素(甲醇结晶)、上海现代哈森(商丘)药业有限公司生产的罗红霉素(甲醇结晶)和提供的非生产工艺罗红霉素(丙酮结晶),用X射线粉末衍射法测定。X射线源为Cu靶Kα射线(λ=0.154 056 nm),电压40 kV,电流40 mA,测得结果显示3个结晶的X射线粉末衍射图均不相同,为3种不同的晶型,甲醇结晶的罗红霉素与丙酮结晶的罗红霉素差异较大,同为甲醇结晶但工艺有差别的上海现代哈森(商丘)药业有限公司和浙江震元制药有限公司生产的罗红霉素,X射线粉末衍射图也有差异,说明为2种不同的晶型。制剂制备工艺涉及碾磨可能会导致药物晶型变化,所以测定了制剂过程中经过碾磨的罗红霉素X射线衍射图(图2D),以考察制剂工艺是否引起晶型改变,结果显示图2(A)和图2(D)的X射线衍射图基本一致,说明此制剂工艺没有引起晶型改变。结果见图2。
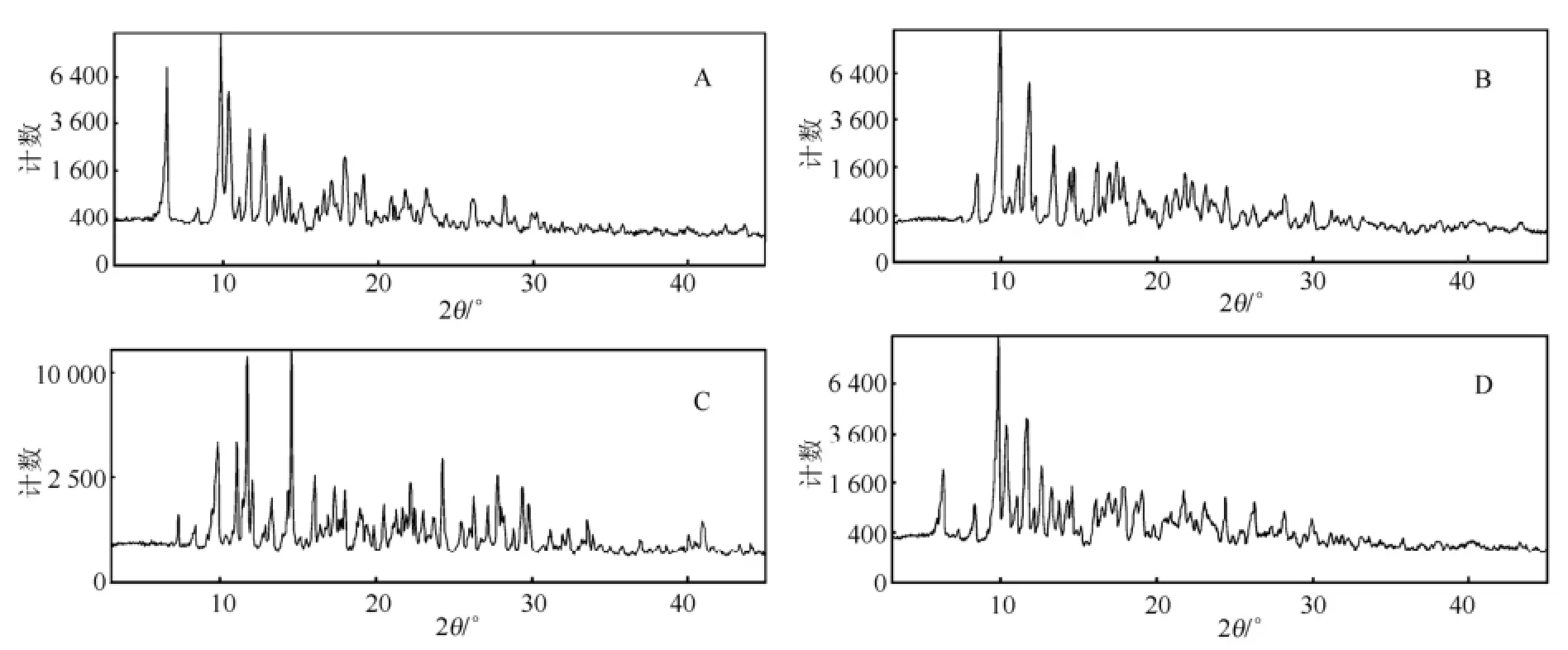
图2 罗红霉素3种结晶X射线粉末衍射图A-上海现代哈森(商丘)药业有限公司生产的罗红霉素(甲醇结晶);B-浙江震元制药有限公司生产的罗红霉素(甲醇结晶);C-上海现代哈森(商丘)药业有限公司提供的罗红霉素(丙酮结晶);D-上海现代哈森(商丘)药业有限公司生产罗红霉素(甲醇结晶,经过制剂过程中碾磨)Fig 2 Roxithromycin X ray powder diffraction pattern of 3 kinds of crystal A-roxithromycin made by Shanghai Modern Hasen(Shangqiu) Pharmaceutical Company Limited through methanol; B-roxithromycin made by Zhejiang Zhenyuan Pharmaceutical Corporation through methanol; C-roxithromycin made by Shanghai Modern Hasen(Shangqiu) Pharmaceutical Company Limited through acetone; D-roxithromycin made by Shanghai Modern Hasen (Shangqiu) Pharmaceutical Company Limited through methanol and milling
2.2 3种晶型罗红霉素原料药溶解速率和相应的胶囊溶出度测定
2.2.1 原料药溶解速率和胶囊溶出度测定方法[4-8]
按中国药典2010年版二部罗红霉素胶囊溶出度检查第一法测定,罗红霉素原料药溶解速率测定用100目转篮(自制)。
色谱条件:色谱柱:岛津 ShimVP-ODS (4.6 mm×250 mm,5 µm)柱;流动相:0.067 mol·L-1磷酸二氢铵(用三乙胺调节pH至6.5)-乙腈(65∶35);流速:1.0 mL·min-1;检测波长为:210 nm;进样量:20 µL。
2.2.2 原料药溶解速率和胶囊溶出度测定 取3种晶型罗红霉素原料药及相应制得的胶囊剂,原料药测定溶解速率,胶囊测定溶出度。照溶出度测定法(中国药典2010年版二部附录XC第一法),以醋酸盐缓冲液(pH 5.5)为溶出介质,转速为100 r·min-1,依法操作,在5,10,20,30,45 min时,分别取溶液5 mL,滤过,并及时在操作容器中补充上述溶剂5 mL。另取罗红霉素对照品适量,精密称定,用上述溶出介质溶解并稀释制成每1 mL中含0.16 mg的溶液,作为对照品溶液。按“2.2.1”色谱条件,精密量取上述2种溶液各20 μL,注入液相色谱仪,记录色谱图,按外标法以峰面积计算出每粒的溶出量。HPLC的色谱图见图3,溶出度结果见图4~5。
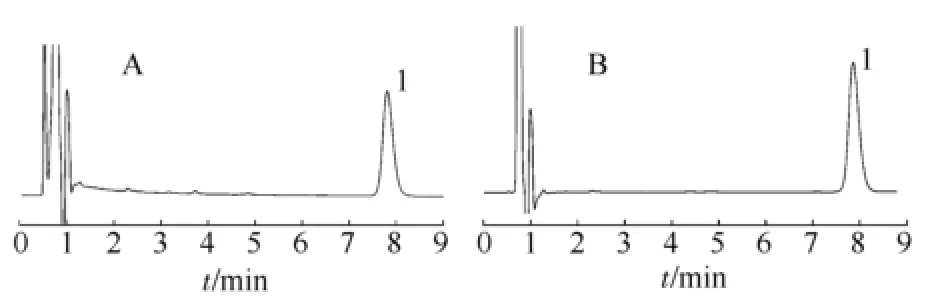
图3 样品和对照品HPLC色谱图A-样品;B-对照品;1-罗红霉素Fig 3 Chromatograms of roxithromycin sample and reference substance A-sample; B-reference; 1-Roxithromycin
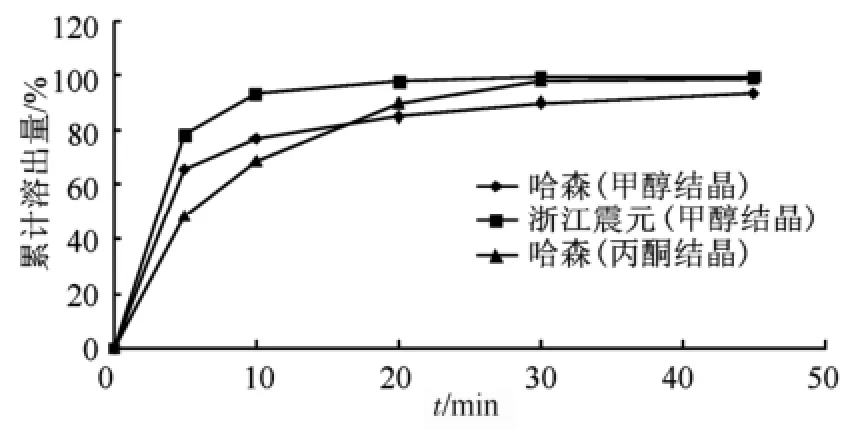
图4 罗红霉素原料药溶解速率曲线Fig 4 The dissolution rate curve of roxithromycin
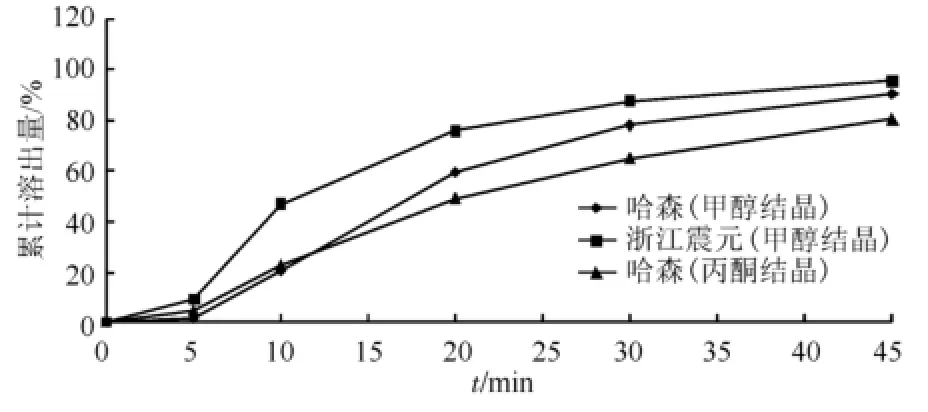
图5 罗红霉素胶囊溶出曲线Fig 5 The dissolution curve of roxithromycin capsule
3 讨论
本实验用X射线粉末衍射法和红外光谱法,分析并比较了罗红霉素的3种结晶,图1和图2显示3个结晶的X射线粉末衍射图均不相同,为3种不同的晶型。
从图4~5可知,丙酮结晶的罗红霉素溶出慢,溶出度较差;甲醇结晶的二种晶型溶出快、溶出度好,溶出度均在90%以上。提示不同晶型的罗红霉素溶出度有一定差异。
REFERENCES
[1] HUANG S H, LONG X Y, YUAN F, et al. Correlativity between solubility O/W partition coefficients of berbenine hydrochloride and intestinal absorption in rats in situ [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2012, 29(3): 233-238.
[2] XIONG Y K, LIANG S, DU Y, et al. HPLC determination of equilibrium solubility and apparent oil/water partition coefficient of senkyunolide I [J]. Chin J Pharm Anal(药物分析杂志), 2012, 32(9): 1644-1647.
[3] LI Z W. Methods for the analysis of drug crystal forms [J]. Chin J Vet Med(中国兽药杂志), 2006, 40(1): 45-48.
[4] LOTTER A P, FLANAGANJR D R, PALEPU N R, et al. A simple reproducible method for determining dissolution rates of hydrophobic powders [J]. Pharm Technol, 1983(4): 56-66.
[5] CHENG X F, ZHAO C J. HPLC for determination of dissolution of roxithromycin [J]. J Prac Med Pharm(实用医药杂志), 2004, 21(9): 818-819.
[6] CHENG Y M, LIN L, CHENG Y P, et al. Study on the dissolubility of roxithromycin capsules and tables from different manufactures [J]. Fujian Med J(福建医药杂志), 2005, 27(3): 132-134.
[7] WANG S M, ZHAO S F, WANG C P. Study on the dissolubility of roxithromycin capsules [J]. J Hebei Med Univ(河北医科大学学报), 2001, 22(1): 24-25.
[8] WANG J, MONG Z. Development of the dissolution methods for roxithromycin granules and roxithromycin for suspension by HPLC [J]. Chin J Antibiot(中国抗生素杂志), 2009, 34(8): 489-492.
Relationship of Roxithromycin Crystal Types, Dissolution Rates and Dissolution
WANG Jian1,2, ZENG Hongxia1, CHEN Yue2*
(1.Zhejiang University of Technology, Hangzhou 310014, China; 2.Zhejiang Institute for Food and Drug Control, Hangzhou 310004, China)
OBJECTIVE To study the crystal types of roxithromycin, and the relationship of roxithromycin crystal types and its dissolution rate and dissolution. METHODS X-ray powder diffraction and infrared spectroscopy were used in the analysis of crystal types. The dissolutive apparatus was used with 100 r·min-1. RESULTS The result showed that three crystalsof roxithromycin were different crystal types, and the dissolution rates and dissolutions of different crystal types had some differences. CONCLUSION The study provids a scientific basis for the effectiveness of roxithromycin.
roxithromycin; crystal type; dissolution rate; dissolution; X-ray powder diffraction; infrared spectroscopy
R994.11
B
1007-7693(2013)10-1094-04
2013-03-01
2012年国家药品评价性抽验项目
王建,男,博士,主任药师,博导 Tel: (0571)86459458 E-mail: wangjianhw2000@aliyun.com*
陈悦,男,主任药师 Tel: (0571)86459427 E-mail: 13868057010@163.com

