110例药品不良反应汇总分析
耿晓宁 邵春月
(泰山医学院附属泰山医院,山东 泰安 271000)
1 资料与方法
对2012年我院上报的110例药物不良反应(adverse drug reaction,ADR)报告进行回顾性分析及讨论,采用描述性研究方法[1],对110例ADR 报告的一般情况、用药途径、药物种类、临床表现、上报人科室及职业等进行统计、分析。
2 结果与分析
2.1 不良反应的类型
将药品不良反应按照反应程度分为一般和严重(包括死亡)、已知和新的,各统计例数和所占百分比,见表1。

表1 按不良反应类型分类表
将上报例数、新的严重的例数与历年数据做对比,2012年上报的ADR例数、新的严重的ADR例数及所占比例均居历史最高位,详见图1。
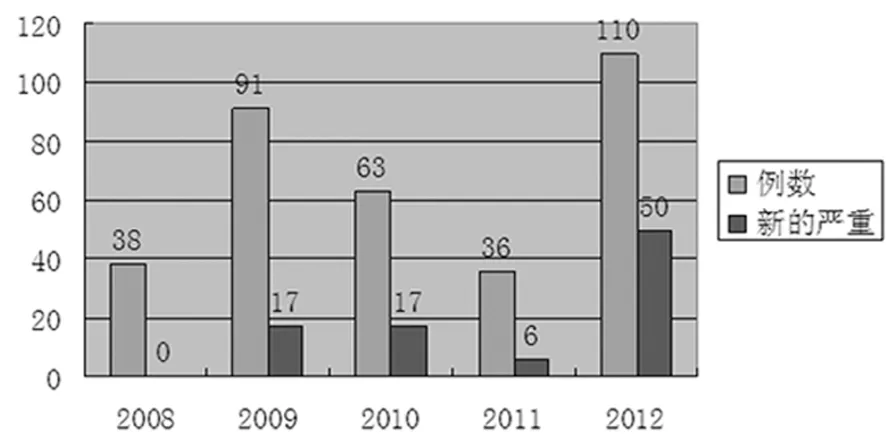
图1 历年ADR上报例数对比
注:2008年新的严重的例数数据缺失。新的严重的包括新的一般的病例和严重的病例。
2.2 参与不良反应上报的科室及人数
2012年全年共有15个科室上报ADR,31人参与上报工作。将参与上报科室和人数与历年数据对比,2012年参与上报工作的科室和人数居历史高位,详见图2。

图2 历年上报科室及人数对比
2.3 不良反应上报趋势
将不良反应上报例数按月份进行统计,将数据进行对比,夏季ADR发生率有所提高,11、12月上报例数明显高于其他月份,见图3。
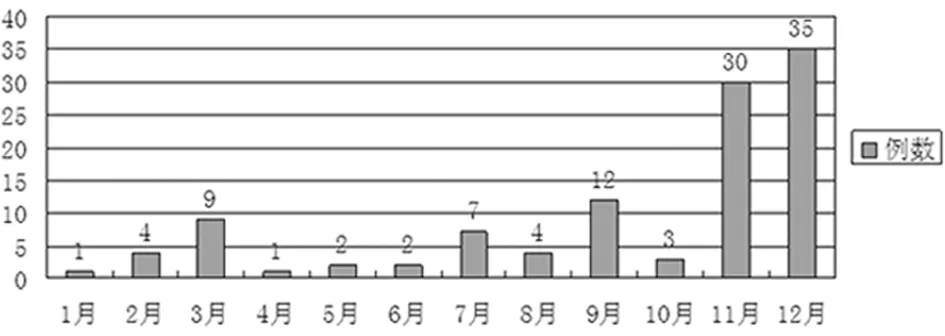
图3 全年ADR上报趋势
2.4 报告人职业和科室分布
报告人包括医生、护士和药师,其中医生上报38例,占35%;护士上报3例,占3%;药师上报69例,占62%。药师在ADR上报工作占主导地位。2012年全年共有15个科室上报ADR,31人参与上报工作,详见表2。
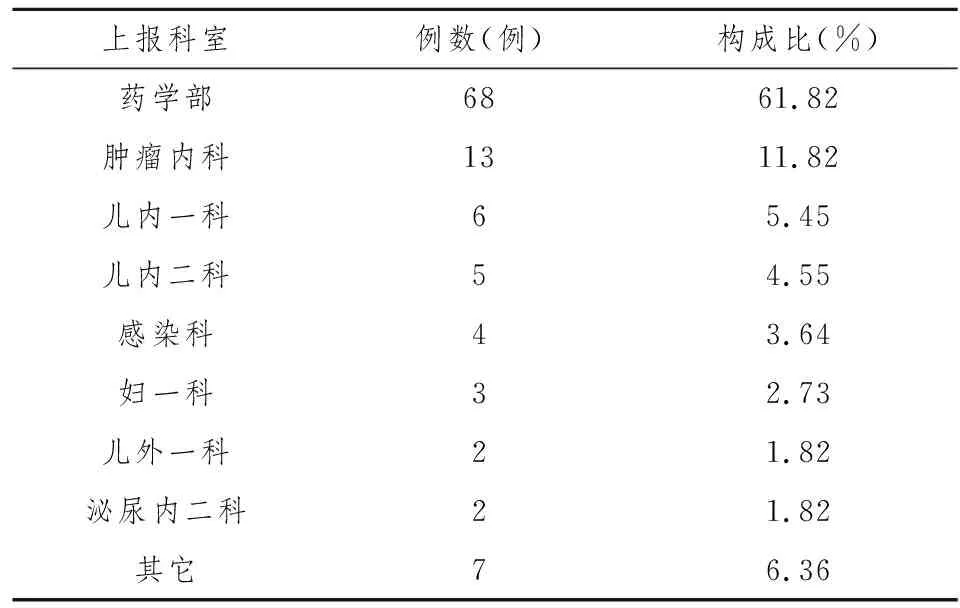
表2 ADR报表科室分布
2.5 病例报告人口学特征
110例ADR报告中,男性57例,占52%,女性53例,占48%。14岁以下及45岁以上年龄段为ADR高发年龄段,年龄构成详见表3。
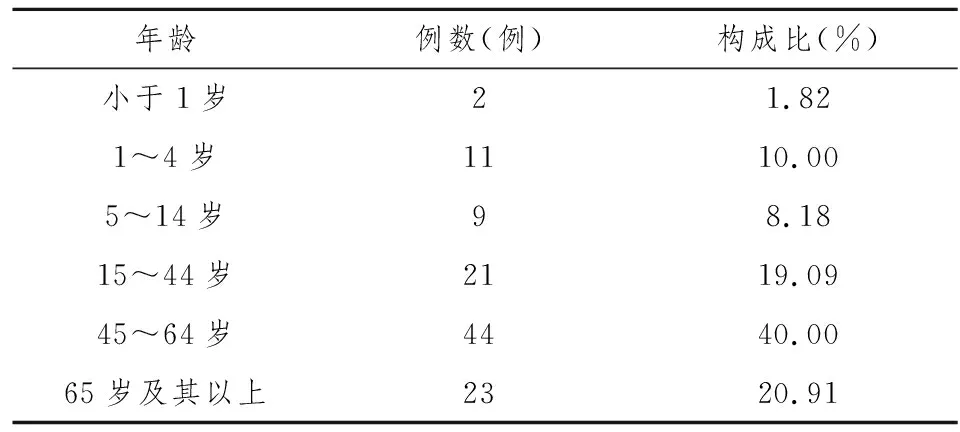
表3 患者年龄分布(按医学年龄)
2.6 用药情况分析
2.6.1引起ADR的药品按药理学分类 引起ADR的药物前5名为:抗肿瘤药物、抗菌药物、中成药制剂、生物制剂、维生素类药物,详见图4。
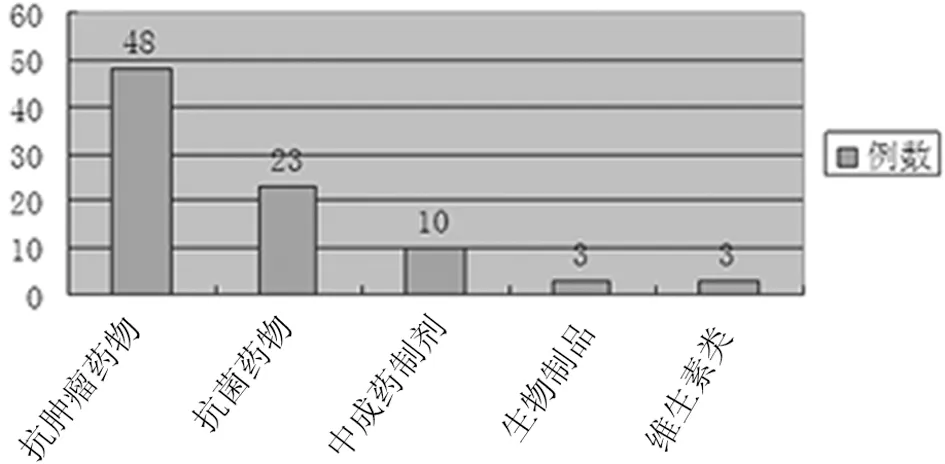
图4 按药理学分类前5名
2.6.2引起ADR的药品的给药途径 将110例病例按给药途径分类统计,并按类型统计例次和所占百分比,静脉滴注的给药方式发生ADR的比例最高,详见表4。
2.7 不良反应所涉及的系统/器官
将ADR按所涉及系统/器官分类统计,并按前10名排序,主要涉及的系统/器官为皮肤、血液学和胃肠道系统,详见图5。
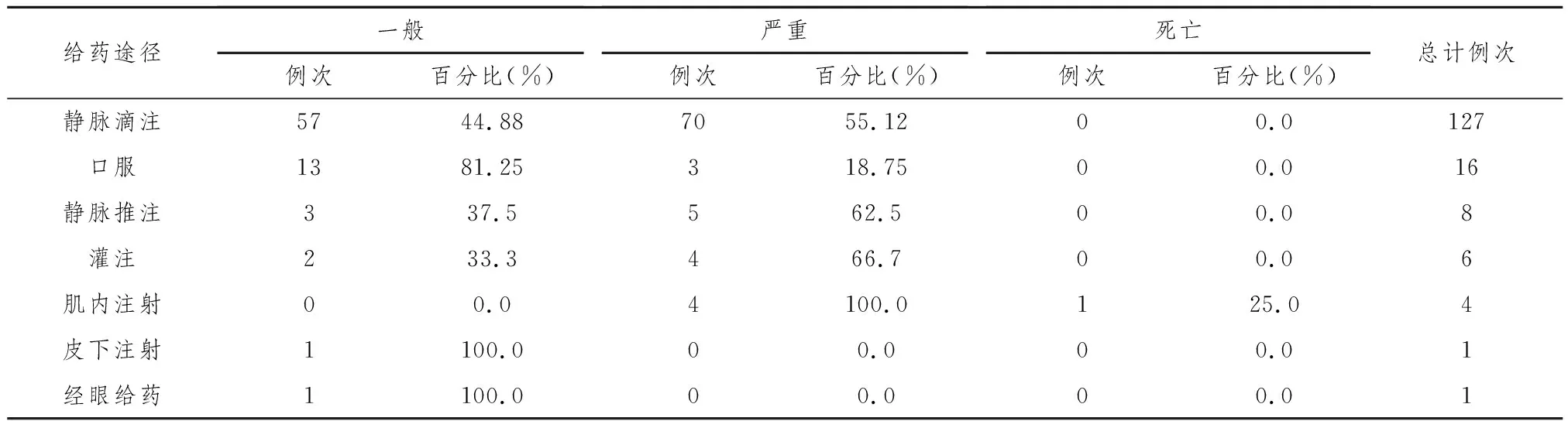
表4 按给药途径分布表
注:一例ADR病例中有多种怀疑用药、多种给药途径。
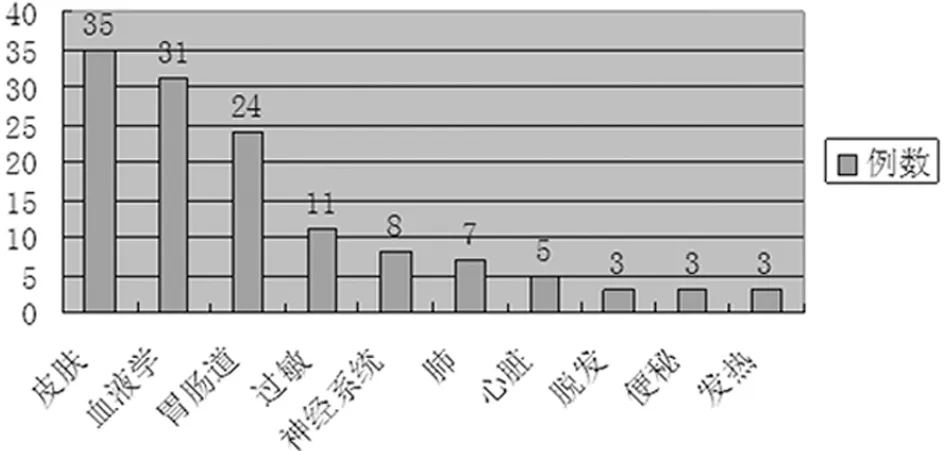
图5 按ADR涉及系统/器官排名表
注:分类参照WHO抗癌药物急性及亚急性毒性反应分度标准。
2.8 不良反应结果
将110例ADR按结果分类统计,其中好转53例,占48%;痊愈33例,占31%;未好转20例,占19%;不详1例,占1%;死亡1例,占1%。未好转病例多为报告时治疗未结束,不详病例为门诊病例,无法得知ADR结果,死亡病例为注射复方氨林巴比妥注射液后5 min后,因过敏性休克,心率下降,呼吸衰竭,抢救无效而死亡。
3 讨 论
3.1 人口学特征对药品不良反应发生率的影响
从患者性别分布分析,男性占52%,女性占48%,两者并无明显差异性,可见性别对ADR发生率并无明显影响。从患者年龄分布(表6)分析,14岁以下患者构成比为20%,45~60岁患者构成比为40%,65岁以上年龄段的患者构成比达20.91%,可见儿童和中老年患者ADR发生率较高。由于110例患者中肿瘤患者有50例,占到45.45%,而45~60岁年龄段为肿瘤高发年龄段,故这一年龄段ADR发生率较高, ADR多为抗肿瘤药物及其辅助用药所引发。65岁以上老年人 ADR发生率较高的原因可归结为:⑴ 老年人的肝、肾功能下降,导致药物在体内的代谢、排泄能力下降,药物蓄积[2-3];⑵ 老年人多患老年慢性疾病[4],在就诊时,常忘记向医生说明自己正在服用的药物,而导致重复用药或药物间相互作用。14岁以下儿童 ADR发生率较高的原因可归结为:⑴由于儿童各器官生理功能尚未成熟,免疫功能低下,对外界侵袭的防御能力较差,因此比成人更易罹患疾病;⑵由于儿童的药物代谢酶分泌不足或缺少,肾功能发育不完善,药品清除能力差,对药品的敏感性较高,故极易发生ADR[5]。⑶各年龄段儿童的身高、体质量、体表面积、组织器官、内脏功能等差别很大,其药物动力学和药效学过程极具特殊性。所以,对于儿童和老年患者,应慎重选择药物、选定剂量,避免药物相互作用。
3.2 给药途径对药品不良反应的影响
110例ADR报告中,77.91%的药物给药途径为静脉滴注,4.91%的药物给药途径为静脉推注,静脉给药引起不良反应远高于其他给药途径[6-7]。静脉给药产生ADR 的间接诱因较多,如内毒素、pH 值、渗透压、微小粒子等[8],所以,除临床上应根据患者病情正确选择给药途径外,同时还应加快多种给药途径的研究,以期找到既符合临床治疗要求,又可有效降低ADR发生率的给药途径。
3.3 不同药品对药品不良反应的影响
引起ADR的药物前3名为:抗肿瘤药物、抗菌药物、中成药制剂。由于近些年来如粒细胞刺激因子、5-HT3受体拮抗剂等各种辅助用药的问世,使抗肿瘤药物的用量大大突破了之前的界限,使肿瘤患者对抗肿瘤药物的耐受性进一步提高,但并不代表ADR的发生率大幅下降,患者仍要面对抗肿瘤药物不良反应所带来的痛苦,虽然绝大多数患者经治疗可好转或痊愈,但仍有相当一部分患者治疗效果不佳。除个体差异因素的区别外,多周期用药的毒性蓄积、患者免疫能力的持续下降、精神因素等等也是造成治疗效果不佳的症结所在。由抗菌药物引起的ADR中,以头孢菌素类[9]、喹诺酮类[10]及青霉素类为主,这些药物均为临床常用、已知毒副作用较小、安全性较高的药品,但有报道指出,临床上报的不良反应报告中,超适应症、超剂量用药[11]的情况屡有发生。因此,合理使用抗菌药物应引起重视。中成药制剂则因成分复杂、提纯工艺不高、药物稳定性差等因素也极易引发ADR的发生。而由于临床试验数据缺乏,相关部门监管不力等因素,中成药制剂的药品说明书中对ADR的描述也往往含糊不清,也不利于对ADR的预防和监测。
从ADR发生所涉及的系统/器官分析,皮肤、血液学、胃肠道方面的ADR居前三位,与抗肿瘤药物、抗菌药物、中成药制剂的主要不良反应相吻合。皮肤反应数量居首的原因,一是因为其临床表现易于观察和诊断,且不易与其他疾病相混淆;二是药疹是变态反应所致,目前临床上的一些常用药物,如抗菌药物、解热镇痛药物、抗癫痫药物等,它们的抗原性较强,最易引起该类反应。尽管皮肤过敏反应发生率较高,但是病情较轻,一般予以停药或治疗症状即消失。血液学毒性反应数量居前则是因为化疗患者常规检查血常规,其程度有明确的检验结果支持,较容易做出诊断。胃肠道反应数量居前也是因为其临床症状较为明显,患者能够注意与医护人员沟通。
综上所述,药品不良反应发生率受人口学因素、给药途径、药品差异等多种因素影响,临床应用中应以患者为中心,充分发挥医、护、药多种职业的协同优势,加强防患意识,做好药品不良反应的监测和上报工作,为临床合理用药提供支持。
[1] 陈新谦,金有穆,汤光. 新编药物学[M]. 第15 版. 北京: 人民卫生出版社, 2003: 253-259.
[2] 魏娟娟,白玉国,魏国义. 我院339 例药物不良反应分析[J]. 中国医药, 2010,5(6) : 534-535.
[3] 陈富超,方宝霞,朱军,等. 302 例药物不良反应临床分析[J]. 中国医药, 2007,2(8) : 473-474.
[4] 李旭梅,涂厉标. 2006-2007 年我院药品不良反应报告比较分析[J]. 药学进展, 2009,33(1) : 38.
[5] 张志华,何周康,吴浩.药品说明书中有关儿童用药内容的调查[J].儿科药学杂志,2004,10(5):41.
[6] 张天栋,刘世峰. 药物不良反应146 例临床特点分析[J]. 中国医药,2010,5(2) : 174-175.
[7] 丁海燕,王浩. 药物不良反应587 例监测报告分析[J]. 中国医药,2009,4(7) : 526-527.
[8] 谢丽君,吴佳滨,张华. 我院2008 年药品不良反应报告总结[J]. 中国民族民间医药,2009,18(2):156.
[9] 王亚军. 头孢菌素类药物在儿科应用中的不良反应[J]. 中国医药,2009,4(7) : 559-560.
[10] 方宝霞,时晓亚,李鹏,等. 抗菌药物引起骨与关节疼痛169例分析[J]. 中国医药, 2010,5(7) : 627-628.
[11] 戚颖. 129 例抗菌药不良反应报告分析[J]. 中国现代药物应用,2009,3(1) : 65-67.

