做“好”实验,让学生感受化学的魅力
都海英
(南京市第九中学 江苏 南京 210018)
化学是一门实验科学,以实验为基础是化学教学的最基本特征。 在日常教学中,我尽可能让结论以实验结果的形式呈现,而不是直接陈述。 这样做的目的,不仅是要告诉学生化学研究过程中的结论并非凭空想象,而是有一定的事实依据,同时也传递给学生一种研究科学的态度和方法。
一、充分利用课本实验,让学生感受化学世界之真
课本实验无疑是非常重要的,同时我们还可以利用这些实验帮助理解其他更深层次的问题。 在钠的化合物中课本设计了“Na2CO3和NaHCO3的碱性对比”实验(使酚酞变红的颜色深浅), 这其实给我们讲授Na2CO3和酸的反应原理提供了很好的素材。 有些老师往往习惯跟学生直接做出理论解释:第一步:CO32-+H+=HCO3-;第二步:HCO3-+H+=H2O+CO2。 其实我们应该思考一下,怎么让学生相信第一步反应是产生了HCO3-呢? 我是这样来处理的:先做课本实验:向同浓度的Na2CO3和NaHCO3滴加等量的酚酞, 观察颜色。 Na2CO3溶液(试管I ) 深红,NaHCO3溶液(试管II)浅红。 然后向含有酚酞的Na2CO3溶液(试管I)中逐滴加稀盐酸,酚酞的红色由深变浅,和试管II 的浅红色NaHCO3溶液作比较, 颜色几乎相同。继续滴加稀盐酸,产生大量气泡,溶液的红色消失。

其实也就是用酚酞来指示整个实验的过程并判断反应的生成物, 这就让反应原理通过直观现象来呈现。此时学生不是被动接受老师的分析讲解,而是主动根据实验现象判断每步反应的生成物从而写出反应方程式,这种学习方式正是我们倡导的自主学习,只是通过实验的手段来完成自主学习的过程。
二、精心设计微型实验,让学生感受化学变化之美
在学习元素化合物知识时,有很多物质的性质是通过试管实验完成的。 如果老师按照课本要求来操作当然可以完成实验,但由于试管本身很小,坐在教室后排的同学就可能观察不清楚实验现象而影响实验效果,同时也不利于培养学生的动手能力,此时我们可以选择学生分组实验来完成,但是如果只是简单的把演示实验变成学生实验,必然要消耗大量的化学试剂,这并不符合绿色环保的理念,如果能设计一些有趣的微型实验,通过微型滴管滴几滴试剂就能观察明显的实验现象,这样的效果最佳。 在铁的化合物教学中我尝试用这样的方法取得了很好的效果。 整个实验只需要在一张滤纸上完成,每种溶液只需要一滴。
1. Fe3+和SCN-的反应
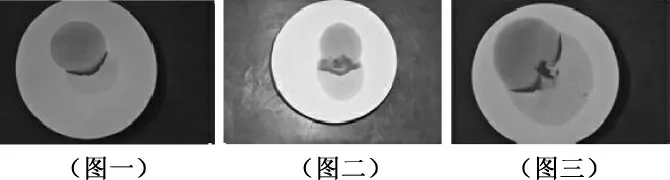
如下图所示:在一张滤纸上(滤纸放在表面皿上。 后同)分别滴一滴FeCl3和KSCN 溶液,两滴试剂靠近但不混合,(如图一、二)它们通过渗透接触,相遇的部分变成红色,并形成非常漂亮的“一线潮”景观(图三),实验完成。

2. Fe2+的检验:先加KSCN,后加氯水
在一张滤纸上依次滴一滴FeSO4、KSCN、氯水,三滴试剂靠近但不接触,(见图一、二、三)由图四可以看出:当溶液两两混合时不出现红色,只有当三溶液交汇时才会出现红色。 学生由实验现象得出两个结论:(1)Fe2+遇KSCN 不变红;(2)氯水可以氧化Fe2+变成Fe3+

3. Fe3+被铁粉还原
在一张滤纸上分别滴一滴FeCl3和KSCN,当两滴试剂接触时出现一线潮现象,(如图一)。 然后在红色区域加少许铁粉,等待片刻,铁粉周围的区域红色渐渐消失(图二),最终呈现图三的结果。 说明Fe3+被铁粉还原。
微型实验不仅弥补了演示实验的缺陷,还可以训练学生的动手操作能力以及思维能力。 学生自己由实验结果分析整合最后得出我们想要的结论,取得了非常好的效果。
三、用实验代替讲解,让学生体会化学实验之妙
化学实验对于解决学生易错难懂的问题同样有非常精妙的运用。 比如:苯和水混合后出现分层的现象能不能观察到,学生想象中认为两种都是无色液体应该看不到。 此时,我们只需要拿一根试管分别加入少量苯和水,就可以完成实验,学生们亲眼目睹明显的分层现象,有了一次体验和感受就不会再出现认识上的偏差。 又比如:氯化钙溶液中通入CO2是否有沉淀产生,学生们往往把它和澄清石灰水中通CO2混淆,老师们往往想当然的认为自己的分析很细致到位,但学生再次遇到此类问题时还是会出错,那我们不妨做个对比试验,学生首先能看到直观的结果:氯化钙溶液中通入CO2没有沉淀产生! 然后再由老师和学生一起来分析原因,效果就好得多。
总之, 化学实验在化学教学中的地位无可替代,我们不仅要充分利用课本实验进行知识迁移,同时还可以对课本实验的设计提出挑战,设计出更能锻炼学生思维和操作能力的实验,而当学生对知识的认知出现共性的问题时,我们也不妨试试能否用实验的手段来解决。 这就需要我们在平时的教学中能站在学生的角度多一些反思,多一些用心,多一些探索。

