化学计量学方法用于甘草和芫花及其药对的挥发性成分分析Δ
周 能,周 振,梁逸曾,曾楚杰
(1.玉林师范学院化学与材料学院,广西玉林537000;2.中南大学化学化工学院,长沙 410083)
化学计量学方法用于甘草和芫花及其药对的挥发性成分分析Δ
周 能1,2*,周 振1,梁逸曾2#,曾楚杰1
(1.玉林师范学院化学与材料学院,广西玉林537000;2.中南大学化学化工学院,长沙 410083)
目的:分析甘草和芫花单味药材及其药对的挥发性成分。方法:以正十四烷为内标,采用气相色谱-质谱联用技术对甘草、芫花的单味药材及其组成的药对的挥发性成分进行测定,利用多种化学计量学方法对产生的二维色谱/质谱数据同时进行分辨和解析,获取各个组分的纯色谱曲线和纯质谱,根据分辨得到的纯质谱在质谱库中进行相似检索以实现对组分的定性。利用转换移动窗口因子分析法对组合前后的成分进行归属分析,采用面积归一化法进行定量。结果:分别在甘草、芫花及其药对中鉴定出34、41和68个成分,占各自挥发油成分的90%、84%和75%。药对中挥发性成分的相对含量与单味药比较差异较大。结论:本试验结果可为中药配伍的研究提供较为重要的依据。
甘草;芫花;挥发油化学成分;药对;气相色谱-质谱联用技术;转换移动窗口因子分析法
甘草(Glycyrrhiza uralensis Fisch,GUF)是中医应用最为广泛的原料药[1]。在中药处方中,芫花(Daphne genkwa Sieb,DGS)是毒性药,其剂量被严格限制。在中国和朝鲜,DGS被用于治疗水肿、哮喘和癌症[2]。根据中药的基本药性理论[3],GUF与DGS不能共用于一个方中,但对其共用的物质基础没有进一步说明。有关GUF和DGS单味药化学成分的研究已有不少报道,但是GUF-DGS药对的物质基础缺乏系统的研究。本研究利用气相色谱-质谱(GC-MS)联用技术并结合化学计量学方法如直观推导式演进投影法(HELP)和转换移动窗口因子分析法(AMWFA)[4~6]对该药对的单味药与药对在煎煮过程中的物质及其变化作较为系统的探讨,GUF、DGS和其药对中的挥发性成分被分别提取,然后被GC-MS联用技术测定,所获得的二维数据利用化学计量学方法进行分辨,使得单味药和药对中的挥发性成分被鉴定和定量。结果显示,单味药和药对中挥发性成分的相对含量有了很大的变化。本试验对中药配伍的研究具有较为重要的意义。
1 仪器与试药
2010型GC-MS仪、MS工作站、NIST107型 MS库(日本岛津公司)。
正己烷(分析纯,苏州市第二化工研究所);正十四烷(色谱纯,美国Sigma公司)。GUF和DGS均购于广西玉林中药材专业市场,经湖南师范大学医学院赵冰清教授鉴定均为真品。
2 方法
2.1 挥发油的提取
GUF和DGS于60℃干燥3 h。称取GUF(30 g)、DGS(30 g)、GUF-DGS(30 g-30 g)样品,分别置于500 mL圆底烧瓶中,加水浸泡3 h后照挥发油测定法[7]提取挥发油,收集挥发油,转移至2 mL量瓶中,加入一定量的正十四烷(约0.2μL)作为内标,以正己烷稀释到刻度,4℃贮藏,备用,分析时取1μL进样。各种样品均重复做2份。
2.2 GC-MS测定条件
2.2.1 GC条件 色谱柱:OV-1毛细管柱(30 m×0.25 mm I.D.,0.25µm);进样口温度:280℃;载气:氦气;流速:0.70 mL·min-1;分流比:1∶1;程序升温(起始温度为60℃,保持4 min;以2℃·min-1的速度升至66℃,保持3 min;以2℃·min-1的速度升至70℃,保持3 min;以3℃·min-1的速度升至100℃,保持1 min;以4℃·min-1的速度升至130℃,保持2 min;以5℃·min-1的速度升至190℃,保持1 min;以3℃·min-1的速度升至220℃,保持1 min;以5℃·min-1的速度升至250℃);进样量:1.0μL。
2.2.2 MS条件 离子源:标准EI源(轰击能量:70 eV);离子源温度:280℃;接口温度:280℃;质量扫描范围:20~450 amu;扫描间隔:0.2 s/次;溶剂切除:4 min。
2.3 数据处理
所有数据分析均在Celeron(R)2.53 GHz(Intel)个人计算机上完成。采用峰面积归一化法确定各化合物的相对含量。文中所涉及程序采用MATLAB 6.5编写;数据文件由自编的程序转为文本文件后,在MATLAB 6.5中处理。解析后的光谱在NIST147和107标准MS库中进行检索,结合文献[8,9]数据进行定性。
2.4 采用AMWFA分辨数据
一般而言,GC-MS联用技术由于受到测量背景和峰重叠的影响,使测定的MS与标准MS库的匹配搜索非常困难;此外,峰的漂移使得在不同体系中(如在单味药和药对中)进行成分的鉴定和比较相当棘手。因此,在许多情况下,大量的数据被浪费了。幸运的是,化学计量学方法如HELP[10]、光谱相关色谱法(SCC)[11,12]等,已经成功地用于处理这些数据并解决像中药这样复杂的体系。AMWFA[4]对存在于不同复杂体系中的化学成分的比较研究非常有帮助,故本研究应用此方法并结合HELP进行分析。
3 结果与讨论
3.1 用AMWFA对单味药和药对进行定性和比较分析
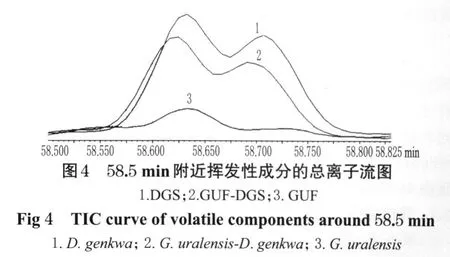
GUF、DGS和其药对中挥发性成分的总离子流图分别见图1~图3。

从图1~图3可以看出,中药中的挥发性成分是非常复杂的。除了几个较大的峰以外,还存在其他大量小峰。在这些峰之中,有超过100个相对含量>0.1%的峰。当对这些峰进行分析时,背景会受到严重影响,而大峰的延伸也会干扰小峰的鉴定分析。此外,尽管对分离条件进行了优化,还有部分峰重叠在一起。因此,如果没有对GC-MS数据进行进一步处理就进行定性和定量分析是很困难的,也是不准确的。在这部分工作中,应用AMWFA可对数据进行扣背景、消除大峰干扰和对重叠峰进行分辨。此外,还可用AMWFA对药对和组成它的单味药进行比较。

在此,笔者选择58.5 min附近的峰簇(见图4)为例来说明如何利用AMWFA进行重叠峰的分辨、比较和鉴定来自2个复杂体系的共有组分并获取其纯MS。图4显示,GUF-DGS和DGS的色谱图非常相似,而GUF的色谱信号相对于GUF-DGS和DGS较弱,其形状也有些不同。乍一看在这一时间段内仅存在2种成分,但结果证明这是不正确的。子空间比较法和奇异值法都显示在该时间段内GUF-DGS和DGS都含有3种成分。多组分光谱相关色谱(MSCC)和逆向组分光谱相关色谱(IP-MSCC)显示,GUF-DGS中的组分包含DGS中的组分,反之亦然。接着进行的是共有秩分析,结果发现在GUF-DGS和DGS中有3种共有组分,这与前述结果一致。
利用AMWFA进行进一步解析可以得到各组分的解析色谱图,见图5;抽取的纯MS图见图6。
图6的上方是共有秩图(common rank map),该图显示了所研究的峰簇在不同的时间点有多少共有组分;图6的中间是光谱自相关曲线(spectral auto-correlative curves),它表示相邻两点MS的相似度,在该曲线的单组分区可进行纯MS的提取;图6的下方是所提取的某组分的纯MS。用所提取的纯MS在NIST147和107标准MS库中进行检索,并结合一些文献,该成分被鉴定为十八碳烯酸甲酯。另外2个在GUF-DGS和DGS中的共有组分分别被鉴定为亚油酸甲酯和5,11,14,17-二十碳四烯酸甲酯。

同法对GUF-DGS和GUF中的共有组分进行分析,结果显示它们之间只有1个共有组分,即亚油酸甲酯。其他峰簇可同样使用AMWFA进行比较和分析。所有AMWFA解析结果与经典的HELP分析结果一致。而以本中心开发的中药相似度评价软件对重复的2个样品进行相似度分析,发现它们的相似度在0.95以上,说明试验结果是可靠的。
3.2 药对成分定量分析
单个成分的含量以面积归一化法进行测定,而对于重叠峰的含量以解析后的峰面积进行计算。通过分析,GUF-DGS、DGS和GUF中分别有68、41和34个成分得到定量,占各自挥发性成分的75%、84%和90%。因为在每一种挥发油溶液中都加入了等体积的正十四烷(内标),因此用单个成分的面积百分数与正十四烷(内标)的面积百分数之比来说明药对组合前后的含量变化更加合理。30 g GUF、DGS以及它们各30 g组成的药对的2次重复试验的平均结果见表1(表1中,RC为相对百分含量,RC=某成分百分含量/内标百分含量;RT为保留时间(min))。
3.3 GUF-DGS药对和单味药中挥发性成分的比较分析
从表1可以看出,大多数存在于单味药(GUF、DGS)中的挥发性成分均可以在它们组成的药对(GUF-DGS)中找到,只有极少数成分未能在药对中检测到(相对含量为0.02~2.02)。另外,还有一种成分(2-辛烯醛,相对含量为0.43)只能在药对中检测到,而在单味药中未能找到。这说明药对的挥发性成分几乎完全来源于各单味药,这2味中药单独煎煮和组合煎煮对挥发性成分的种类没有影响。

续表1Contiuned tab 1
但是,药对中挥发性成分的相对含量与单味药相比发生了较大的变化,只有5种成分是药对含量大约等于单味药含量之和。此外,GUF-DGS中2-庚酮(保留时间为7.350 min)的相对含量为0.65,大于该成分在GUF中的相对含量(0.13)与在DGS中的相对含量(0.09)之和。类似还有44个成分在药对中的含量大于单味药含量之和。GUF-DGS中亚油酸(保留时间为59.640 min)的相对含量为0.89,小于该成分在GUF中的相对含量(11.4)与在DGS中的相对含量(3.56)之和。类似还有18个成分的含量变化属于这种情况。这种含量变化最高可达10倍。而有趣的是,药对中成分含量减少的,其保留时间大多在50 min以后(沸点相对较高);而药对中成分含量增加的,其保留时间大多在50 min以前(沸点相对较低)。单味药和药对中的主要成分如棕榈酸、亚油酸甲酯、叶绿醇、亚油酸和硬脂酸的绝对减少量较大。这些变化也存在于其他药对和它们的单味药之中[13],研究者将这种变化的原因归于在煎煮过程中的酸碱反应:存在于单味药的生物碱和有机酸可以在煎煮过程中发生反应生成有机盐,而这种有机盐可以溶解于水中而失去挥发性[13]。此外,在高温和长时间的煎煮过程中,其他类型的反应也可能发生。事实上,这种变化的原因和意义还有待进一步研究。
[1] Fukai T,Marumo A,Kaitou K,et al.Anti-helicobacter pylori flavonoids from licorice extract[J].Life Sci,2002,71(12):1 449.
[2]Park BY,Min BS,Ahn KS,et al.Daphnane diterpene esters isolated from flower buds of Daphne genkwa induce apoptosis in human myelocytic HL-60 cells and suppress tumor growth in Lewis lung carcinoma(LLC)-inoculated mousemodel[J].JEthnopharmacol,2007,111(3):496.
[3] 王宇光,高 月.中药十八反药理毒理研究进展[J].中国实验方剂学杂志,2003,9(3):60.
[4] Zeng ZD,Liang YZ,Wang YL,et al.Alternative moving window factor analysis for comparison analysis between complex chromatographic data[J].JChromatogr A,2006,1 107(1-2):273.
[5] 易伦朝,曾仲大,梁逸曾,等.GC-MS与交互移动窗口因子分析法(AMWFA)用于3种陈皮挥发油成分的比较分析[J].高等学校化学学报,2006,27(9):1 626.
[6] 易伦朝,曾仲大,梁逸曾,等.交互移动窗口因子分析法(AMWFA)用于二维数据重叠色谱峰的比较分析[J].高等学校化学学报,2006,27(11):2 052.
[7] 国家药典委员会.中华人民共和国药典(一部)[S].2010年版.北京:中国医药科技出版社,2010:附录63.
[8] Zhao CX,Liang YZ,Fang HZ,et al.Temperature-programmed retention indices for gas chromatography-mass spectroscopy analysis of plant essential oils[J].J Chromatogr A,2005,1 096(1-2):76.
[9] 原思通,张保献,黄红生.气质联用法分析炮制对芫花挥发油的影响[J].中国中药杂志,1993,18(10):596.
[10] Kvalheim OM,Liang YZ.Heuristic evolving latent projections:resolving two-way multicomponent data.Ⅰ.Selectivity,latent-projective graph,datascope,local rank,unique resolution[J].Anal Chem,1992,64(8):936.
[11]Li BY,Hu Y,Liang YZ,et al.Spectral correlative chromatography and its application to analysis of chromatographic fingerprints of herbal medicines[J].J Sep Sci,2004,27(7-8):581.
[12]Li BY,Hu Y,Liang YZ,et al.Quality evaluation of fingerprints of herbal medicine with chromatographic data[J].Anal Chim Acta,2004,514(1):69.
[13] Li XR,Liang YZ,Guo FQ.Analysis of volatile oil in Rhizoma ligustici chuanxiong-Radix paeoniae rubra by gas chromatography-mass spectrometry and chemometric resolution[J].Acta Pharmacol Sin,2006,27(4):491.
Analysis of Volatile Components in Glycyrrhiza uralensis and Daphne genkwa and Their Drug-pair by Chemometric Methods
ZHOU Neng,ZHOU Zhen,ZENG Chu-jie
(College of Chemistry&Materials,Yulin Normal University,Guangxi Yulin 537000,China)
ZHOU Neng,LIANG Yi-zeng
(School of Chemistry and Chemical Engineering,Central South University,Changsha 410083,China)
OBJECTIVE:To analyze the volatile components in Glycyrrhiza uralensis and Daphne genkwa and their drug-pair.METHODS:With tetradecane as internal standard,the volatile components in G.uralensis and D.genkwa and their drug-pair were determined by GC/MS technique.Multiple chemometric methods were used to identify and analyze two dimension chromatograms/mass spectrum in order to obtain pure GC curves and pure MS of each component.The quality of components was identified through pure MS similarity retrieval.The attributions of components were analyzed by transform and subwindow factor analysis before and after compatibility,and quantitative study was conducted by peak area normalization method.RESULTS:34,41,68 components were qualitatively identified in G.uralensis and D.genkwa and their drug-pair,representing about 90%,84%,75%of volatile oil of them,respectively.Relative contents of volatile components in drug-pair were greatly different from those of single ingredient.CONCLUSION:Results of study can provide important basis for the research of TCM compatibility.
Glycyrrhiza uralensis;Daphne genkwa;Chemical components of volatile oil;Drug-pair;GC/MS;Transform and subwindow factor analysis
R284.1;R284.2
A
1001-0408(2012)43-4078-04
DOI 10.6039/j.issn.1001-0408.2012.43.18
Δ国家自然科学基金资助项目(81060360);广西自然科学基金面上项目(2010GXNSFA013065);2010年“广西高校优秀人才资助计划”项目
*教授,博士。研究方向:中药现代化。电话:0775-2818619。E-mail:2818619@163.com
#通讯作者:教授,博士研究生导师。研究方向:化学计量学和中药现代化。电话:0731-88830831。E-mail:yizeng_Liang@263.net
2011-11-05
2012-01-09)

