纳米NiAl2O4粉体的制备与表征
胡志强,黄德锋,刘显卿,高 丽,高 宏
(1大连工业大学,辽宁 大连116034;2大连交通大学,辽宁 大连116028)
纳米NiAl2O4粉体的制备与表征
胡志强1,2,黄德锋1,刘显卿1,高 丽1,高 宏2
(1大连工业大学,辽宁 大连116034;2大连交通大学,辽宁 大连116028)
NiAl2O4是一种混合阳离子化合物,具有尖晶石结构,其中Al占据八面体位置,Ni占据四面体位置。由于其具有高温稳定性和催化性,在介电、敏感、发光、超导等功能材料中得到应用[1]。此外,NiAl2O4还是一种窄禁带半导体,具有较好的可见光吸光性能、催化性、耐酸碱等优点[2]。Ramesh D.Peelamedu[3]采用微波烧结在数十分钟制备出晶型完好的NiAl2O4粉体。Nielson F.P.Ribeiro[4]等采用燃烧法制备NiAl2O4纳米粉体。Nogueira[5]等采用溶胶-凝胶法制备出颗粒细小、高比表面积的NiAl2O4粉体,与NiO形成NiO/NiAl2O4复合体系,可作为化学链燃烧的固体介质。E.Loginova[6]等研究了 NiAl2O4在(111)晶面具有较好的催化性能和防腐蚀性能;由于传统液相法或者固相法制备的粉体颗粒粒径尺寸大小及分布难以控制、团聚严重、单分散性差,将醇-水共沉淀法引入到液相合成过程中可以降低粉体的粒径[7,8]。醇水法主要是利用了醇较低的介电常数来降低生成的粉体在醇水混合溶液中的溶解度,使生成的粉体极易达到过饱和而成核生成细小的颗粒。在反应过程中由于醇基的存在,阻止了非架桥羟基与粒子表面氢键的形成,有效地避免了粉体的硬团聚,同时醇具有的空间位阻效应有利于生成颗粒小、分散性好的纳米颗粒[9]。本工作采用醇-水共沉淀法,以PEG6000作为分散剂制备NiAl2O4粉体,研究了醇-水比对粉体晶粒度的影响以及PEG6000分散作用机理,并探讨了NiAl2O4粉体在染料敏化太阳能电池光阳极中的应用。
1 实验
1.1 原料与试剂
AlCl3·6H2O(97%,分析纯),NiCl2·6H2O(98%,分析纯),氨水(NH4OH),乙醇(99.7%,分析纯),PEG6000(化学纯,平均分子量6000)。
1.2 粉体制备
将AlCl3·6H2O和NiCl2·6H2O按n(Al3+)∶n(Ni2+)=1∶2(摩尔比)混合并分别溶于不同醇-水体积比(0∶4,1∶3,1∶2,1∶1,2∶1,3∶1,4∶0)溶液中,在水浴40℃条件下不断搅拌加入氨水,调节pH值为8~9得到复合氢氧化物前躯体。将前躯体水洗、乙醇中回流1h、抽滤、干燥并研磨,于1200℃马弗炉中焙烧2h制得六组试样。通过一次粒径分析,确定试样制备的最佳醇-水比,在此条件下制备粉体A试样;以A试样同等制备条件下,在水洗后的前躯体中加入质量分数为2%的PEG6000,经回流、抽滤、干燥、1200℃下焙烧制得B试样。
1.3 粉体表征
采用 D/max-3B型X射线衍射(X-ray diffraction,XRD)仪确定粉体的晶相,并根据Scherrer公式[10]计算其平均晶粒尺寸;JEOL-JEM-1200EX 型透射电镜(Transmission Electron Microscope,TEM)观察表面形貌、粉体的粒度及团聚程度;物质的结构与成分变化通过Nicolet FTIR-5DX型红外光谱仪检测,分析聚乙二醇防团聚的作用机理。采用SS50ABA(AM1.5,100mW/cm2)型太阳能模拟器及 CHI600C型电化学工作站表征电池的光电性能。
2 结果与讨论
2.1 晶相结构分析
图1为A,B试样的XRD图谱。(331)晶面特征峰2θ均为37.14°,其他特征吸收峰均与NiAl2O4标准图谱衍射峰相吻合,且无AlCl3和NiCl2的杂相峰,表明A,B试样均为纯度较高的NiAl2O4尖晶石。该尖晶石相属于立方晶系,Fd-3m 空间群,a0=8.05nm,Z=8[7]。根据Scherrer公式计算A,B试样的平均晶粒尺寸。A试样在垂直于(331)晶面的平均晶粒尺寸为24.25nm,B试样平均晶粒尺寸为23.64nm。

图1 A,B试样的XRD图Fig.1 The X-ray diffraction spectra of sample A and B
2.2 不同醇-水比对晶粒度影响
利用X射线衍射峰半高宽化法,根据Scherrer公式得不同醇-水比体系制备试样的平均晶粒尺寸,结果如表1所示。

表1 不同醇-水比试样的粒径数据表Table 1 The particle size of different ratio of alcohol-aqueous samples
采用不同的醇水比制备粉体的一次粒径差别较大,随着醇加入的比例增大,粉体的一次粒径先减小后增大。当醇-水体积比为1∶1时,样品粒子的平均晶粒尺寸趋于最小,达到24.25nm。由于乙醇的介电常数比纯水小,根据热力学原理,在液相环境中,得到稳定的最小晶体粒径与过饱和比的关系可以用Kelvin[11]公式来表示,即:

式中:r是与过饱和比S相对应的临界颗粒半径;σs-1是新生的晶体与溶液间的固液表面自由能;M为结晶物质的分子量;R为气体常数;T为形成晶体时系统的绝对温度;ν为每分子溶质中离子的数目,对由分子构成的晶体ν=1;过饱和比S为溶液实际浓度与溶质溶解度的比值,S=C/C1。在溶液中,引入乙醇降低了醇水混合溶剂的介电常数,导致溶液的溶剂化能力下降,同时也降低了生成物的溶解度Cl,使得溶液的过饱和比S增大,从而降低了形核半径r,因此有利于生成小尺寸的纳米颗粒。但是,由于沉淀反应是在醇-水混合溶液中进行,当乙醇过多时,势必会减少粒子间的相互作用力。根据DLVO理论[12],颗粒间的相互作用势能可表示为:
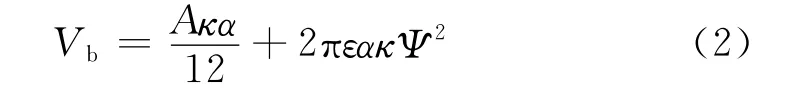
式中:A是 Hamker常数;κ是Debye-Huckel参数;α是颗粒直径;ε是溶液的介电常数;Ψ是表面势能。由于参数A,κ变化不大,所以Vb的大小主要由溶液的介电常数ε决定。溶剂中引入乙醇时,颗粒表面会吸附大量醇分子,明显降低了颗粒的表面张力和表面能,从而降低了颗粒间的团聚趋势。当加入的醇超过1∶1时,溶剂的介电常数ε逐渐减小,颗粒间的斥力势能也就逐渐降低,颗粒容易聚集生长成更大的颗粒。而仅在纯水溶液的体系中进行反应,若生成的沉淀粒子尺寸很小,比表面积较大,粒子之间就很容易形成团聚形成大颗粒。只有当醇-水比最佳时,既可形成细而多的晶核,又可使一定量的乙醇分子包覆在初生粒子周围,使得粒子之间的静电斥力适中,从而阻止生成粒子进一步团聚,因此确定制备A,B试样的最佳醇-水比为1∶1。
2.3 形貌分析
图2为NiAl2O4粉体A,B试样的TEM图。未加PEG6000的A试样出现了严重的硬团聚(图2(a)),粉体难以分散,颗粒之间相互连结,粉体颗粒较大。在粉体制备过程中,由于颗粒间的静电力以及表面能作用增大了粒子间的聚合;又因颗粒间的非架桥羟基和吸附水的存在,使得外来粒子就可以吸附在其空白位置上形成搭桥效应,引起颗粒团聚,导致颗粒度增大。在粉体合成过程中,由于纳米粉体表面效应的作用,粉体表面聚集了大量的电荷或官能团,增大了粉体表面能,为了降低纳米粉体表面能而出现团聚使其倾向于变小。表面活性剂亲水基团对固体的吸附性和化学反应活性及降低表面张力的特性可以控制纳米微粒的亲水性、亲油性或表面活性,同时能对纳米微粒表面进行改性。其作用机理为[13]:(1)表面活性剂亲水基团与粉体表面基团结合赋予纳米粒子表面新的活性;(2)降低纳米粒子表面能使纳米粒子达到稳定状态;(3)表面活性剂的长链端在纳米粒子表面形成空间位阻,防止纳米粒子的再团聚,从而改善纳米粉体在不同介质中的分散性、表面活性以及表面结构等。

图2 A试样(a)和B试样(b)的TEM图Fig.2 The TEM images of sample A (a)and sample B(b)
加入PEG6000的B试样(图2(b))分散效果得到明显的改善,粒度分布均匀,平均粒径较小(约30nm),与A试样相比,粉体的分散性得到明显的改善,颗粒分散均匀,说明PEG6000的加入起到良好的分散作用,并且在一定程度上抑制了粒子的长大。聚乙二醇属非离子表面活性剂[14],它只有醚键与羟基两种亲水基而无疏水基,其分子链在水溶液中呈蛇形,在制备过程中引入PEG6000,通过氢键吸附在粒子表面,主要由前驱体表面羟基与大量PEG6000醚键相互作用形成氢键包覆于粒子表面,使PEG6000分子链的一端紧密地吸附于粉体颗粒表面,在颗粒表面形成一层有机亲水保护膜,颗粒表面活性剂亲水基团与粒子相互作用,改变了粒子表面性质,对生成的粒子起稳定和保护作用,防止粒子进一步生长。根据相似相溶原理PEG6000的另一端则尽可能伸入溶液中,形成的大分子亲水保护膜,增大了颗粒之间静电斥力位能。同时由于长链PEG6000表面活性剂的空间位阻效应,有机链引起颗粒间排斥力,从而使固相粒子之间的距离增大,在一定程度上避免了晶核或晶粒由于氢键、化学键和分子作用力等的作用促使粒子的聚合长大,抑制了粒子团聚的产生[15],最终使体系达到稳定分散,阻止前驱体颗粒的团聚,使得前躯体颗粒在宏观性质上表现为松散。在焙烧的过程中,由于颗粒外表面形成的包覆膜,随着PEG6000分解脱除,PEG6000长链与颗粒表面脱离,颗粒成为独立的微细个体,进而达到分散的作用。
2.4 红外光谱分析
图3为NiAl2O4前驱体热处理前后的红外吸收光谱图。-OH基伸缩振动一般出现在3700~3100cm-1,弯曲振动出现在1600~1300cm-1。由图3中a,b曲线可以得出,在合成过程中加入了PEG6000所制得的前驱体B的-OH基伸缩振动峰比未加入PEG6000所制得的前驱体红移了30cm-1(3465.78~3435.00cm-1),弯曲振动峰红移了4cm-1(1631.03~1627.97cm-1),且变平、变宽、强度减弱。说明在前驱体表面发生了PEG吸附,从而减弱了-OH基与粒子表面的键合作用,桥-OH基及非桥-OH基也有所减少,导致振动吸收带移向低频,进而削弱了粒子间的团聚作用[16]。
图3中b,c曲线为在合成过程中加入了PEG6000所制得的前驱体B热处理前后的红外吸收图谱,经热处理后图中c曲线与未经热处理的b曲线相比,-OH基伸缩振动峰和弯曲振动峰都已消失,说明热处理后颗粒表面完全脱除了-OH基等的包覆,PEG6000分解完成,瓦解了颗粒间大分子基团的键合,粉体得到均匀分散。据研究前驱体上的表面吸附水、配位水在150℃开始脱除,作用较强的非桥-OH基、桥-OH基等在300~450℃都已陆续分解脱除[17]。说明PEG大分子不仅在沉淀过程中减弱了团聚作用,而且前躯体干燥、焙烧过程中各种形式的H2O,-OH基的脱除是在PEG大分子“掩盖”下或与PEG大分子的分解脱除同步进行,减少了-OH(尤其是非桥-OH)、H2O脱除引起的团聚作用,从而减弱前躯体热处理后的硬团聚。

图3 试样前驱体FT-IR光谱图Fig.3 FT-IR spectra of precursor for samples
2.5 NiAl2O4粉体的应用
NiAl2O4纳米粉体在可见光范围具有较好的吸收效果,且为窄禁带尖晶石类化合物[2],使其作为染料敏化太阳能电池光阳极复合材料成为可能。课题组[18]将NiAl2O4粉体应用到染料敏化太阳能电池光阳极中,与TiO2纳米晶制备NiAl2O4/TiO2复合薄膜电极,电池的光电转换效率得到提高,与未掺入NiAl2O4粉体的纯TiO2电极相比,光电转换效率提高了17.4%。
3 结论
(1)将适量乙醇引入水溶剂中,降低了溶液的溶剂化能力,改变NiAl2O4粒子的成核半径r,有利于生成较小尺寸的纳米颗粒。结果表明最佳醇-水比为1∶1,此时粉体一次粒径为24.25nm。
(2)在醇-水共沉淀过程中加入PEG6000时,改变了前躯体粒子的表面活性、粒子表面能及其空间位阻效应,进而阻止前驱体颗粒的团聚;在热处理过程中随着PEG6000分解脱除,包覆在粒子表面的-OH也全部脱附,瓦解了颗粒间大分子基团的键合,从而对NiAl2O4粉体取到均匀分散的作用。
(3)在染料敏化太阳能电池应用中,NiAl2O4粉体掺合制备的TiO2复合薄膜电极与未掺合的薄膜电极相比,光电转换效率提高了17.4%。
[1]SHU J,KALIAGUINE S.Well-dispersed perovskite-type oxidation catalysts[J].Applied Catalysis B:Environmental,1998,16(3):303-308.
[2]韦秀华,姚山山,陈栋华,等.尖晶石型 MAl2O4(M=Ni、Mg)纳米粉体的溶胶凝胶法制备及表征[J].中南民族大学学报,2006,25(1):8-11.
[3]RAMESH D PEELAMEDU,RUSTUM ROY,DINESH K AGRAWAL.Microwave-induced reaction sintering of NiAl2O4[J].Materials Letters,2002,55(4):234-240.
[4]NIELSON F P RIBEIRO,RAIMUNDO C R NETO,SILVIA F MOYA.Synthesis of NiAl2O4with high surface area as precursor of Ni nanoparticles for hydrogen production[J].International Journal of Hydrogen Energy,2010,35(21):11725-11732.
[5]NUBIA ALVES SOUZA NOGUEIRA,ERANDIR BRASIL DA SILVA.Synthesis and characterization of NiAl2O4nanoparticles obtained through gelatin[J].Materials Letters,2007,61(25):4743-4746.
[6]LOGINOVA E ,COSANDEY F,MADEY T E.Nanoscopic nickel aluminate spinel(NiAl2O4)formation during NiAl(111)oxidation[J].Surface Science Letters,2007,601(3):L11-L14.
[7]李蔚,王浚,高濂.分散剂在醇-水溶液加热法制备球形ZrO2粉体过程中的作用[J].硅酸盐学报,2000,28(6):582-584.
[8]李蔚,高濂,郭景坤.醇水溶液加热法制备纳米ZrO2粉体及相关过程研究[J].无机材料学报,2000,15(1):16-20.
[9]李霞章,陈志刚,陈建清,等.醇水法制备纳米粉体原理及应用[J].硅酸盐通报,2006,25(2):82-86.
[10]AYANA TOMITA,TOKUSHI SATO.Luminescence channels of manganese-doped spinel[J].J Lumin,2004,109(1):19-24.
[11]吴树森.应用物理化学(第一分册)——界面化学与胶体化学[M].北京:高等教育出版社,1983.36-42.
[12]高濂,李蔚.纳米陶瓷[M].北京:化学工业出版社,2002.19-22.
[13]阳鹏飞,颜雪明,刘传湘.表面活性剂在合成纳米钛酸钡粉体中的应用[J].南华大学学报,2006,20(1):104-107.
[14]卫芝贤,欧海峰,宫喜军,等.表面活性剂PEG在掺锑纳米SnO2粉末氧化共沉淀制备中的作用[J].过程工程学报,2005,5(3):305-308.
[15]董赛男,商少明,王璟.表面活性剂对超细钛酸钡粉体制备的影响[J].世界科技研究与发展,2008,30(5):538-541.
[16]张海军,贾晓林,刘战杰,等.纳米Al2O3-SiO2的分散及颗粒间的相互作用[J].硅酸盐学报,2003,31(10):928-933.
[17]徐明霞,方洞浦,郭瑞松.PEG在ZrO2前躯体表面的吸附及改性作用[J].天津大学学报,1994,27(2):172-178.
[18]高丽,胡志强,曹梦菲,等.NiAl2O4掺杂TiO2薄膜电极的制备及其性能研究[J].大连工业大学学报,2010,29(5):349-353.
Synthesis and Characterization of NiAl2O4Nano-powders
HU Zhi-qiang1,2,HUANG De-feng1,LIU Xian-qing1,GAO Li1,GAO Hong2
(1Dalian Polytechnic University,Dalian 116034,Liaoning,China;2Dalian Jiaotong University,Dalian 116028,Liaoning,China)
采用醇-水共沉淀法制备NiAl2O4纳米粉体,PEG6000作分散剂。通过XRD,TEM及FT-IR等测试手段,研究醇-水比对粉体晶粒度的影响以及PEG6000对NiAl2O4粉体分散性能的影响。结果表明:醇-水的最佳比例为1∶1,此时粉体的晶粒尺寸趋于最小。在沉淀过程中加入PEG6000,可避免前躯体粒子的团聚及粉体在焙烧过程中形成的团聚,改善了粉体的分散性。将制备的NiAl2O4纳米粉体掺合到染料敏化太阳能电池TiO2光阳极中,电池的光电转换效率得到明显的改善。
NiAl2O4;纳米粉体;尖晶石;醇-水共沉淀法
NiAl2O4nano-powders were synthesised by coprecipitation process of alcohol-aqueous,PEG6000served as dispersant.The effects of the ratio of alchohol-aqueous on the grain size of powders and the PEG6000on dispersion characteritics of NiAl2O4nano-powders were investigated by XRD,TEM analysis,and FT-IR spectrum.The results indicate that the optimal ratio of alcohol-aqueous is 1∶1,in this case the grain size of the powders tend to minimum.By adding the PEG6000in the deposition process,the reunion of precursor particles and the powder in roasting process can be avoided obviously.And then,the dispersion of the powder was improved significantly.Therefore,after adopting the NiAl2O4nano-powders to the TiO2film of dye-sensitized solar cells,the photoelectric conversion efficiency of the battery increases efficiently.
NiAl2O4;nano-powder;spinel;coprecipitation process of alcohol-aqueous
TB34
A
1001-4381(2012)08-0051-04
国家863高技术研究发展计划资助项目(2006AA05Z417);大连市科技平台建设项目资助(2010-354)
2011-08-03;
2012-01-09
胡志强(1956-),男,教授,主要从事功能材料研究,联系地址:大连工业大学新能源材料研究所(116034),E-mail:hzq@dlpu.edu.cn

