槲皮素衍生物的合成及生物活性研究进展
渠文涛,朱 玮,翟广玉,颜子童
(郑州大学 药学院,河南 郑州450052)
槲皮素衍生物的合成及生物活性研究进展
渠文涛,朱 玮,翟广玉*,颜子童
(郑州大学 药学院,河南 郑州450052)
综述了槲皮素衍生物的合成及生物活性研究进展,介绍了国内外槲皮素氨基酸类、糖苷类、酯类、醚类衍生物及金属配合物的合成方法及其生物活性研究现状.指出槲皮素是一种从天然植物中提取的黄酮醇类化合物,具有抗氧化,抗菌,扩张血管,抗肿瘤及抗突变等多种生物学活性.然而,槲皮素具有水溶性差、生物利用度较低等缺点,临床应用受到限制.为此,国内外学者对其结构进行修饰改造,开发出了一系列具有新颖结构的槲皮素先导化合物,可望为新型槲皮素衍生物的设计合成提供参考.
槲皮素;槲皮素衍生物;合成;生物活性;研究进展
槲皮素(quercetin,3,3′,4′,5,7-五羟基黄酮,结构见图1)是具有多种生物学活性的黄酮类化合物,广泛存在于蔬菜、水果及中草药中,如洋葱、苹果、葡萄、银杏、茶叶等.研究表明槲皮素具有抗氧化、抗炎、抗菌、抗肿瘤及抗突变等多种生物学活性[1-4].然而,由于槲皮素为平面型分子,分子堆砌较紧密,分子间引力较大,不易被溶剂或溶质分散,所以槲皮素的水溶性较差,生物利用度较低(血浆浓度峰值仅为0.13~7.6 μmol·L-1),而使槲皮素的临床应用受到极大的限制[5].为此,国内外学者对其结构进行修饰、改造,合成出了大量水溶性增强,生物利用度改善的槲皮素衍生物,以期开发出活性更高、更具有临床应用价值的药物.作者就槲皮素衍生物的合成及其生物活性的研究状况作一综述,以促进其研究应用.

图1 槲皮素及其衍生物的化学结构Fig.1 Chemical structure of quercetin and its derivatives
1 槲皮素氨基酸类衍生物
GOLDING等[6]合成了一种水溶性的槲皮素前药,3′-O-N-羧甲基甲酰胺基槲皮素(QC12,图2).MULHOLLAND等[7]对QC12进行非正式的Ⅰ期临床研究发现,QC12和槲皮素一样口服无效,但注射QC12后其血浆浓度峰值可达到108.7±41.67μmol·L-1.QC12可以抑制人卵巢癌A2780细胞的生长,并将细胞增殖阻滞在S后期与G2早期.

图2 QC12的合成Fig.2 Synthesis of QC12
伍贤学等[8]利用光气对氨基酸甲酯进行异腈酸酯化,合成了一系列槲皮素氨基甲酸酯(图3a).叶斌等[9]用槲皮素苯基异氰酸酯(PHICNQ)进行抗肿瘤试验(图3b).结果发现:槲皮素和PHICNQ对人慢性骨髓白血病细胞K562和小鼠结肠癌细胞CT26均有抑制作用,且呈时间、剂量依赖性.PHICNQ对K562细胞和CT26细胞的增殖抑制作用分别是槲皮素的73倍和308倍.
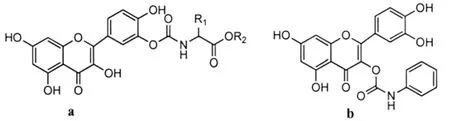
图3 槲皮素氨基甲酸酯及槲皮素异腈酸酯的结构Fig.3 Structures of amino acid carbamates of quercetin and phenylisocyanate of quercetin
BIASUTTO等[10]直接将槲皮素与叔丁氧羰基(Boc)保护的非α-氨基酸反应,通过酯化,氯化氢脱Boc得到了一系列槲皮素-3′-氨基酸酯盐酸盐,结果显示,这些衍生物的生物利用度较槲皮素明显提高(总产率20%,图4).
HUANG等[11]从芦丁出发,经过三步合成了15种槲皮素-3-O-氨基酸酯.生物活性评价显示,与槲皮素不同,槲皮素-3-O-氨基酸酯可以高选择性地抑制Src酪氨酸激酶,IC50在3.2~9.9μmol·L-1之间(图5).
MI等[12]从特布他林前药班布特罗受到启发,在槲皮素3位引入N,N-二甲基氨基甲酰基,合成了3-N,N-二甲基氨基甲酰基槲皮素(DCQ,图6).实验显示,DCQ的水溶性较槲皮素增强了14倍;稳定性实验也表明该化合物不易发生非酶水解,在PBS缓冲液中的半衰期比QC12(t1/2=16.9)还长1h,是一种新型的槲皮素的前药.
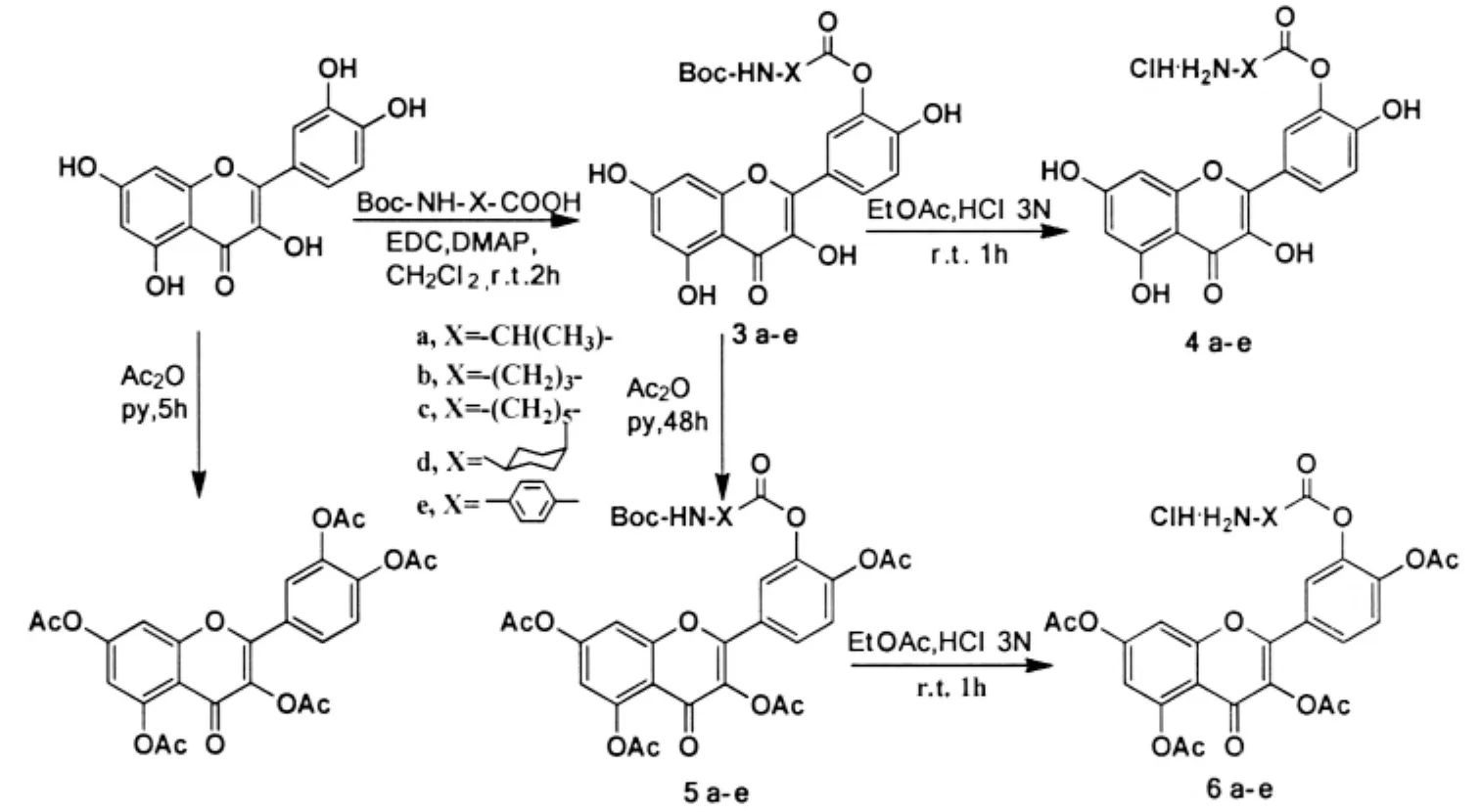
图4 槲皮素-3′-氨基酸酯盐酸盐的合成Fig.4 Synthesis of quercetin-3′-amino acid ester hydrochloride

图5 槲皮素-3-O-氨基酸酯的合成Fig.5 Synthesis of quercetin-3-O-amino acid esters

图6 DCQ的合成Fig.6 Synthesis of DCQ
2 槲皮素酯类衍生物
佘戟等[13]通过对槲皮素硫酸酯化,合成出槲皮素-7-硫酸酯钠(Ⅰ)和槲皮素-7,4′-二硫酸酯二钠(Ⅱ)两种水溶性化合物(图7).体外活性实验表明:这两种新化合物虽解决了槲皮素水溶性的问题,但都在一定程度上降低了槲皮素对HL-60细胞的抑制作用.提示封闭4′-OH和7-OH会降低槲皮素的活性.翁云[14]的研究也证实了这一点.

图7 槲皮素硫酸盐的合成Fig.7 Synthesis of quercetin sulphates
彭游等[15-16]合成了槲皮素磺酸酯类衍生物并申请了专利,其首先在有机溶剂中选择性保护槲皮素的羟基,然后与芳磺酰氯反应后,再经过脱保护得到目标产物.该法提高了槲皮素衍生物的生理活性,并改善了它们的溶解性(图8).
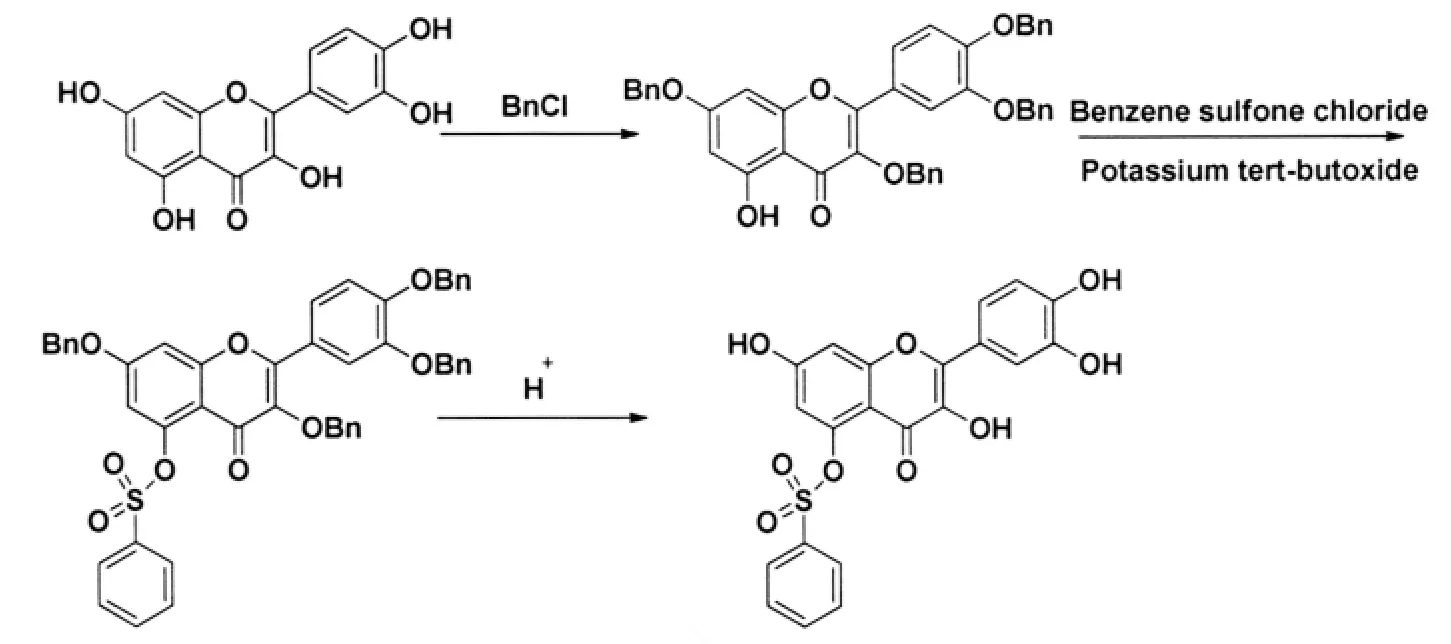
图8 槲皮素磺酸酯的合成Fig.8 Synthesis of quercetin sulfonic acid esters
MADHUKAR等[17]以芦丁为原料,用硫酸二甲酯保护羟基,然后水解,再与联苯乙酰氯反应得到槲皮素-3-联苯乙酰酯(BPA-QTME,图9).结果发现:BPA-QTME作为一种安全的非甾体抗炎药,具有化学稳定性和生物活性,既保留了抗炎活性,又降低了溃疡发生几率.
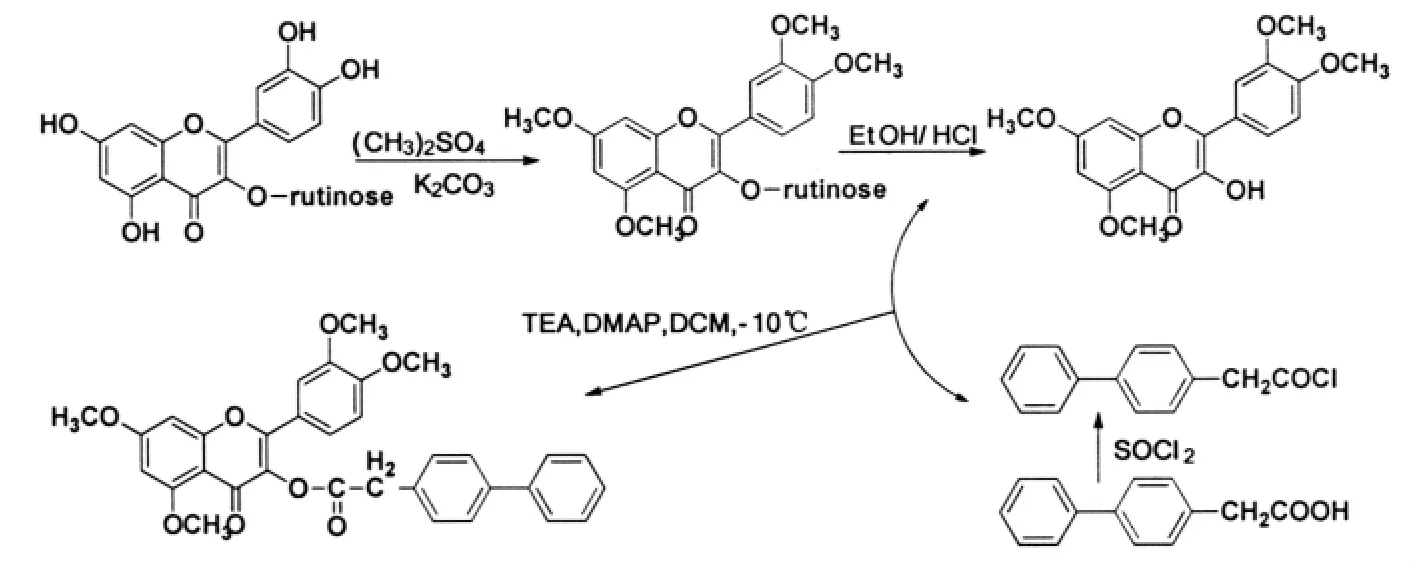
图9 槲皮素-3-联苯乙酰酯的合成Fig.9 Synthesis of quercetin-3-biphenyl acetyl ester
3 槲皮素糖苷类衍生物
槲皮素-3-O-(2-没食子酰基)-L-阿拉伯吡喃糖苷是从天然植物中分离出来的一种槲皮素糖苷.研究显示,槲皮素-3-O-(2-没食子酰基)-L-阿拉伯吡喃糖苷不仅有明显的抗菌活性[18],还可以抑制 HIV-1病毒的复制(IC50=18.1μg/mL)[19].LI MING等[20]选择性保护槲皮素羟基,经七步合成得到该化合物(图10).

图10 槲皮素-3-O-(2-没食子酰基)-L-阿拉伯吡喃糖苷的合成Fig.10 Synthesis of quercetin 3-O-(2″-galloyl)-α-L-arabinopyranoside
槲皮素-3-O-β-D-葡糖苷酸是槲皮素在人体的主要代谢产物之一,MOHAMMED等[21]以芦丁为原料,合成了槲皮素-3-O-β-D-葡糖苷酸(产率28%,图11),为槲皮素代谢产物的研究提供了方便.FAN等[22]利用大鼠进行体内实验发现,槲皮素-3-O-β-D-葡糖苷酸不仅具有抗病毒和抗感染活性,还可以明显地抑制二甲基苯诱导产生的大鼠耳朵水肿.
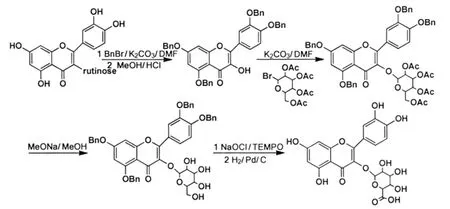
图11 槲皮素-3-O-β-D-葡糖苷酸的合成Fig.11 Synthesis of quercetin 3-O-β-D-glucuronide
ABUGAFAR等[23]报道从槲皮素出发,合成了一系列槲皮素酰基糖苷类似物.结果发现,这些化合物对多种革兰阳性菌有抗菌活性,且同时抑制细菌的DNA解旋酶和拓扑异构酶IV.其中化合物5i的抗菌活性是万古霉素的两倍,或将成为一个很有潜力的抗菌药物(图12).
此外,LEGAULT等[24]的研究也发现,槲皮素-7-O-β-D-葡糖苷除了有抗氧化活性之外,还可以通过抑制NO的释放,COX-2的表达等方式发挥抗炎作用.
4 槲皮素醚类衍生物
李化军等[25]从芦丁出发,经苄基保护、酸水解得到3′,4′,7-O-三苄基槲皮素.再与CH3I反应后经催化氢化脱苄基,选择性地得到3-O-甲基槲皮素.不仅简化了其合成方法,提高了收率,而且使用了更廉价易得的原料芦丁,降低了成本(总收率76.3%,图13).

图12 槲皮素酰基糖苷的合成Fig.12 Synthesis of acyl glycosides of quercetin
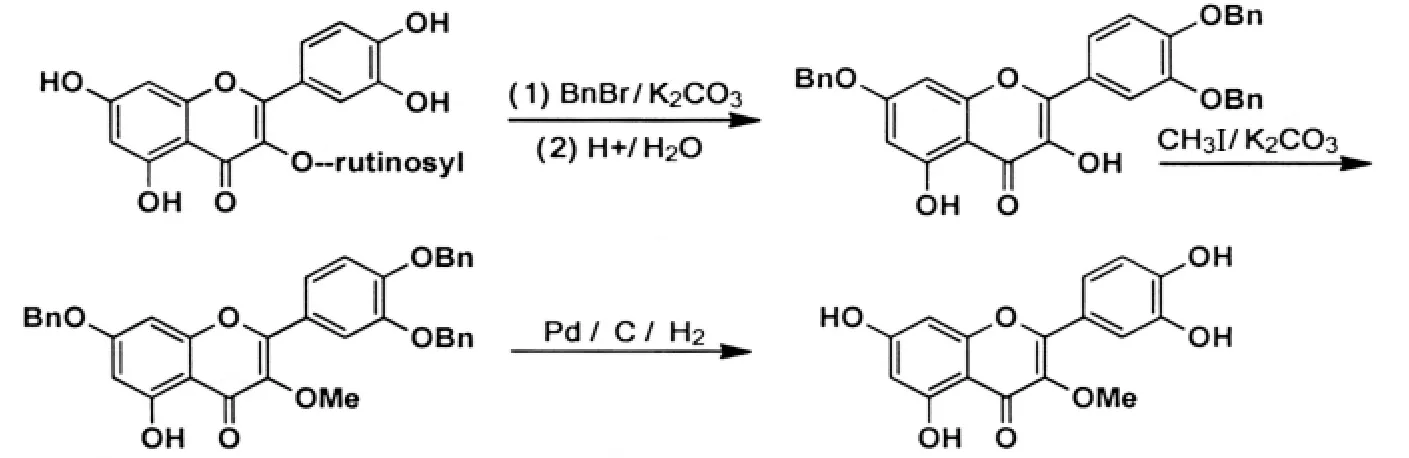
图13 3-O-甲基槲皮素的合成Fig.13 Synthesis of 3-O-methyl quercetin
LI等[26]以槲皮素为原料,先用二氯二苯基甲烷保护B环的儿茶酚羟基,再用氯甲基甲醚(MOMCl)保护3-OH和7-OH,经五步选择性地合成了4′-O-甲基槲皮素(总收率63%,图14).
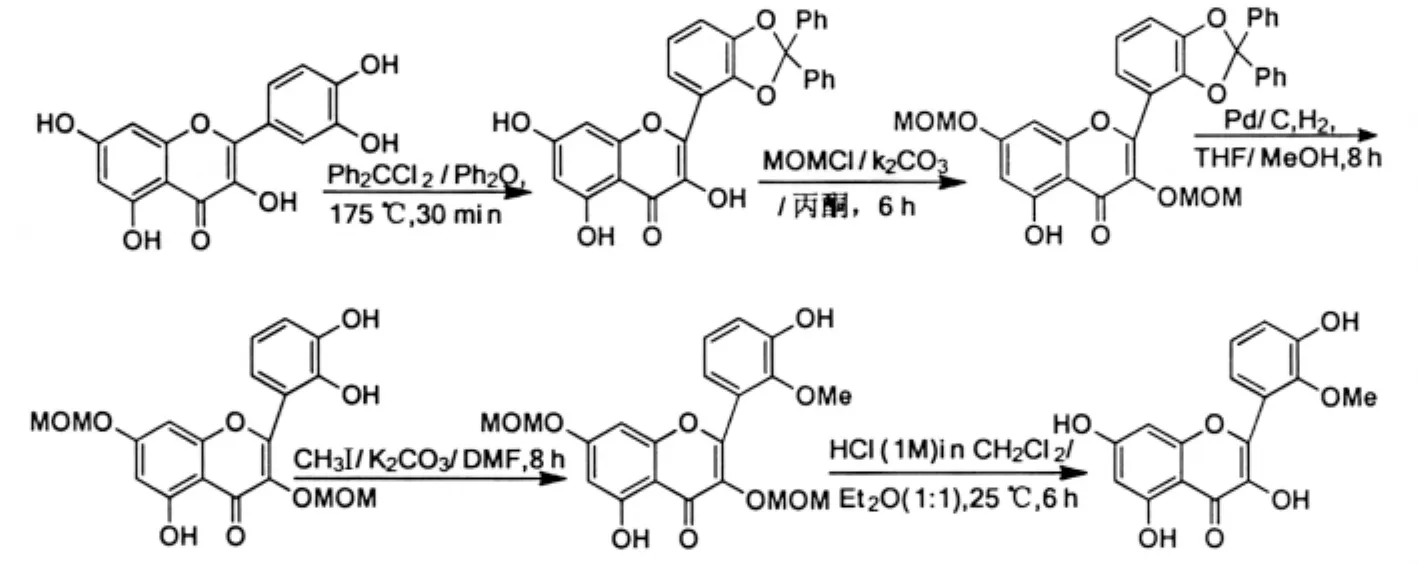
图14 4′-O-甲基槲皮素的合成Fig.14 Synthesis of 4′-O-methyl quercetin
TORRE等[27]合成了一系列黄酮的富勒烯衍生物,其中包括三个槲皮素的C60衍生物14(a-c).由于富勒烯和槲皮素均是优秀的自由基俘获剂,所以它们有望成为有药用价值的自由基俘获剂(图15).
槲皮素的3-位和7-位是化学和代谢敏感的基团,为了增加槲皮素的稳定性,KIM等[28]用聚甲醛(POM)与槲皮素反应,合成了两个新的槲皮素共轭化合物(7-O-POM-Q 和3-O-POM-Q,图16).结果显示,不仅这两个共轭化合物在细胞培养基中的稳定性明显提高,而且7-O-POM-Q的细胞膜通透性也明显增加.

图15 槲皮素富勒烯衍生物的合成Fig.15 Synthesis of fullerene derivatives of quercetin
5 槲皮素金属配合物
RUCHI等[29]合成了槲皮素钒配合物[VO(L)2](HL=槲皮素,图17).研究发现,槲皮素钒在链脲佐菌素诱导糖尿病小鼠的实验中,显示出胰岛素增加的趋势.通过测定腺嘧啶脱氧核苷的吸收作用显示,对Ⅱ型糖尿病的实验可作为胰岛素的提升剂.
谭君等[30-33]合成了槲皮素锌、铜、镍和锰等配合物(图18),应用紫外-可见光谱、荧光光谱分析、黏度测定、琼脂糖胶电泳和硫巴比妥酸反应测定法,发现槲皮素锌和槲皮素镍能够嵌插入DNA的碱基对中,使细胞核皱缩,引起细胞凋亡.槲皮素锌和槲皮素镍在体外对三种癌细胞(HePG2、SMMC7721和A549)均有显著的细胞毒素抑制作用,槲皮素铜能促进A549cells(人肺腺癌细胞)的凋亡.
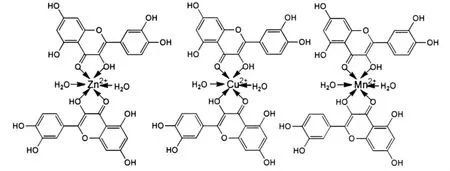
图18 槲皮素锌、铜、锰的结构Fig.18 Chemical structures of quercetin zinc,copper,manganese
谢伟玲等[34]合成了槲皮素锗配合物(图19),采用紫外、红外、核磁共振谱、元素分析、高效液相色谱、电化学方法对配合物的结构进行表征,同时探讨槲皮素及其配合物的抗氧化活性和可能的作用机制.实验结果表明,两种配合物均比槲皮素具有更强的清除自由基活性.因此,研究槲皮素及其配合物及其生物活性,对开发具有保健功能的新型锗化合物具有重要意义.

图19 槲皮素锗的结构Fig.19 Chemical structure of quercetin germanium
陈小平[35]将槲皮素与铂类抗肿瘤药物制成络合物,这种槲皮素二氨合铂既具有协同抗肿瘤作用、又可以降低铂类抗肿瘤药物的毒副作用、避免抗药性(图20).翟广玉等[36]使用槲皮素与铂盐在碱溶液中合成了槲皮素铂配合物.通过MTT法实验得出结论:槲皮素铂配合物对肝癌HepG2、宫颈癌Hela和喉癌Hep2等肿瘤细胞增殖具有明显的抑制作用.
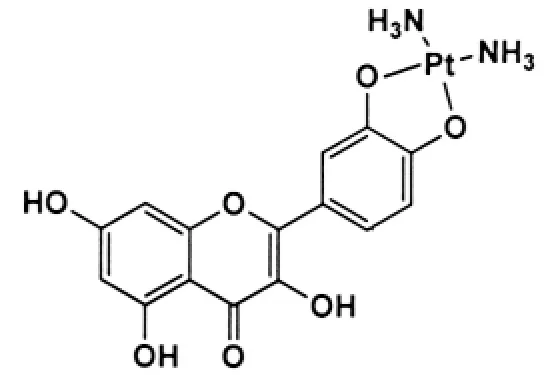
图20 槲皮素二氨合铂的结构Fig.20 Chemical structure of quercetin-platinum complex
结语:近年来,国内外对槲皮素及其衍生物的研究报道日益增多,且已经获得了一些活性较好的化合物.槲皮素前药QC12已经完成了Ⅰ期临床研究,这对研究者是很大的鼓舞,相信未来会有更多的槲皮素前药进入临床研究.尽管槲皮素有抗氧化,抗肿瘤,抗菌,扩张血管等多种生物学活性,但是由于其水溶性差,生物利用度低等缘故,大大限制了其临床应用.未来对槲皮素的修饰、改造,在考虑增加其水溶性的同时,要尽量提高其稳定性,使其在到达作用靶点之前尽可能不被代谢,从而更好地发挥治疗作用.
[1]PIETTA P G.Flavonoids as antioxidants[J].J Nat Prod,2000,63(7):1035-1042.
[2]CHOI J A,KIM J Y,LEE J Y.et al.Induction of cell cycle arrest and apoptosis in human breast cancer cells by quercetin[J].Int J Oncol,2001,19(4):837-844.
[3]YOSHIZUMI M,TSUCHIYA K,KIRIMA K,et al.Quercetin inhibits Shcand-phosphati dylinositol 3-kinase-mediated c-Jun N-terminal kinase activation by angiotensin II in cultured rat aortic smooth muscle cells[J].Mol Pharmacol,2001,60(4):656-665.
[4]SCHROETER H,SPENCER J P E,RICE E C,et al.Flavonoids protect neurons from oxidized low-density-lipoproteininduced apoptosis involving c-Jun N-terminal kinase(JNK),c-Jun and caspase-3[J].Biochem J,2001,358:547-557.
[5]MANACH C,WILIAMSONi G,MORAND C,et al.Bioavailability and bio-efficacy of polyphenols in humans.I.Review of 97bioavailability studies[J].Am J Clin Nutrit,2005,81:230-242.
[6]GOLDING B T,GRIFFIN R J,QUARTERMAN C P,et al.Analgues or derivaties of quercetin(prodrugs)[P].PCT/GB97/01727,1997-06-27.
[7]MULHOLLAND P,FERRY D,ANDERSON D,et al.Preclinical and clinical study of QC12,a water-soluble,pro-drug of quercetin[J].Annal Oncology,2001,12:245-248.
[8]WU Xian,CHENG Li,XIANG Dong,et al.Syntheses of carbamate derivatives of quercetin byreaction with amino acid ester isocyanates[J].Lett Org Chem,2005,2:535-538.
[9]YE B,YANG J L,CHEN L J,et al.Induction of apoptosis by phenylisocyanate derivative of quercetin:involvement of heat shock protein[J].Anti-Cancer Drugs,2007,18(10):1165-1171.
[10]BIASUTTO L,MAROTTA E,DE MARCHI U,et al.Ester-based precursors to increase the bioavailability of quercetin[J].J Med Chem,2007,50(2):241-253.
[11]HUANG He,JIA Qi,MA Jin Gui,et al.Discovering novel quercetin-3-O-amino acid esters as a new class of Src tyrosine kinase inhibitors[J].Eur J Med Chem,2009,44:1982-1988.
[12]MI K K,YOU M O,KWANG S P,et al.A novel prodrug of quercetin,3-N,N-dimethyl carbamoyl quercetin(DCQ),with improved stability against hydrolysis in cell culture medium[J].Bull Korean Chem Soc,2009,30(9):2114-2116.
[13]JI S,MO L E,KANG T B,et al.Preparation of water soluble quercetin derivatives and their biological activities[J].Chin J Med Chem,1998,8(4):287-289.
[14]翁 云,佘 戟,蔡康荣,等.槲皮素及其水溶性衍生物对HL-60细胞生长影响的比较[J].中国药理学通报,2000,16(2):154-157.
[15]YOU Peng.Synthesis method of a kind of flavonoid alcohol sulfonate derivatives.中国,200810060140.2[P].2008-03-07.
[16]YOU Peng,ZE Yuan Deng,WANG Chun Feng.Preparation and prodrug studies of quercetin pentabenzensulfonate[J].Pharm Soc Japn,2008,128(12):1845-1849.
[17]MADHUKAR M,SAWRAJ S,SHARAM,P D.Design,synthesis and evaluation of mutual prodrug of 4-biphenylacetic acid and quercetin tetramethyl ether(BPA-QTME)as gastrosparing NSAID[J].Eur J Med Chem,2010,45:2591-2596.
[18]IWAGAWA T,KAWASAKI J I,HASE T,et al.An acylated flavonol glycoside from lasiobema japonica[J].Phytochemistry.1990,29(3):1013-1014.
[19]KIM H J,WOO E R,SHIN C G,et al.A new flavonol glycoside gallate ester from acer okamotanum and its inhibitory activity against human immunodeficiency virus-1(HIV-1)integrase[J].J Nat Prod,1998,61:145-148.
[20]LI Ming,HAN Xiu Wen,Yu Biao.Synthesis of quercetin 3-O-(2″-galloyl)-α-L-arabino-pyranoside [J].Tetrahedron Lett,2002,43:9467-9470.
[21]MOHAMMED K,RAJAE Z,CHRISTIAN R.An expeditious synthesis of quercetin-3-O-β-D-glucuronide from rutin[J].Tetrahedron Lett,2011,52(37):4738-4740.
[22]FAN Dong Sheng,ZHOU Xin,ZHAO Chao,et al.Anti-inflammatory,antiviral and quantitative study of quercetin-3-O-β-D-glucuronide in polygonum perfoliatum L[J].Fitote-rapia,2011,82(6):805-810.
[23]ABUGAFAR M L H,YOSHITO Z,RAFIYAa K K,et al.Quercetin diacylgly-coside analogues showing sual inhibition of DNA gyrase and topoisomerase IV as novel antibacterial agents[J].J Med Chem,2011,54(11):3686-3703.
[24]LEGAULT J,PERRON T,MSHVILDADZE V,et al.Antioxidant and anti-inflammatory activities of quercetin 7-O-β-D-glucopyranoside from the leaves of brasenia schreberi[J].J Med Food,2011,14(10):1127-1134.
[25]李化军,栾新慧,赵毅民.3-O-甲基槲皮素的合成[J].有机化学,2004,24(2):1619-1621.
[26]LI Nian Guang,SHI Zhi Hao,TANG Yu Ping,et al.An efficient partial synthesis of 4′-O-methyl quercetin viaregioselective protection and alkylation of quercetin[J].Beilstein J Org Chem,2009,5:60.
[27]TORRE M D L,TOME A C,SILVA A M S,et al.Synthesis of[60]Fullerene-quercetin dyads[J].Tetrahedron Lett,2002,43:4617-4620.
[28]KIM M K,PARK K S,LEE C,et al.Enhanced stability and intracellular accumulation of quercetin by protection of the chemically or metabolically susceptible hydroxyl groups with a pivaloxymethyl(POM)promoiety[J].J Med Chem,2010,53(24):8597-8607.
[29]RUCHI S,VIVEK B,SUBHASH P,et al.Synthesis,structural properties and insulin-enhancing potential of bis(quercetinato)oxovanadium(IV)conjugate[J].Bioorg Med Chem Lett,2004,14(19):4961-4965.
[30]TAN Jun,WANG Bo Chu,ZHU Lian Cai.DNA binding,cytotoxicity,apoptotic inducing activity,and molecular modeling study of quercetin zinc(II)complex[J].Bioorg Med Chem Lett,2009,17(2):614-620.
[31]TAN Juun,ZHU Lian Cai,WANG Bo Chu.From GC-rich DNA binding to the repression of survivin gene for quercetin nickel(II)complex:implications for cancer therapy[J].Biometals,2010,23(6):1075-1084.
[32]TAN Jun,WANG Bo Chu,ZHU Lian Cai.DNA binding and oxidative DNA damage induced by aquercetin copper(II)complex:potential mechanism of its antitumor properties[J].J Biol Inorg Chem,2009,14(5):727-739.
[33]TAN Jun,WANG Bo Chu,ZHU Lian Cai.Hydrolytic cleavage of DNA by quercetin manganese(II)complexes[J].Colloids Surf B Biointerfaces,2007,55(2):149-152.
[34]谢伟玲,杨培慧,蔡继业.锗(Ⅳ)-槲皮素配合物的制备、表征及其抗氧化活性测定[J].分析化学,2010,38(12):1809-1812.
[35]陈小平.槲皮素合氨络铂抗癌药及其制备方法:中国,101177434A[P].2007-12-13.
[36]翟广玉,王 鹏,王 涛,等.槲皮素铂的合成:中国,101353339A[P].2008-09-16.
Research progress of synthesis and biological activity of quercetin derivatives
A review is provided of the progress of research on the synthesis and biological activity of quercetin derivatives.The methods for preparing quercetin amino acids,glycosides,esters,ethers derivatives and metal complexes as well as the current status of study on the biological activities of those derivatives are briefed.It is pointed out that,as a kind of flavonol compound extracted from natural plants,quercetin has many biological activities such as antioxidant,antibacterial,antihyper-tensive,anti-tumor and anti-mutation.However,the poor water solubility and low bioavailability of quercetin limit its clinical application.Therefore,domestic and foreign scholars have made efforts to modify the structure of quercetin and developed a series of novel lead compounds of quercetin,which,hopefully,is to provide references for the design and synthesis of novel quercetin derivatives.
quercetin;quercetin derivatives;synthesis;biological activities;research progress
O 625.32
A
1008-1011(2012)04-0101-10
2012-01-01.
渠文涛(1986-),男,硕士生,研究方向为有机合成及天然药物的结构修饰.*
,E-mail:zhaiguangyu1@sina.com.

