固定甘氨酸制备阳离子交换树脂及其吸附金属离子性能的研究
吕 哲,沈梓粤,秦宗华,李任强
(暨南大学生物工程学系,广东 广州510632)
甘氨酸分子结构有其特殊性,其α碳原子为非不对称碳原子,除了连接2个氢外,还连接有1个氨基和1个羧基[1,2]。如果将甘氨酸分子通过其氨基固定于惰性载体上,它的氨基与载体形成共价键,羧基则可通过α碳臂伸出成为配基,配基上的H+可以与碱性离子相互交换从而吸附这些离子,也就是说,这样固定甘氨酸可以制备阳离子交换树脂[3,4]。
环氧氯丙烷法常用于活化多羟基惰性载体[5]。在碱性条件下,环氧氯丙烷激活载体上的羟基并与之结合,其另一边则与氨基连接,本身又起到“接臂”作用。如果运用环氧氯丙烷法将甘氨酸固定在惰性载体上,“接臂”会较长。鉴于此,作者选择Sephadex G-25作为载体,利用环氧氯丙烷活化法将甘氨酸固定制备阳离子交换树脂,并探讨了所制备树脂对碱性金属离子的吸附性能。
1 实验
1.1 试剂与仪器
甘氨酸、氨水、环氧氯丙烷、Sephadex G-25、1,4-二氧六环、氯化镁、氯化钙、氯化钠、盐酸、EDTA、铬黑T。
紫外可见分光光度计、摇床、水浴锅、天平、布氏漏斗、恒流泵、层析柱、滴定管。
1.2 阳离子交换树脂的制备[5,6]
1.2.1 载体Sephadex G-25的活化
取适量的Sephadex G-25于烧结漏斗中抽气、过滤、抽干;称取24g(湿重),以300mL 1mol·L-1NaCl和300mL蒸馏水先后在漏斗上洗涤,抽干后移至小三角瓶内;加入19.5mL 2mol·L-1NaOH、4.5mL 环氧氯丙烷、15mL 56%的1,4-二氧六环,于40℃摇床中振摇活化2h后取出;在烧结漏斗中分别以蒸馏水和pH 值为9.5的0.2mol·L-1Na2CO3-NaHCO3缓冲溶液洗涤、抽干。
1.2.2 甘氨酸与载体的连接
取25mL 1mol·L-1的甘氨酸与活化载体Sephadex G-25混合,在40℃摇床上振荡偶联24h左右,用烧结漏斗过滤,收集滤液,并用少许蒸馏水淋洗一并收集,量体积,测甘氨酸含量,计算甘氨酸结合于载体的偶联率。
将偶联复合物(载体+甘氨酸)用pH值为9.5的0.2mol·L-1Na2CO3-NaHCO3缓冲溶液浸泡后装柱。用相同缓冲溶液平衡。
1.3 树脂吸附性能的测定
1.3.1 静态吸附
分别取一定浓度的CaCl2/MgCl2溶液35mL于具塞锥形瓶中,加入7g(湿重)的树脂,于恒温振荡器中以110r·min-1的转速振荡1h后,用EDTA滴定法测定溶液中Ca2+/Mg2+的浓度,按式(1)计算树脂的平衡吸附量(Qe,mg·g-1)。

式中:V 为溶液的体积,L;c0和ce分别为 Ca2+/Mg2+溶液初始浓度和平衡浓度,mg·L-1;W 为树脂质量,g。
1.3.2 动态吸附
准确称取一定量树脂,采用湿法装柱,即将树脂与去离子水混合后,从交换柱上端逐渐倒入以尽量避免带入气泡[7]。然后用pH 值为8.5的Tris-HCl溶液平衡柱子2h。将一定浓度的CaCl2/MgCl2溶液以一定的流速通过交换柱,定容接收流出液,测定Ca2+/Mg2+的浓度,绘制穿透曲线。
1.3.3 动态解吸
用去离子水将已吸附饱和的树脂洗净;以一定流速通入不同浓度的NaCl-HCl溶液进行洗脱再生,定容接收洗脱液,测定Ca2+/Mg2+的浓度,绘制洗脱曲线。按式(2)计算解吸率(y,%)。

式中:x1、x2分别为解吸得到的 Ca2+/Mg2+质量、树脂上吸附的Ca2+/Mg2+质量,g。
1.4 Ca2+/Mg2+浓度、质量的计算[8]
采用EDTA滴定法测定溶液中Ca2+/Mg2+的浓度。先配制pH值为10的氨性缓冲溶液(将6.7g NH4Cl溶于30mL水,再加入57mL氨水,稀释至100mL,混匀)。取5mL样液,加入1~2mL氨性缓冲溶液,再加入适量的铬黑T指示剂,用EDTA标准溶液滴定至溶液由酒红色变成蓝色为终点。平衡滴定2份,所消耗的EDTA标准溶液的体积差应小于0.1mL。按式(3)计算样液中 Ca2+/Mg2+的浓度(c,mol·L-1):

式中:V为样液体积,L;cEDTA为EDTA标准溶液的浓度,mol·L-1;VEDTA为滴定消耗EDTA标准溶液的体积,L。
按式(4)计算样液中Ca2+/Mg2+的质量(m,g):

式中:M为Ca2+/Mg2+的相对分子质量,g·mol-1。
2 结果与讨论
2.1 甘氨酸与载体的偶联率
用茚三酮比色法测定偶联后收集到的滤液中的甘氨酸含量(以1g Sephadex G-25偶联甘氨酸的毫克数表示)。通过偶联前后甘氨酸含量的变化得出结合甘氨酸的量为0.95g,从而算出偶联率为12mg·g-1。
2.2 树脂静态吸附特性[9~11]
2.2.1 吸附曲线(图1)
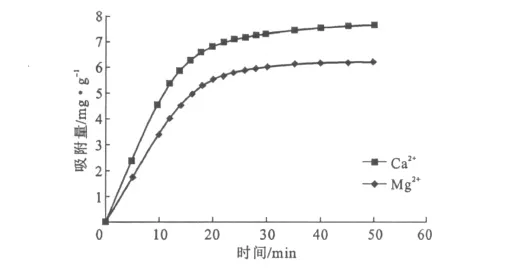
图1 树脂对Ca2+和 Mg2+的静态吸附曲线Fig.1 Static adsorption curves of resin for Ca2+ and Mg2+
由图1可看出,在吸附的前16min内,树脂对两种金属离子的吸附速率较快,分别达到饱和吸附量的82.8%(Ca2+)和80.5%(Mg2+);随后,随时间延长吸附量升幅趋缓,50min后达到平衡;平衡时,树脂对Ca2+的饱和吸附量为7.59mg·g-1、对 Mg2+的饱和吸附量为6.16mg·g-1。
2.2.2 金属离子初始浓度对树脂饱和吸附量的影响
在25℃下,Ca2+和Mg2+的初始浓度对树脂饱和吸附量的影响如图2所示。
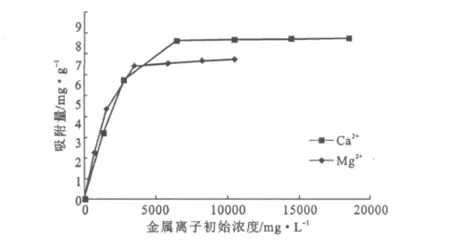
图2 Ca2+和Mg2+初始浓度对树脂饱和吸附量的影响Fig.2 Effect of initial concentration of Ca2+ and Mg2+on resin saturated adsorption capacity
由图2可看出,随着初始浓度的增大,金属离子在树脂上的饱和吸附量先迅速升高,而后逐渐趋于稳定。当Ca2+初始浓度增大至8000mg·L-1时,饱和吸附量为7.59mg·g-1;当 Mg2+初始浓度增大至4800 mg·L-1时,饱和吸附量为6.16mg·g-1。这是因为,金属离子浓度较小的情况下,树脂的吸附位点未达到饱和,吸附位点较多,此时树脂的饱和吸附量取决于溶液中的金属离子浓度;当金属离子浓度增大至一定程度时,吸附剂的吸附位点完全被金属离子结合,继续增大金属离子浓度对树脂的饱和吸附量影响不大。
2.2.3 树脂对Ca2+和 Mg2+的等温吸附模型
将图2中实验数据分别与Langmuir及Freundlich等温吸附方程[12,13]进行拟合,结果见表1 。

表1 等温吸附方程(T=278K)Tab.1 Isothermal adsorption equations(T=278K)
由表1 可知,Langmuir等温吸附方程较Freundlich等温吸附方程能更好地拟合树脂对Ca2+和Mg2+的吸附过程,其相关系数均在0.99以上。
2.3 树脂动态吸附特性
2.3.1 穿透曲线
取10g树脂装柱,在室温下,将初始浓度分别为8000mg·L-1和4800mg·L-1的CaCl2和 MgCl2溶液以1mL·min-1流速通过柱子,其穿透曲线如图3所示。
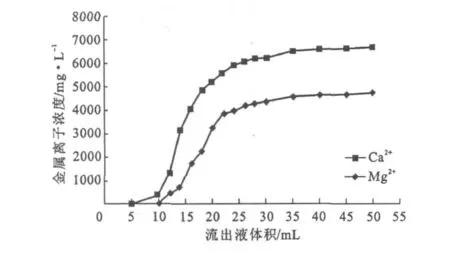
图3 树脂装柱后的吸附穿透曲线Fig.3 Adsorption breakthrough curves of the column made by resin
由图3可见,当Ca2+和Mg2+流出液体积分别为10mL和12mL时,流出液中Ca2+和Mg2+的最大浓度分别为384.6mg·L-1和480mg·L-1,此时可作为穿透点[14],10mL和12mL为穿透体积;之后流出液中Ca2+和Mg2+的浓度随流出液体积的增加而迅速升高,当流出液体积均为35mL时,Ca2+和Mg2+的浓度升幅趋缓,说明树脂对Ca2+和Mg2+的吸附已经饱和。经累积计算,树脂对Ca2+和Mg2+的动态饱和吸附量分别为10.83mg·g-1和8.80mg·g-1。由此可看出,对于相同的树脂,动态饱和吸附量明显高于静态饱和吸附量。这是因为,在静态吸附过程中,溶液中金属离子的量随着吸附的进行逐渐降低,树脂吸附金属离子的量逐渐增加,两者最终达到吸附静态平衡;而动态吸附流经树脂层的金属离子始终保持较高浓度,促进了树脂的吸附。
2.3.2 进液流速对动态吸附的影响
在室温下将初始浓度为8000mg·L-1和4800 mg·L-1的CaCl2和MgCl2溶液以不同的流速通过直径为1.6cm的交换柱,直至吸附饱和,结果如表2 所示。
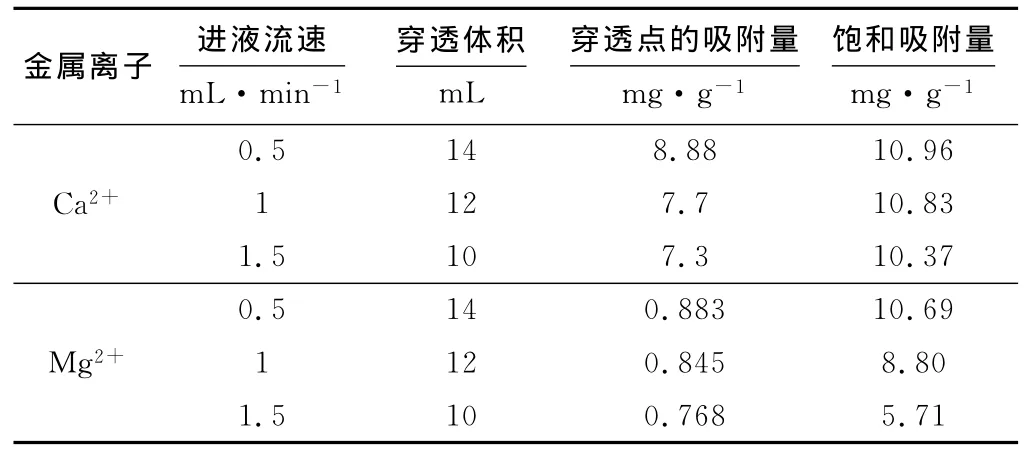
表2 进液流速对动态吸附的影响Tab.2 Effect of flow rate on the dynamic adsorption
由表2 可知,进液流速越大,穿透体积越小,穿透点提前。这是因为,进液流速加快,金属离子与树脂的接触时间缩短,影响其被充分吸附。考虑到吸附量大小和树脂单位时间处理能力的高低,选择动态吸附的进液流速为1mL·min-1。
2.3.3 树脂pH值对动态吸附的影响
pH值可以影响树脂表面的电荷以及树脂的离子化程度[15,16]。分别用不同 pH 值的0.05mol·L-1Tris-HCl溶液平衡树脂2h,然后在室温下测定树脂对Ca2+和Mg2+的动态饱和吸附量,结果如图4所示。
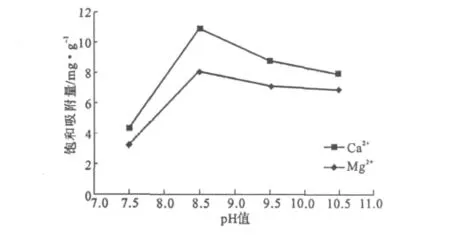
图4 pH值对动态吸附的影响Fig.4 Effect of pH value on the dynamic adsorption
由图4可看出,pH值为8.5时的吸附效果最好。因此,选用pH 值为8.5的0.05mol·L-1Tris-HCl溶液作为平衡液。
2.3.4 洗脱流速对解吸效果的影响
用去离子水将交换柱中吸附饱和的树脂洗净,室温下分别用pH 值为1.5的1mol·L-1NaCl-HCl溶液以不同流速解吸,定容接收洗脱液,测定Ca2+和Mg2+的浓度,绘制洗脱曲线,结果见图5。
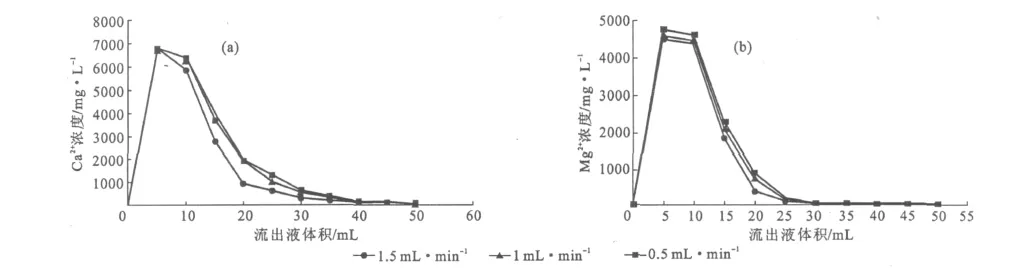
图5 洗脱流速对Ca2+(a)和 Mg2+(b)解吸效果的影响Fig.5 Effect of flow rate on the desorption of Ca2+(a)and Mg2+(b)
由图5可看出,洗脱流速较慢时,Ca2+的洗脱峰尖、宽且峰值变大,Mg2+的洗脱也有相同的趋势。通过累计积分计算得到,流出液体积为50mL时相对于0.5mL·min-1、1mL·min-1、1.5mL·min-1的洗脱流速,Ca2+的解吸率分别约为98.6%、95.9%和85.3%,Mg2+的解吸率分别约为91.3%、85.9%和69.1%,说明低洗脱流速效果较好。同时,累计积分曲线显示,洗脱液中Ca2+和Mg2+浓度的变化规律一致,流出液体积达到30mL后,曲线斜率均变小,Ca2+和Mg2+的浓度减小速度减慢;流出液体积达到40mL(约4.4倍树脂体积)后,曲线趋于平缓,Ca2+和 Mg2+的浓度变化不大。因此,为了洗脱完全,实验中加入55mL(约6倍树脂体积)洗脱液对树脂进行洗脱。
2.4 稳定性实验
取10g树脂装柱,室温下将60mL初始浓度分别为8000mg·L-1和4800mg·L-1的CaCl2和 MgCl2溶液以1mL·min-1的流速上交换柱,确保树脂吸附达饱和;然后用pH 值为1.5的1mol·L-1NaCl-HCl溶液以0.5mL·min-1流速洗脱,并用pH 值为8.5的0.05mol·L-1Tris-HCl溶液作为平衡液进行再生,如此重复进行5次吸附/解吸实验,考察树脂对Ca2+和Mg2+吸附/解吸性能的稳定性,结果见表3 。
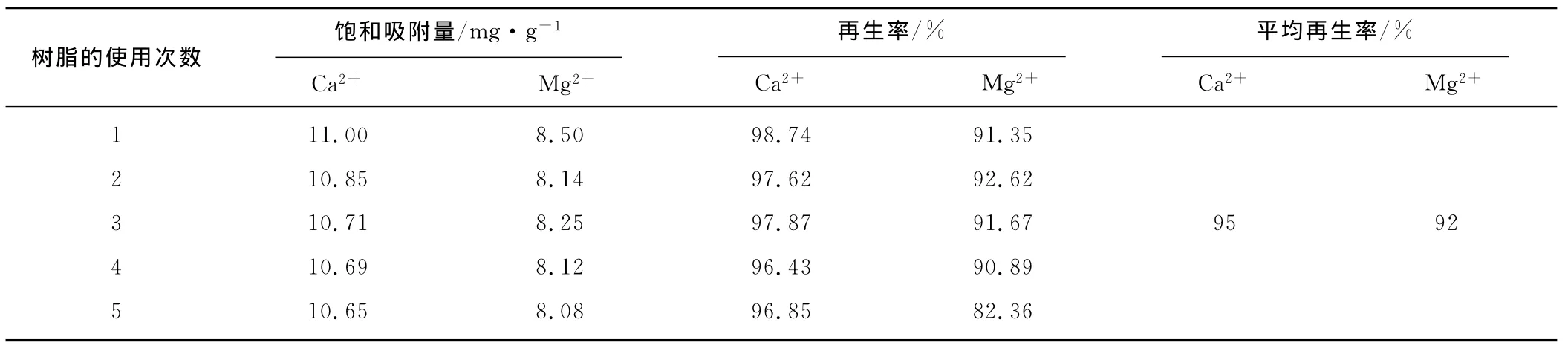
表3 稳定性实验结果Tab.3 Results of the stability experiment
由表3 可知,在选定的吸附和洗脱条件下,树脂对Ca2+和Mg2+的吸附/解吸性能比较稳定,其中Ca2+的平均再生率为95%、Mg2+的平均再生率也达92%,说明树脂可多次重复使用。
3 结论
(1)利用环氧氯丙烷活化法可以将甘氨酸很好地固定到Sephadex G-25上,从而制备出弱酸性阳离子交换树脂,偶联率为12mg·g-1。
(2)固定甘氨酸制备的阳离子交换树脂可吸附水中Ca2+和Mg2+等金属离子。树脂对Ca2+和 Mg2+的静态饱和吸附量分别为7.59mg·g-1和6.16mg·g-1,而动态饱和吸附量则分别达10.83mg·g-1和8.80mg·g-1。树脂对金属离子的吸附符合Langmuir等温吸附方程,相关系数R2达0.99以上。
(3)选择pH 值为8.5的0.05mol·L-1Tris-HCl溶液作为树脂的平衡液,平衡2h,可使树脂达到良好的吸附状态。Ca2+和 Mg2+溶液进液流速越快,树脂动态吸附金属离子的穿透体积越小,穿透点前的累计吸附量也越小;同样的,洗脱流速越慢,洗脱效果越好。树脂交换柱较好的操作条件为:以pH值为8.5的0.05mol·L-1Tris-HCl溶液作为平衡液,上样流速1mL·min-1;以pH值为1.5的1mol·L-1NaCl-HCl溶液作为洗脱液,洗脱流速0.5mL·min-1。
(4)在最佳吸附和洗脱条件下,树脂对Ca2+和Mg2+有良好的吸附/解吸性能和机械性能,再生效果好,可多次重复使用。在富集金属离子、对污水和硬水处理等方面具有良好的应用前景。
[1]和芹,王克诚,周立新.甘氨酸与二价金属离子相互作用的理论研究[J].南开大学学报(自然科学版),2007,40(4):36-41.
[2]赵强,廖天录,王俊峰,等.研析甘氨酸与二价金属离子配合物的循环伏安行为[J].通化师范学院学报,2010,31(10):31-32.
[3]樊天霖,陈纪海.大孔螯合型丙烯酸系氨羧基离子交换树脂[J].化学试剂,1980,(5):55-59.
[4]耿军.络合萃取法及离子交换法处理DMA废水的研究[D].合肥:合肥工业大学,2009.
[5]李任强,周天鸿,李月琴,等.生物技术实验精选[M].广州:暨南大学出版社,2006:192-194.
[6]李江,杜开峰,朱卫霞,等.甘氨酸修饰大孔纤维素微球的制备及其对Cr3+、Fe3+的吸附研究[J].工业水处理,2011,31(5):58-61.
[7]钱庭宝.离子交换剂应用技术[M].天津:天津科学技术出版社,1984:277-278.
[8]高丽华.基础化学实验[M].北京:化学工业出版社,2004:119-121.
[9]孟媛媛,胡勤海,陆侨治,等.离子交换树脂处理二甲胺废水的研究[J].环境污染与防治,2010,32(9):58-63.
[10]潘高峰.合成革工业废水中低浓度DMA的分离研究[D].合肥:合肥工业大学,2009.
[11]魏凤玉,耿军.一种离子交换法处理二甲胺废水的方法[P].CN 101 337 707,2009-01-07.
[12]陈云嫩,丁元春.谷壳对水中镉离子的吸附动力学及热力学研究[J].安徽农业科学,2009,37(7):3190-3192.
[13]Huang Xin,Gao Nai-yun,Zhang Qiao-li.Thermodynamics and kinetics of cadmium adsorption onto oxidized granular activated carbon[J].Journal of Environmental Sciences,2007,19(11):1287-1292.
[14]范晨曦.大孔苯乙烯系螯合树脂对铅的吸附行为及其应用[D].南京:南京理工大学,2008.
[15]Chiarle S,Ratto M,Rovatti M.Mercury removal from water by ion exchange resins adsorption[J].Water Research,2000,34(11):2971-2978.
[16]Bayramogolu G,Altintas B,Arica M Y.Adsorption kinetics and thermodynamic parameters of cationic dyes from aqueous solutions by using a new strong cation-exchange resin[J].Chemical Engineering Journal,2009,152(2-3):339-346.

