质谱动力学方法原理及应用
李 明,李红梅,熊行创,江 游,黄泽建,方 向
(中国计量科学研究院,北京 100013)
质谱动力学方法原理及应用
李 明,李红梅,熊行创,江 游,黄泽建,方 向
(中国计量科学研究院,北京 100013)
质谱动力学方法(Kinetic Method,简称KM法)是一种基于经质量选择的簇离子竞争解离反应速率的不同对热力学数据进行测定的方法,由于采用串联质谱技术,分析样品无需纯化,具有简便、快速、灵敏等优点。目前该方法已应用于气相酸碱度和质子亲合势的测定、电子亲和能的测定、电离能的测定、多电荷生物分子气相碱度的测定、金属离子与生物分子亲和力的测定、异裂离解能的测定、离子结构的检测及对手性化合物对映体过量的测定等。本工作在介绍质谱动力学方法原理的同时,列举了其应用实例,详细地对质谱动力学方法进行了综合述评。
动力学方法;簇离子;串联质谱;热力学
1 质谱动力学方法的原理及发展
在质谱学中,很早就发现在热力学控制下活化离子有竞争碎裂行为,Stevenson规则认为:从同一复合物碎裂得到两个碎片的过程中,基于电离能的不同,碎裂时两个碎片会争夺电荷[1]。Cooks等进行质量分析离子动能谱 (Mass Ana-lyzed Ion Kinetic Energy Spectrum,MIKE)的研究中发现,共享质子的氨基酸二聚体经质量选择后进行亚稳离子解离,产物离子的丰度比与单体的性质有关[2]。在这一实验结果的推动下,发展了可获得相对热力学信息的定量方法——质谱动力学方法。该方法研究的是簇离子的两个竞争解离反应:
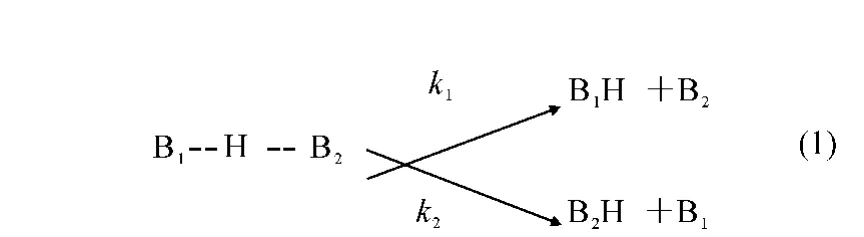
其中k1、k2分别为两种反应途径的反应速率常数,忽略碎裂过程的熵变,簇离子碎裂反应的速率与两种反应途径的焓变的差值相关,产物丰度比的自然对数与相关热力学值的差值成线性关系:

这里,Q1*和Q2*指两种解离途径不同过渡态的配分函数,Δε0为反应活化能的差值,R为理想气体常数,Teff为有效温度(在KM法中与簇离子平均内能相关的一个参数,活化簇离子的内能随碰撞能量或碰撞气体的压力改变,Teff也随之改变)。
质谱动力学方法最初采用近似的形式[3],尤其是关于内能的分布(波尔兹曼分布)和忽略熵变的假定。方程(2)的理论推导过程中用到绝对速率理论,它的前提是反应在平衡条件下进行,簇离子裂解显然是在非平衡条件下进行的,内能分布不遵循波尔兹曼分布。近年来,基于RRK(Rice-Ramsperger-Kassel)和 RRKM (Rice-Ramsperger-Kassel-Marcus)理论推导出相同的方程式,并未涉及到热平衡,解决了关于体系内能分布的问题[4-5]。
如果两种碎裂方式过程中的熵变不能忽略,可通过改变碰撞能量进行多次碰撞诱导解离(Collision Induced Dissociation,CID)来测定反应的热力学数据,具体做法如下[6]:


以ln(kunknown/kref)对 ΔHref作图,曲线斜率为1/(RTeff)。采用不同的能量进行碰撞诱导解离,可得到不同的Teff,同时ΔGapp可通过方程(3)的曲线在横轴上的截距求得。通过ΔGapp/Teff对1/Teff的作图得到方程(5)所对应的曲线,斜率为待测物解离的焓变,在y轴上的截距为竞争解离反应熵变的差值。
2 动力学方法的应用
KM法最大的优点是具有很高的灵敏度,甚至可以检测到由同位素取代引起的热力学性质的细微变化。Cooks等利用KM法对氘代乙腈的质子亲和势测量结果为(186.3±1.2)kcal/mol,而乙腈的质子亲和势为(188.2±1.2)kcal/mol[7];另外,由于采用了串联质谱技术,待测物无需纯化,同时具有快速、操作简单等优点,因此被广泛应用于热力学参数和化合物结构的测定,并且越来越多地应用于生物分子热力学性质的研究[6]。
2.1 气相酸碱度和质子亲和势的测定
分子的气相碱度和质子亲和势是气相离子化学反应中的两个重要参数,它们直接给出分子Brostead酸碱性,还能提供其结构以及活性的信息;另外,分子气相碱度是分子本身固有的碱度,可用来阐明液相碱度顺序的起因。因此研究分子的气相碱度和质子亲和势具有重要的理论意义和实用价值。质谱动力学方法被广泛地应用于有机化合物质子亲和势和气相酸碱度的测量[2,8-21]。共享质子的二聚体自发解离或碰撞诱导解离,产生两种离子的丰度比的自然对数(ln k1/k2)与分子的气相碱度或质子亲合势的差值成线性关系。在质谱动力学方法发展初期,对样品进行测定时使用的参考物必须与样品具有相似结构,使两种解离途径的熵变近似相等,见方程(2)。赵玉芬教授[22]测定了磷酰化丙二肽的气相质子亲和能在957.5~965.1kJ/mol之间。后来这种限制逐渐被打破,并能够得到反应的熵变信息,例如Zheng等[23]对尿素的气相碱度和质子亲合势进行了测定,不仅测得了气相碱度为 (838.7±3.0)kJ/mol、质子亲 和势 为(868.4±2.5)kJ/mol,还同时得到了尿素质子化过程中的熵变为(9.4±0.5)J/mol·K。Ren等[24]对半胱氨酸-多丙氨酸肽的气相酸度进行测量,HSCA3和HSCA4去质子过程的焓变分别为(317.3±2.4)kcal/mol和(316.2±03.9)kcal/mol,考虑熵变后,测得的气相酸度分别为(322.1±2.4)kcal/mol和 (320.1±3.9)kcal/mol。
2.2 电离能
电离能(Ionization Energy,简称IE)由分子的原子核结构和核外电子结构共同决定,电离能被用于有机化合物结构与性能关系和结构与活性关系的研究。通常用来测定电离能的方法有电子撞击法、光电光谱法、电荷交换法、光电离方法等。利用正簇离子的解离,提供了一种测定IE较为简便的方法:由一级质谱选出的二聚体的自由基阳离子离解途径有两种。
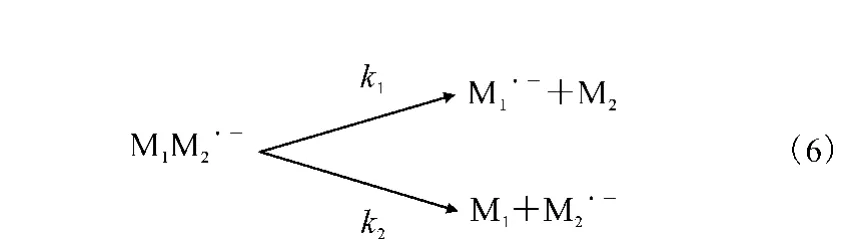
产物自由基阳离子的丰度比与电离能差值存在以下近似关系:

负号表示离子丰度越高,电离能越低。该方法已被成功地用于芳香碳氢化合物和苯胺的电离能的检测[25-26],其灵敏度很高,甚至可识别异构体的电离能差值[26]。
2.3 电子亲和能
原子(或分子)的电子亲和能是指当一个电子加在一个中性原子(或分子)上形成负离子的过程所释放的能量。与电离能相反,它反映了原子(分子)得到电子的能力。然而由于实验技术的限制,目前可供利用的有机化合物电子亲和能的数据还较少。KM法则可用于电子亲和能的测定。诸如芳香类碳氢化合物产生的负电荷簇离子经诱导解离产生自由基阴离子。
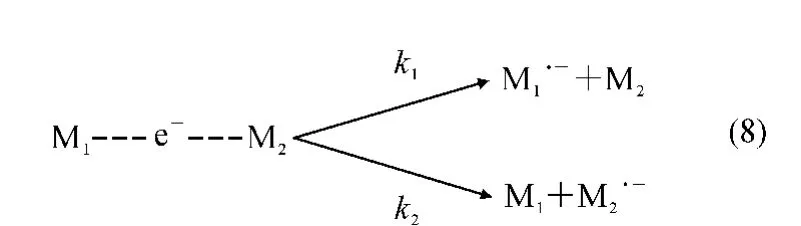
与共享质子的二聚体相似,共享电子的二聚体解离后生成的离子丰度比与电子亲和能(ΔEA)有关:

Denault等[27]利用该方法测定了环辛四烯(COT)的电子亲和能为(0.58±0.10)eV,与电子转移法测定的结果(0.55±0.02)eV基本一致,他们还同时得到了两种反应途径熵变的差值为(25.6±10.0)J/mol·K。Wenthold等[28]利用该方法测定了α—和β—萘自由基的电子亲和能分别为(33.0±1.4)kcal/mol和(31.4±1.0)kcal/mol,并且同时获得了碳氢键的键能分别为(113.4±5.2)kcal/mol和 (115.4±4.9)kcal/mol。
将方法 1.3.1所提取到的花桥板栗淀粉配置成质量分数为10%的淀粉悬浊液,置于90 ℃热水中加热糊化30 min后,分别移装于平皿(90×15 mm)中并在室温条件下冷却,即得相态转变次数0次的淀粉凝胶样品。再将剩余淀粉凝胶依次移装密封置于-18 ℃的冰箱中进行冷冻处理,冷冻 22 h之后,将其放入30 ℃温水中进行融化,融化时间为2 h。至此获得水分子相态转变1次后的花桥板栗淀粉凝胶。按此方法依次制备相态转变次数为1、2、3、4、5、6、7次的淀粉凝胶样品,备用。
2.4 多电荷生物分子气相碱度
多电荷生物分子的气相碱度是研究生物分子活性的一个重要参数。通过对共享质子的肽和参考物(B)形成的二聚体碰撞诱导解离,可获得多电荷肽的气相碱度。
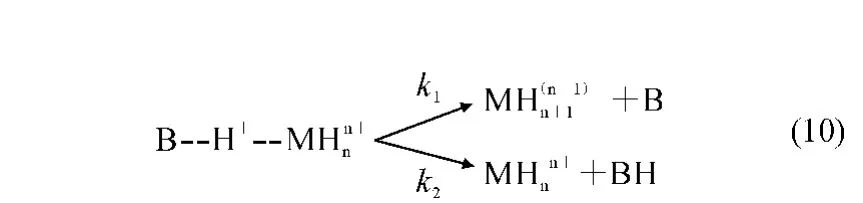
应用质谱动力学方法时,对于单电荷簇离子,可假定可逆活化能能垒为零或两种反应途径可逆活化能能垒相等;然而在双电荷簇离子的离解过程中,MH+和BH+的静电斥力必然会强加一个可逆活化能能垒ε0r。因此有:

它含有库仑斥力项δ,如果可逆活化能能垒ε0r与库仑斥力δ相等,ΔGB的值就可从方程(11)获得。Kaltashov等[29]应用该方法测定了质子化缓激肽的气相碱度为(217.8±1.7)kcal/mol。
2.5 异裂离解能的测定
通过测定[C1AC2]+解离产生的离子丰度比,可测定异裂离解能(C和A分别代表阳离子和阴离子)。与共享质子的簇离子一样,这些由共享阴离子的簇离子竞争解离的速率与阴离子和两种不同阳离子的结合力有关。Wu等[30]对共享氯离子的簇离子[Rb-35Cl-Mi]+(Mi=Na,K,Cs)进行解离,测得RbCl的异裂离解能为(480.8±8.5)kJ/mol,与通过热力学循环计算的数值(482.0±8.0)kJ/mol一致。
2.6 金属离子亲和势
金属离子亲和势在催化体系和生物体系中的地位越来越受到重视,例如,Ca2+与肽的亲和势已有报道[31-32],与相应的质子亲和势相比,金属离子与氨基酸的亲和势大小的顺序有所不同。例如Cu+与20种基本氨基酸的亲和势和相应质子亲和势的顺序大不相同,半胱氨酸与Cu+具有很高的亲和势,但具有较低的质子亲和势,而脯氨酸却相反,这是因为Cu+作为一种软酸可以与半胱氨酸中的SH形成较稳定的化学键[33]。
2.7 金属和生物分子配合物的结构
通过多次碰撞诱导解离,质谱动力学方法可用来测定反应熵变的差值Δ(ΔS),从而可以推测出核酸碱基与金属离子的结合机制。Cerda等[34]对共享钾离子的嘧啶和腺嘌呤二聚体进行研究,通过对二聚体离子碰撞诱导解离测得Δ(ΔS)为+6.9J/mol·K。两种反应途径熵变的差值表明腺嘌呤取代氨基参与了K+的成键,鸟嘌呤和胞核嘧啶与腺嘌呤相似,而胸腺嘧啶和尿嘧啶则不同,这是因为它们没有与钾离子配合的合适构型。
2.8 手性化合物对映体过量的测定
基于质谱串联技术的动力学方法可用来测定手性化合物的对映体过量值,而且可对复杂样品进行测定,不需提纯,具有快速、高灵敏度、高精确度等优点[35]。方法分别采用[MII(A)(ref*)2-H]+或[MII(ref*)(A)2-H]+作为母离子,碰撞诱导解离后,丢失一分子分析物(A)或一分子辅助配体(ref*)。根据不同构象的分析物形成子离子丰度比的不同对同分异构体进行区分和定量。李明等[36-37]已对质谱动力学方法对手性化合物进行分析的原理进行了详细综述,本工作只对其最近进展进行总结和评述。Charles等[38]对3种糖的同分异构体进行同时区别和定量;Yong-Ill Lee等[39]采用单比法测定了甲状腺激素的同分异构体3,5,3-三碘甲腺原氨酸和三碘甲腺原氨酸;Karel Lemr等[40]在液相色谱分离后采用动力学方法对苯丙氨酸等分析物进行测定;张靖云等[41]将动力学方法与常压质谱技术结合,通过加速挥发游离方式对复杂基体样品(如血液和尿液)进行直接进样和离子化,测定了同分异构体非对称性二甲基精氨酸和对称性二甲基精氨酸的气相酸度分别为1361.6 kJ/mol和1361.2kJ/mol,并能够对同分异构体进行区分和定量测量;Lemr等[42]采用电喷雾解吸技术 (Desorption Electrospray Ionization,DESI)对血液样品中药物(如多巴、麻黄素、布洛芬等)进行直接手性区分和定量;近期,孔祥蕾[43]发现了二价金属连接的三聚体的新解离途径,对65Cu形成的三配体簇离子进行碰撞诱导解离,簇离子丢失分析物(或辅助配体)的自由基,而非完整分子,这种新的解离途径的手性识别能力明显优于丢失完整分子的解离途径;Leveque等[44]对甘油三酯区域异构体进行了区分和定量测定;Mohamed等[45]对寡糖的异构体进行了区分和定量;Berkecz等[46]利用该方法对β-3-高氨基酸进行了手性识别。
2.9 其他应用
Avila-Sal等[47]应用质谱动力学方法研究了一系列聚酰胺树枝状分子与萘普生等非甾体消炎药的相互作用,这对于开发新的药物载体有所助益。
3 结 语
采用串联质谱技术的动力学方法可被广泛应用于热力学性质的检测。热力学性质的很小差别对反应速率常数的影响也很大,因此该方法具有较高的灵敏度,不仅可以给出热力学数据,而且在一定条件下可以得到离子结构、立体效应等。该方法可应用于大分子质量生物分子与金属离子成键的研究;并且可用于多电荷阴离子、阳离子、有机盐簇离子的研究及主-客体结合能、大分子电离能和电子亲和能的测定。随着常压质谱技术[48-51]的发展,质谱动力学方法有望用于复杂基体样品中目标物热力学性质的直接测量以及复杂基体样品中同分异构体的区分和定量。
[1] STEVENSON D P.Ionization and dissociation by electronic impact.the ionization potentials and energies of formation of sec.-propyl and tert.-butyl radicals.some limitations on the method[J].Discuss Faraday Soc,1951,10:35-45.
[2] COOKS R G,KRUGER T L.Intrinsic basicity determination using metastable ions [J].J Am Chem Soc,1977,99:1 279-1 281.
[3] MCLUCKEY S A,CAMERON D,COOKS R G.Proton affinities from dissociations of protonbound dimers[J].J Am Chem Soc,1981,103:1 313-1 317.
[4] CRAIG S L,ZHONG M L,CHOO B,et al.Branching ratios in activated systems [J].J PhysChem A,1997,101(1):19-24.
[5] BOJESEN G,BREINDAHL T.On the proton affinity of someα-amino acids and the theory of the kinetic method[J].J Chem Soc,Perkin Trans 2,1994,(5):1 029-1 037.
[6] COOKS R G,WONG P S H.Kinetic method of making thermochemical determinations:advances and applications[J].Acc Chem Res,1998,31(7):379-386.
[7] WILLIAMS T L,DENAULT J W,COOKS R G.Proton affinity of deuterated acetonitrile estimated by the kinetic method with full entropy analysis[J].Int J Mass Spectrom,2001,(210/211):133-146.
[8] HOLMES J L,AUBRY C,MAYER P M.Proton affinities of primary alkanols:an appraisal of the kinetic method[J].J Phys Chem A,1999,103(6):705-709.
[9] COOKS R G,PATRICK J S,MCLUCKEY S A.Thermochemical determinations by the kinetic method[J].Mass Spectrom Rev,1994,13(4):287-339.
[10] MAJUMDAR T K,CLAIRET F,COOKS R G,et al.Epimer distinction and structural effects on gas-phase acidities of alcohols measured using the kinetic method[J].J Am Chem Soc,1992,114:2 897-2 903.
[11] KLOTS C E.Comment on“branching ratios in activated systems”[J].J Phys Chem A,1997,101:5 378-5 378.
[12] GRAUL S T,SCHNUTE M E,SQUIRES R R.Gas-phase acidities of carboxylic acids and alcohols from collision-induced dissociation of dimer cluster ions [J].Int J Mass Spectrom Ion Process,1990,96(2):181-198.
[13] HAAS M J,HARRISON A G.The fragmentation of proton-bound cluster ions and the gasphase acidities of alcohols[J].Int J Mass Spectrom Ion Process,1993,124:115-124.
[14] CHENG X H,WU Z,FENSELAU C.Collision energy dependence of proton-bound dimer dissociation:entropy effects,proton affinities,and intramolecular hydrogen-bonding in protonated peptides[J].J Am Chem Soc,1993,115:4 844-4 848.
[15] GAL J F,HERREROS M,MARIA P C,et al.On the use of the kinetic method for the determination of proton affinities by fourier-transform ion cyclotron resonance mass spectrometry[J].Rapid Commun Mass Spectrom,1996,10(2):242-245.
[16] CHEN G,KASTHURIKRISHNSN N,COOKS R G.Proton affinity of the stable free radical 2,2,6,6-tetramethyl-l-piperidinyloxy measured by the kinetic method[J].Int J Mass Spectrom Ion Process,1995,151:69-75.
[17] CACAE F,PETRIS G DE,PEPI F,et al.Gasphase nitronium ion affinities [J].Proc Natl Acad Sci,1995,92:8 635-8 639.
[18] TAN J P,REN J H.Determination of the gasphase acidities of cysteine-polyalanine peptides using the extended kinetic method[J].J Am Soc Mass Spectrom,2007,18(2):188-194.
[19] ANDRIOLE E J,COLYER K E,CORNELL E,et al.Proton affinity of canavanine and canaline,oxyanalogues of arginine and ornithine,from the extended kinetic method [J].J Phys Chem,2006,110(40):11 501-11 508.
[20] WIND J J,PAPP L,HAPPEL M,et al.Proton affinity of beta-oxalylaminoalanine(BOAA):Incorporation of direct entropy correction into the single-reference kinetic method [J].J Am Soc Mass Spectrom,2005,16(7):1 151-1 161.
[22] 陈 晶,陈 益,赵玉芬,等.电喷雾质谱动力学方法测定磷酰化丙丙二肽的气相质子亲和能[J].高等学校化学学报,2003,24(3):459-461.
[23] ZHENG X,COOKS R G.Thermochemical determinations by the kinetic method with direct entropy correction[J].J Phys Chem A,2002,106:9 939-9 946.
[24] TAN J P,REN J H.Determination of the gasphase acidities of cysteine-polyalanine peptides using the extended kinetic method[J].J Am Soc Mass Spectrom,2007,18(2):188-194.
[25] WONG P S H,MA S,COOKS R G.Ionization energy determination by the kinetic method[J].Anal Chem,1996,68:4 254-4 256.
[26] DENAULT J,CHEN G,COOKS R G.Estimation of ionization energies of substituted anilines by the kinetic method[J].Int J Mass Spectrom Ion Process,1998,175(1/2):205-213.
[27] DENAULT J,CHEN G,COOKS R G.Electron affinity of 1,3,5,7-cyclooctatetraene determined by the kinetic method[J].J Am Soc Mass Spectrom,1998,9:1 141-1 145.
[28] LARDIN,H A,SQUIRES R R,WENTHOLD P G.Determination of the electron affinities of alpha-and beta-naphthyl radicals using the kinetic method with full entropy analysis.The C-H bond dissociation energies of naphthalene[J].J Mass Spectrom,2001,36(6):607-615.
[29] KALTASHOV I A,FENSELAU C.Thermochemistry of multiply charged melittin in the gas phase determined by the modified kinetic method[J].Rapid Commun Mass Spectrom,1996,10:857-861.
[30] WU L,DENAULT J W,COOKS R G.Alkali halide cluster dissociation examined by the kinetic method:heterolytic bond dissociation energies,effective temperatures and entropic effects[J].J Am Soc Mass Spectrom,2002,13:1 388-1 395.
[31] NEMIROVSKIY O V,RAMANATHAN R,GROSS M L.Investigation of calcium-induced,noncovalent association of calmodulin with melittin by electrospray ionization mass spectrometry[J].J Am Soc Mass Spectrom,1997,8(8):809-812.
[32] NEMIROVSKIY O V,GROSS M L.Intrinsic Ca2+affinities of peptides:application of the kinetic method to analogs of calcium-binding site III of rabbit skeletal troponin C[J].J Am Soc Mass Spectrom,2000,11(9):770-779.
[33] CERDA B A,WESDEMIOTIS C.The relative copper(i)ion affinities of amino acids in the gas phase[J].J Am Chem Soc,1995,117(38):9 734-9 739.
[34] CERDA B A,WESDEMIOTIS C.Li+,Na+,and K+binding to the DNA and RNA nucleobases.bond energies and attachment sites from the dissociation of metal ion-bound heterodimers[J].J Am Chem Soc,1996,118(47):11 884-11 892.
[35] TAO W A,COOKS R G.Chiral analysis by mass spectrometry [J].Anal Chem,2003,75:25A-31A.
[36] 李 明,刘淑莹,金钦汉,等.质谱动力学方法在手性分析中的应用 [J].化学进展,2006,18(10):1 369-1 374.
[37] 于 擎,曹 洁.质谱动力学方法在手性识别及对映体过量值方面的原理及应用 [J].质谱学报,2009,30(3):179-190.
[38] FOUQUET T,CHARLES L.Distinction and quantitation of sugar isomers in ternary mixtures using the kinetic method [J].J Am Soc Mass spectrom,2010,21(1):60-67.
[39] KUMAR A P,JIN H,LEE Y I,et al.Isomeric discrimination and quantification of thyroid hormones,t3and rt3,by the single ratio kinetic method using electrospray ionization mass spectrometry[J].J Am Soc Mass Spectrom,2010,21:14-22.
[40] LEMR K,RANC V,FRYĈÁK P,et al.Chiral analysis by mass spectrometry using the kinetic method in flow systems[J].J Mass Spectrom,2006,41(4):499-506.
[41] 张净云.以动力学法和加速挥发方式快速侦测样品中的特定成分[D].国立高雄大学硕士论文,2010.
[42] RAC V,HAVLÍĈEK V,LEMR K,et al.Nanodesorption electrospray and kinetic method in chiral analysis of drugs in whole human blood samples[J].Eur J Mass Spectrom,2008,14(6):411-417.
[43] KONG X.Chiral differentiation of amino acids by the kinetic method by fourier transform ion cyclotron resonance mass spectrometry via a different dissociation pathway [J].Rapid Commun Mass Spectrom,2012,26:870-873.
[44] LEVEQUE N L,ACHEAMPONG A,HERON S,et al.Determination of triacylglycerol regioisomers using electrospray ionization-quadrupole ion trap mass spectrometry with a kinetic method[J].Anal Chim Acta,2012,722:80-86.
[45] MOHAMED M,THIERRY F,LAURENCE C.Isomeric distinction of small oligosaccharides:a bottom-up approach using the kinetic method[J].J Am Soc Mass Spectrom,2011,22(7):1 252-1 259.
[46] BERKECZ R,HYYRYLAINEN A R M,FULOP F,et al.Chiral discrimination of beta-3-homo-amino acids using the kinetic method [J].J Mass spetrom,2010,45(11):1 312-1 319.
[47] AVILA-SALAS F,SANDOVAL C,CABALLERO J,et al.Study of interaction energies between the pamam dendrimer and nonsteroidal anti-inflammatory drug using a distributed computational strategy and experimental analysis by ESIMS/MS[J].J Phys Chem B,2012,116 (7):2 031-2 039.
[48] 李 明,姜 杰,李红梅,等.电喷雾萃取电离技术在蛋白质分析中的应用及展望 [J].生物化学与生物物理进展,2012,39(2):194-198.
[49] CHEN H W,HU B,ZHANG X.Fundamental principles and practical applications of ambient ionization mass spectrometry for direct analysis of complex samples [J].Chinese J Anal Chem,2010,38(8):1 069-1 088.
[50] VENTER A,NEFLIU M,COOKS R G.Ambient desorption ionization mass spectrometry[J].Trend Anal Chem,2008,27(4):284-290.
[51] HUANG M Z,CHENG S C,SHIEA J,et al.Ambient ionization mass spectrometry:a tutorial[J].Anal Chim Acta,2011,702(1):1-15.
Theory and Application of Mass Spectrometric Kinetic Method
LI Ming,LI Hong-mei,XIONG Xing-chuang,JIANG You,HUANG Ze-jian,FANG Xiang
(National Institute of Metrology,Beijing100013,China)
The mass spectrometric kinetic method based on the competitive dissociations of mass-selected cluster ions has been increasingly applied to thermochemical determination mainly due to its simplicity,speediness and sensitivity.Because the kinetic method employs tandem mass spectrometry,the compounds of interest need not be available in pure form.The kinetic method has been used to estimate gas-phase acidity and basicity and proton affinity,electron affinity,ionization energy,gas-phase basicities of multiply-charged biomolecules,metal ion affinities,heterolytic bond dissociation energies,chiral recognition and quantification.In this paper the theory of kinetic method is introduced in detail and its applications are enumerated.
kinetic method;cluster ion;tandem mass spectrometry;thermochemistry
O 657.63
A
1004-2997(2012)04-0202-06
2012-04-18
2012-06-04
科技部仪器专项(2011YQ09000507)、中国计量科学研究院业务费(21-JB1251)资助
李 明(1979~),男(汉),吉林人,博士,从事质谱学研究。E-mail:mingutah@hotmail.com
方 向(1963~),男(汉),研究员,主要从事质谱仪器研发工作。E-mail:fangxiang@china.com

