食品中甜蜜素检测方法的改进
周慧敏,赵彤
(国家粮食监督检验中心大连市产品质量监督检验所,辽宁大连 116021)
甜蜜素又名环己基氨基磺酸钠,是一种在我国广泛使用的无营养、甜度高的食品甜味剂。但也有研究表明:人体过量摄入甜蜜素会产生致癌、致畸、损害肾功能等副作用[1-2]。到目前为止,已建立的测定甜蜜素的方法很多,主要有气相色谱法、比色法、薄层层析法[3]、液相色谱-质谱法[4]。在国家抽查中,GB/T 5009.97—2003《食品中环己基氨基磺酸钠的测定》中气相色谱法是最常用的,即利用环己基氨基磺酸钠在酸性条件下与亚硝酸钠反应,以生成的环己醇亚硝酸酯定性和定量。但采用填充柱,峰形不够尖锐,给积分定量造成一定误差;没有净化步骤,样品会污染设备;使用100 mL比色管过大,不适合批量检验;环己醇亚硝酸酯不稳定易分解,影响定量。结合食品中甜蜜素测定方法的相关报道和实际工作经验,采用OV-101毛细管色谱柱代替填充柱,使用正己烷净化样品,按比例减小取样量和试剂使用量,以环己醇亚硝酸酯和环己醇峰面积加和定量,以避免以上问题。
1 材料与方法
1.1 仪器与试剂
1.1.1 仪器
6890N气相色谱仪:安捷伦科技有限公司;OV-101毛细管柱(30 m×0.53 mm×0.5 μm)色谱柱:中国科学院大连化学物理研究所;TB—114电子天平:北京塞多利斯仪器系统有限公司;QN—999多功能食物搅拌机:韩国日进精工有限公司;QL-866涡旋混合器:海门市其林贝尔;CR21G离心机:日本日立公司。
1.1.2 试剂
甜蜜素标准品:上海泉岛公司;甜蜜素标准溶液:2 mg/mL用蒸馏水配制;浓硫酸(优级纯):100 g/L,用蒸馏水配制;亚硝酸钠(分析纯):50 g/L,用蒸馏水配制;正己烷(色谱纯)。
1.2 标准系列制备
分别取 2 mg/mL 甜蜜素标准溶液 2、20、50、100、200 μL于10 mL离心管中加蒸馏水至4 mL,加入50 g/L的亚硝酸钠溶液1 mL、100 g/L的硫酸溶液1 mL,涡旋混合,冰浴中反应30 min后,加入2 mL正己烷提取,涡旋混合1 min,4 000 r/min离心2 min,取上清液供分析用。
1.3 方法
1.3.1 固体样品
试样用粉碎机粉碎。称取已粉碎的样品10 g置于50 mL具塞三角瓶中,加入50 mL蒸馏水,振荡60 min,过滤,取滤液10 mL并加入5 mL正己烷,涡旋混合仪混合2 min,4 000 r/min离心5 min,弃去有机相后,移取4 mL水相,转移到10 mL离心管。向离心管中先后加入50 g/L的亚硝酸钠溶液1 mL、100 g/L的硫酸溶液1 mL,涡旋混合,冰浴中反应30 min后,加入2 mL正己烷提取,涡旋混合1 min,4 000 r/min离心2 min,取上清液供分析用。
1.3.2 液体样品
称取10 g样品置于50 mL容量瓶中,加蒸馏水定容至刻度,摇匀,取10 mL并加入5 mL正己烷,涡旋混合仪混合2 min,4 000 r/min离心5 min,弃去有机相后,移取4 mL水相,转移到10 mL离心管。向离心管中先后加入50 g/L的亚硝酸钠溶液1 mL、100 g/L的硫酸溶液1 mL,涡旋混合,冰浴中反应30 min后,加入2 mL正己烷提取,涡旋混合1 min,4 000 r/min离心2 min,取上清液供分析用。
1.4 色谱条件
色谱柱OV-101毛细管柱(30m×0.53mm×0.5μm),进样口温度160℃,FID检测器温度180℃,柱箱温度80℃保持6min。载气高纯氮气4mL/min,进样量1μL。
1.5 测定
甜蜜素标准溶液图,见图1。

经GC-MS验证,如图1所示峰1为甜蜜素衍生主产物环己醇亚硝酸酯,峰2为甜蜜素衍生副产物环己醇,环己醇亚硝酸酯不稳定随时间推移会分解成环己醇。为了减少环己醇亚硝酸酯分解给定量带来的影响,本方法用环己醇亚硝酸酯和环己醇峰面积加和定量。
2 结果与讨论
2.1 线性范围和检出限
按1.2的方法配制标准序列,以1.4的色谱条件进样见图 1。在 2 μg/mL~200 μg/mL 选定的质量浓度范围内甜蜜素的含量与环己醇亚硝酸酯和环己醇峰面积之和的线性相关系数为0.999 6,见表1。

表1 甜蜜素的保留时间、线性范围、相关系数Table 1 Retention time,Linear rang,correlative coefficients(r)of sodium cyclamate
在系列样品中,将浓度为1.6 μg/mL的标液1 μL进样后,所示得到的峰面积为12 PA*S,由此计算最低检出浓度为4 mg/kg。
2.2 定量峰的选择
国标方法以环己醇亚硝酸酯定量,但环己醇亚硝酸酯不稳定会随时间推移分解成环己醇,影响定量,而且衍生后的样品放置时间过长无法使用。在20℃下,以200 μg/mL标准品为例,其衍生产物随时间变化,见表2。

表2 甜蜜素产物随时间变化Table 2 Derivative varition with tim
由表2知,在40 h内两者峰面积之和是稳定的。因此,本方法选择环己醇亚硝酸酯和环己醇峰面积加和定量,以避免上述问题。
2.3 样品的测定、回收率和精密度试验
2.3.1 空白样品
取一空白糕点样品在0.1、0.5、1.0 g/kg三个水平,每个水平同时做6组平行样,按1.3的方法前处理,进行回收率试验。回收率在93%~104%之间,相对标准偏差(RSD)为2.6%~4.3%,结果见表3。
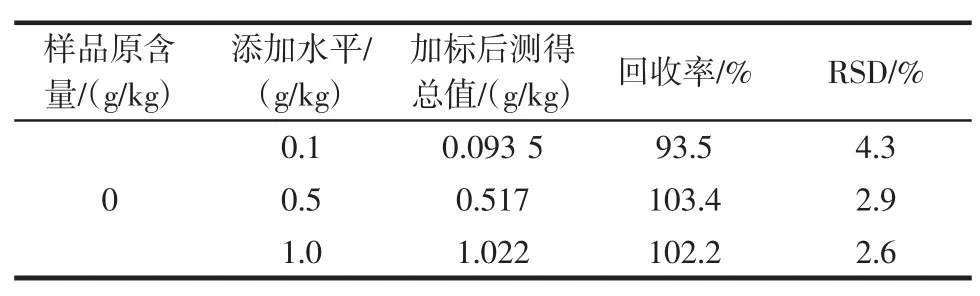
表3 糕点试样加标回收率和精密度(n=6)Table 3 Recoveries and precision of cake samples(n=6)
2.3.2 阳性样品
取一阳性糕点样品在0.5水平,同时做6组平行样,按1.3的方法前处理,进行回收率试验。回收率为93.6%,相对标准偏差(RSD)为4.7%,结果见表4。

表4 糕点试样加标回收率和精密度(n=6)Table 4 Recoveries and precision of cake samples(n=6)
3 结论
本次实验主要是用气相色谱法对实际样品进行检验,结果表明,该方法可准确测定食品中的甜蜜素含量,且有很好的线性关系,相关系数大于0.999 5,最低检出浓度为4 mg/kg,回收率为93%~104%,相对标准偏差(RSD)为2.6%~4.7%。从而确认本方法可准确测定食品中的甜蜜素。
:
[1]Jacks0n C D,Baetcke K P.Causative agents in the induction of bladder cancer[J].Ann Clin Lab Sci,1976,6(3):223-232
[2]Bopp B A,Senders R C,Kesterson J W.Toxicological aspects of cyclamate and cyclohexylamine[J].Crit Rev Toxicol,1986,16(3):213-306
[3]张暖民.GB/T 5007.97-2003《食品中环己基氨基磺酸钠的测定》[S].北京:中国标准出版社:689-693
[4]王明泰.SN/T 1948-2007《进出口食品中环己基氨基磺酸钠的检测方法液相色谱-质谱质谱法》[S].北京:中国标准出版社

