腹腔镜胃肠手术中转开腹的多因素分析
李临海 王昆华 龚昆梅 郭世奎 肖 乐 刘为军
(云南省第一人民医院普外一科 昆明理工大学昆华医院 云南省肠外肠内营养研究中心,昆明 650032)
随着微创技术的发展,腹腔镜手术在胃肠外科的临床应用范围越来越广,绝大多数开腹手术均可在腹腔镜下进行,其中某些手术已表现出独特的优势[1]。随着腹腔镜操作技术不断熟练,腹腔镜胃肠手术的术中、术后并发症逐步减少,与传统开腹手术无明显差异,在手术时间、术中出血等方面甚至优于开腹手术[2],中转开腹率也在不断降低[3]。我院2005年5月~2011年4月共施行腹腔镜下胃肠手术213例,中转开腹 25例,中转率 11.7%(25/213),本文对中转开腹的原因进行多因素分析,报道如下。
1 临床资料与方法
1.1 一般资料
本组213例,男126例,女87例。年龄26~75岁,(61.5 ±11.2)岁。体重 45 ~64 kg,(54.3 ±9.5)kg。胃癌24例,其中胃窦部癌19例,胃体癌5例,肿瘤大小1~5 cm。直肠癌118例,其中直肠上段癌51例,直肠中段癌36例,直肠下段癌31例,肿瘤大小3~6 cm。右半结肠癌22例,其中回盲部癌9例,升结肠癌6例,结肠肝曲癌7例,肿瘤大小3~7 cm。左半结肠癌25例,其中结肠脾曲癌4例,降结肠癌3例,乙状结肠癌18例,肿瘤大小2~8 cm。小肠癌24例,其中空肠癌18例,回肠癌6例,肿瘤大小3~5 cm。
1.2 方法
气管插管全麻,术前准备同常规开腹手术。体位及术者站位视手术部位而定。设定气腹压力12~15 mm Hg(1 mm Hg=0.133 kPa)。脐孔处为观察孔。操作孔视病灶位置而改变,一般3~5个。
1.2.1 腹腔镜胃癌根治术 按胃癌根治性切除的原则行D2根治术,采取与开腹手术相似步骤处理血管及清扫各组淋巴结。腹腔镜下操作结束后,上腹正中行约5 cm辅助切口,完成病灶切除和消化道重建。重建气腹,检查腹腔,放置引流,缝合切口。
1.2.2 腹腔镜直肠癌根治术 腹腔镜直肠癌低位前切除术(Dixon术):从乙状结肠系膜内侧入路进行分离,先处理肠系膜下血管,然后游离乙状结肠系膜和直肠两侧腹膜及腹膜返折,行全直肠系膜切除(TME),镜下切断并闭合肠管,小切口拉出肠管,切除病变,镜下吻合。腹腔镜腹会阴联合直肠切除术(Miles术):游离肠管系膜和血管同上,左中下腹trocar穿刺点术前定位好备造瘘。会阴部手术同开腹手术。
1.2.3 腹腔镜结肠癌根治术(以右半结肠癌为例)采取自下而上、自内而外的操作顺序,以肠系膜上静脉主干为中心,依次游离并切断回结肠动静脉、右结肠动静脉、胃结肠静脉结肠支,游离结肠中动脉右侧支,夹闭切断。离断胃结肠韧带,切开膈结肠韧带及升结肠外侧腹膜至盲肠外侧部,与内侧打开的融合筋膜间隙贯通。辅助小切口进行肿瘤的移除与消化道的重建。
1.2.4 腹腔镜小肠手术 腹腔镜下充分游离小肠后,根据病灶大小做相应辅助切口,将病变小肠段提出腹壁外,做部分小肠肠段切除和吻合。
1.3 观察指标
中转开腹率,术中粘连程度及术中出血情况。术中粘连程度自定义分为轻度(疏松粘连带)、中度(片状粘连)、重度(脏器之间致密粘连)。术中出血自定义分为易控制(3 mm以下的血管出血)、较难控制(3~5 mm血管出血,且位置深在,腹腔镜下不易游离钳夹)、难控制(5 mm以上的血管出血,且位置深在,腹腔镜下难以游离钳夹)。
1.4 统计学处理
用SPSS11.0统计软件进行统计学分析,以术中是否转开腹为应变量,先对7个可能的影响因素进行单因素分析,然后对有统计学意义的影响因素进行多元logistic回归。
2 结果
中转开腹25例,中转开腹率11.7%(25/213),其中胃癌中转3例,结直肠癌中转19例,小肠癌中转3例,见表1。中转开腹原因的单因素分析见表2。
以术中是否转开腹为应变量,最终进入模型的变量为:X3(术中粘连程度)、X4(术中出血情况)、X5(肿瘤分期)和X7(肿瘤分化程度),见表3。4个变量的偏回归系数值(β)均为正(OR值均大于1),表明:术中粘连程度和术中出血是腹腔镜中转开腹的主要因素,术中粘连程度越重、术中出血越难控制越易中转开腹,肿瘤分期、肿瘤分化程度是重要因素。
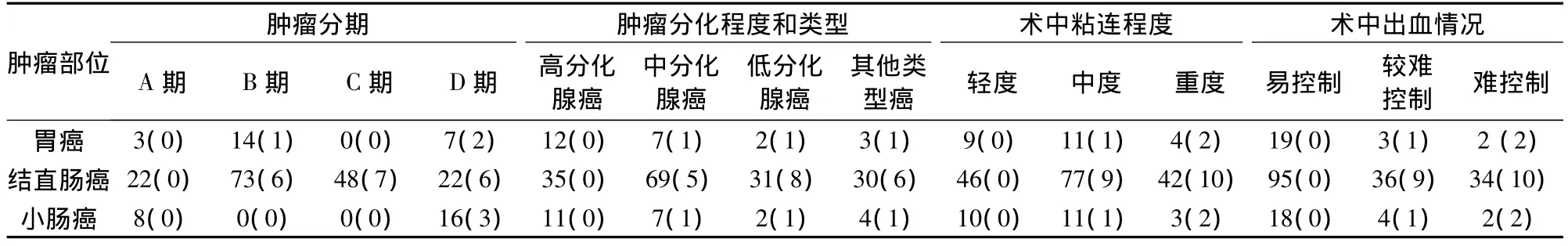
表1 腹腔镜胃肠手术基本情况
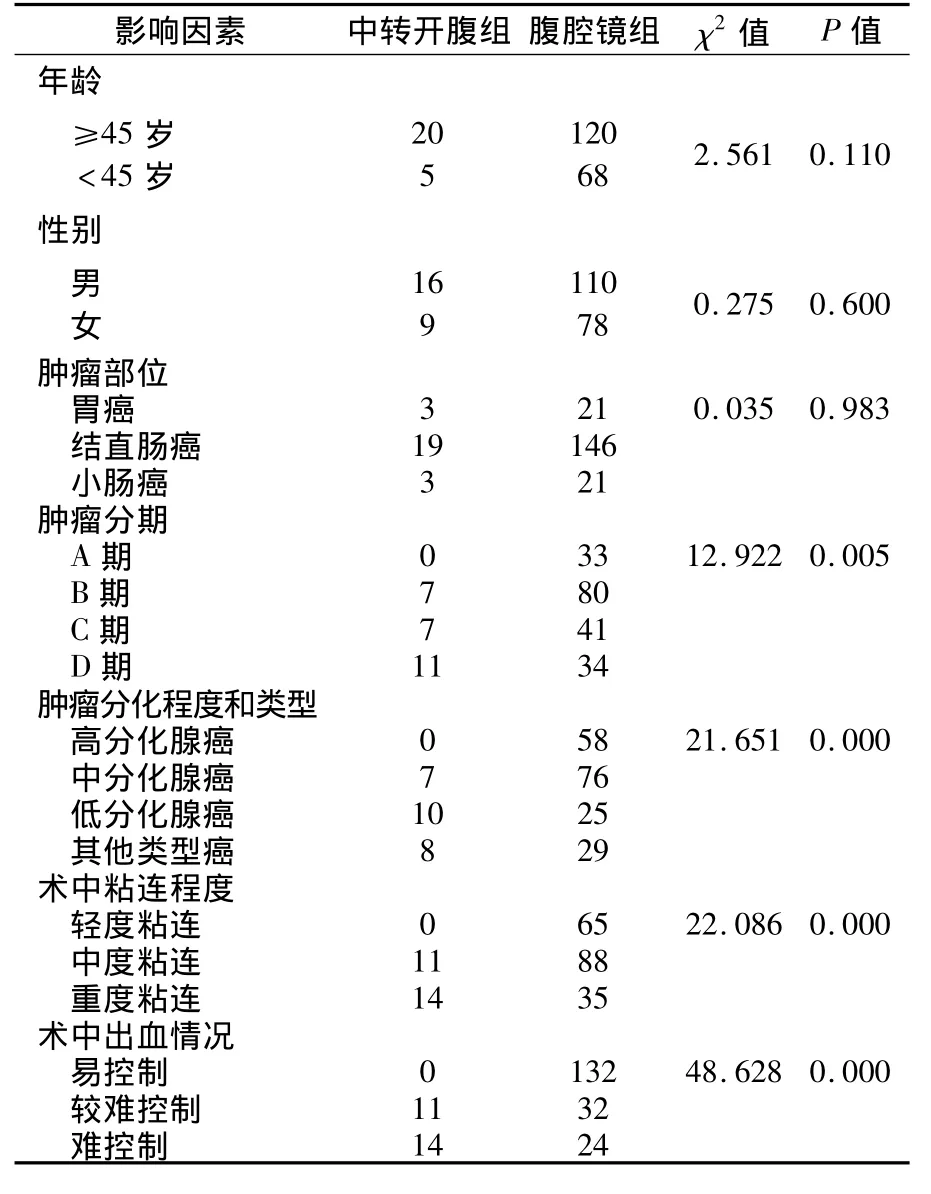
表2 腹腔镜胃肠手术中转开腹原因的单因素分析
3 讨论
腹腔镜手术因其特殊的手术环境以及对设备性能的高度依赖,从一开始就暴露出局限性和独有的潜在危险。在手术环境和设备性能没有得到根本改进之前,腹腔镜手术还不能完全达到开腹手术的境界,术中因病变复杂,术者经验不足及操作技术差异等,须中转开腹手术加以解决,因此,腹腔镜术者对中转开腹所持的态度有非同寻常的意义。李国新等[4]报道1212例腹腔镜结直肠切除术中转开腹138 例,中转开腹率为 11.4%。Nassiopoulos等[5]总结1993年以来650例腹腔镜结直肠切除术中共71例中转开腹,中转开腹率为11%。本研究中转开腹率为11.7%(25/213),与国内外报道相近。
3.1 中转开腹的原因
本组中转开腹25例,按粘连程度,14例重度粘连,11例中度粘连;按术中出血情况,难以控制的出血14例,较难控制的出血11例;按肿瘤分期,A期无中转开腹病例,B期7例,C期7例,D期11例。本研究结果显示术中粘连程度和术中出血情况是腹腔镜中转开腹的主要原因,粘连程度越重、术中出血越难控制,中转开腹率越高;另外,肿瘤分期、肿瘤分化程度也是腹腔镜中转开腹的主要原因;患者年龄、性别及肿瘤部位与中转开腹无关。
中转开腹分为:主动中转开腹和被动中转开腹。主动中转开腹(疾病性原因):①肿瘤分期晚与周围浸润严重、局部解剖不清、清扫困难,如果强行手术,损伤周围脏器或大出血的风险增加,最终导致中转开腹;②术前漏诊和误诊的疾病无法在腔镜下同时处理;③术野广泛粘连,操作空间小;④病人对气腹不耐受导致持续的高碳酸血症无法维持麻醉安全性;⑤一时无法修复的手术器械或设备故障;⑥病人解剖因素,如直肠癌前切除术中,患者骨盆狭小而瘤体相对较大,腔镜下直肠的切断成为手术的难点和中转开腹的主要原因;⑦肥胖病人腔镜视野差,解剖层次不清、结肠系膜肥厚、分离困难。被动中转开腹(技术性原因):①术者的技术水平无法完成本次手术;②出现腔镜无法处理的手术并发症,如无法控制的大出血[6]。本组中转开腹的主要原因为腹腔广泛粘连、术中无法控制的出血及肿瘤与周围组织浸润严重。
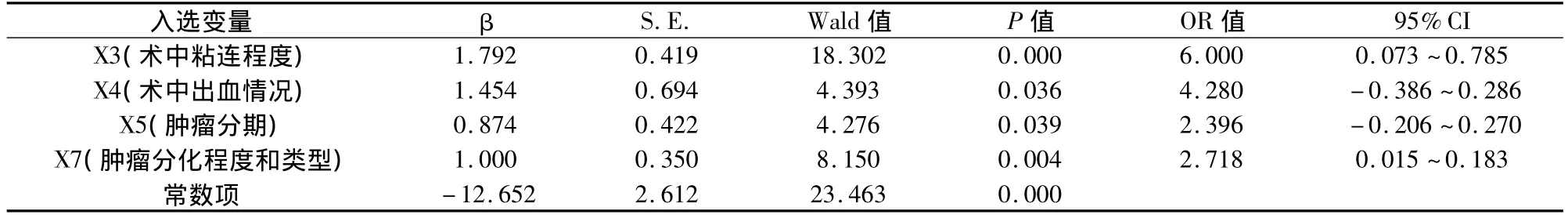
表3 腹腔镜胃肠手术中转开腹原因的logistic回归分析
3.2 中转开腹的意义
腹腔镜手术的微创优势显而易见,但局限性也十分突出,主要表现有:①电视显示屏上的二维术野取代了开腹熟悉的腹腔内三维真实术野;②术者无法用手对预处理病灶做触诊、牵引、压迫、分离,导致“触觉丧失”效应;③手术可操作空间的绝对性狭小和手术动作轴向的相对性受限;④腹腔镜专用的长柄器械比传统器械显得笨拙。腹腔镜外科的这些缺陷在处理复杂或紧急情况时愈加凸显。因此,腹腔镜手术必须要以开腹手术为坚强后盾。根据术中的具体情况及术者技术水平,在发生严重手术并发症之前及时决定中转开腹,以获得最好的疗效。
3.3 如何降低中转开腹手术率
中转开腹率的高低虽然受很多环节制约,但在排除那些影响不大因素(如气腹不耐受、设备故障)之后,决定性的因素只有2个,术者的经验和对适应证的控制。
3.3.1 适应证的控制 Gibson等[7]报道腹腔镜手术最初中转开腹率曾高达64%,此后以每年5%的速度下降。Chen等[8]对9年的腹腔镜结直肠手术进行回顾性分析认为,学习曲线大约为25例左右,经历该曲线后,中转开腹率明显下降。我们认为,术者应该在客观评价自己腹腔镜技术水平的基础上,选择合适病例,处于学习曲线不同时期的术者,所选病例应该有很大的不同。虽然腹腔粘连、肥胖和肿瘤位置、大小等并不是腹腔镜直肠癌根治术的绝对禁忌证,但开展之初应避免选择直肠肿瘤直径过大(>5 cm),肿瘤伴梗阻,肿瘤侵袭周围邻近器官及腹腔镜技术受限的腹腔广泛粘连、心肺功能差,不能耐受气腹,凝血功能障碍等情况,以减少中转开腹率。选择A期肿瘤、既往无腹部手术史的病例能最大限度地提高腹腔镜手术的成功率。
3.3.2 操作者的技巧及经验 对每位正在或准备开展腹腔镜手术的医师,要重视和加强腹腔镜技术基本功的训练,不断积累经验。我们有以下2点初步经验:①重视血管的处理,特别是静脉的解剖,避免因出血而造成视野不清。在解剖血管时,牵拉组织要轻柔、张力适当,不要大块离断组织。腹腔镜胃癌根治术特别需要注意胃网膜右静脉的处理,因其位于幽门下、胰腺上,容易撕裂出血。女性腹腔镜直肠癌低位前切除术中需要注意直肠与阴道后穹隆、后壁的解剖间隙,避免损伤阴道血管。腹腔镜右半结肠癌根治术中,肠系膜上静脉主干解剖要在静脉鞘内沿其走行方向进行,特别注意静脉分支的变异,游离组织时,超声刀的工作面不要接触静脉血管壁。②腹腔镜直肠癌低位前切除术中,最好适当游离部分降结肠系膜,以避免吻合口张力过大。吻合完毕后常规经肛门分别注入空气及亚甲蓝液,检查有无吻合口漏,若发现吻合口渗漏,可行腹腔镜下缝合修补及经肛门修补。本组2例注气试验阴性,但发现有亚甲蓝液渗漏,经修补后满意未中转开腹。
总之,腹腔镜胃肠手术中转开腹的原因众多,严格选择适应证,规范手术操作和充分的围手术期处理,并根据术中具体情况及术者的实际水平,决定中转开腹时机,是降低中转率、减少并发症发生的重要措施。
1 王哲近,周振旭,朱恒梁,等.腹腔镜全直肠系膜切除联合经肛内括约肌切除保肛术治疗超低位直肠癌.中国微创外科杂志,2011,11(2):135-138.
2 Kim YW,Baik YH,Yun YH,et a1.Improved quality of life outcomes after laparoscopic-assisted distal gastrectomy for early gastric cancer:results of a prospective randomized clinical tria1.Ann Surg,2008,248(5):721 -727.
3 崔 明,李子禹,邢加迪,等.腹腔镜与开腹胃癌根治术D2淋巴结清扫的比较研究.中国微创外科杂志,2010,10(5):395-398.
4 李国新,闫鸿涛,余 江,等.腹腔镜结直肠手术中转开腹原因分析.中国实用外科杂志,2006,26(11):881 -882.
5 Nassiopoulos K,Pavlidis TE,Menenakos E,et al.Laparoscopic colectomy in the management of large,sessile,transformed colorectal polyps.JSLS,2005,9(1):58 -62.
6 钟克力,潘 凯,夏利刚,等.腹腔镜直肠癌根治手术病例选择策略.中国内镜杂志,2008,14(3):240 -242.
7 Gibson M,Byrd C,Pierce C,et al.Laparoscopic colon resection:A five year retrospective review.Am Surg,2000,66(3):245 -248.
8 Chen W,Sailhamer E,Berger DL,et al.Operative time is a poor surrogate for the learning curve in laparoscopic colorectal surgery.Surg Endosc,2007,21(2):238 -243.

