纳米Ni/Fe双金属催化降解盐酸环丙沙星的研究
梁 斌,莫海筹,黎宏玉,沈玉翠,萧洁韵,方战强
(华南师范大学化学与环境学院,广东广州510006)
环丙沙星(Ciprofloxacin,CPFX)属第三代喹诺酮类抗生素.临床主要用于敏感菌所致的呼吸道、泌尿道、消化道、皮肤软组织等感染,具有安全性高,价格低廉等优点[1-3].抗生素生产废水中含有大量生物抑制性物质,属于高浓度、难降解有机废水.目前,对抗生素废水的处理方法主要有物化处理技术、生化处理技术及其它联合处理技术等[4].这些技术对于高生物毒性的抗生素废水的处理效果并不理想.
纳米材料具有极强的吸附能力、还原能力、防腐抗菌功能为环境污染治理提供了新技术[5-6].纳米零价铁(NZVI)因具有尺寸小、比表面积大、内在活性高和有效减少有毒副产物产生等优点,广泛用于有机和无机污染物的降解研究[5],但暴露在空气中极易被氧化[7],容易发生团聚现象,降低反应活性.采用双金属修饰是对纳米零价铁颗粒表面进行修饰改性,是一种有效的方法[8].本文制备Ni/Fe纳米双金属,以盐酸环丙沙星作为目标污染物,研究其降解性能,为抗生素废水处理提供新材料.
1 实验部分
1.1 试剂与仪器
试剂:盐酸环丙沙星(99%)(BIO BASIC INC);无水乙醇、FeSO4·7H2O、NaBH4和 NiCl2·6H2O 均为分析纯,产地均为天津市大茂化学试剂厂;甲醇(HPLC)(天津市科密欧化学试剂有限公司);甲酸(HPLC)(Sigma-Aldrich);乙腈(HPLC)(CNW Technologies GmbH);实验用水均为去离子水.
仪器:高效液相色谱仪(Shimadzu,LC10A HPLC);恒温摇床(Fuhe SHZ-82);数显pH计(上海精密科学仪器有限公司PHS-29A);ASAP2020M比表面分析仪(Micromeritics Instrument,USA);透射电镜(TEM)(H-3000,Hitachi,Japan);X-射线衍射仪(XRD)(Y-2000,Dirgc,China);火焰原子吸收光谱仪(TAS-986,Pgeneral,China).
1.2 纳米Ni/Fe双金属的制备
100 mL 0.1 mol/L的 FeSO4·7H2O乙醇溶液(水/乙醇为 7/3)中加入适量聚乙烯吡咯烷酮(PVPK-30)(WPVPK-30/W铁=1/1),搅拌使之形成溶液 A;配制 50 mL 0.03 mol/L的硼氢化钠(NaBH4)乙醇溶液B;在搅拌状态下,迅速将B溶液倒入A溶液中,搅拌5 min,用磁选法选出纳米零价铁,分别去离子水和乙醇洗涤3次.
将新制的纳米零价铁加入到含50mL的乙醇溶液的锥形瓶中,加入由适量NiCl2·6H2O配制的乙醇溶液50 mL,振荡30 min,让Ni沉积到铁表面;将所制得的纳米双金属Ni/Fe用磁选法选出,按照纳米铁的洗涤方法洗净.
1.3 纳米Ni/Fe双金属的表征
采用低温氮吸附比表面分析仪ASAP2020M(Micromeritics Instrument,USA)测定纳米 Ni/Fe双金属颗粒的BET比表面积.纳米Ni/Fe双金属的颗粒粒径与形貌由透射电镜(TEM)(H-3000,Hitachi,Japan)进行表征.将纳米Ni/Fe双金属浸没在无水乙醇中,经过超声波分散后滴在铜网上制成电镜试样,乙醇挥发后,将样品放进真空箱.X-射线衍射仪(XRD)(Y-2000,Dirgc,China)测定纳米Ni/Fe双金属颗粒的晶相.采用铜Kα辐射,电压为40 kV,电流为120 mA.纳米Ni/Fe双金属颗粒中铁和镍各自的含量使用火焰原子吸收光谱仪(TAS-986,Pgeneral,China)测定.
1.4 纳米Ni/Fe催化降解盐酸环丙沙星实验
配制150 mL一定质量浓度的盐酸环丙沙星溶液,用0.1mol/L NaoH 溶液和0.1 mol/L HCl溶液调pH.加入一定质量的纳米Ni/Fe双金属,盖上瓶盖,避光,放入25℃的恒温摇床里,250 r/min反应.间隔一定时间取样,经过0.45μm滤膜后HPLC分析.
1.5 盐酸环丙沙星质量浓度的分析方法
采用高效液相色谱仪(Shimadzu,LC10A HPLC)测定.检测条件:色谱柱:Kromasil 100-5C18(250 mm ×4.6 mm,5 μm),流动相为体积分数0.1%甲酸溶液 -乙腈(80∶20,体积比)体系,柱温:30 ℃,流速:0.7 mL/min,检测波长:277 nm,进样量为20μL,每个样品平行测定3次.
2 结果与讨论
2.1 纳米Ni/Fe双金属的表征
BET分析结果显示,纳米Ni/Fe双金属颗粒的比表面积为68 m2/g,纳米零价铁颗粒比表面积为35 m2/g,说明Ni的负载使纳米零价铁的分散性提高,比表面积增大.合成纳米颗粒的直径均少于100 nm,纳米零价铁颗粒的平均直径约在30~50 nm,纳米Ni/Fe双金属颗粒的平均直径约在10~20 nm(图1).
图2为纳米零价铁和纳米Ni/Fe双金属的XRD表征图,图中44.9°处的峰属α-Fe衍射峰,说明合成的纳米零价铁是以非晶相形式存在的,合成的纳米Ni/Fe双金属也为非晶态合金结构[9].
经原子吸收光谱仪(TAS-986,Pgeneral,China)测定得,合成纳米双金属颗粒中Ni/Fe(m/m)为15.8.
2.2 纳米Ni/Fe投加量对降解效果的影响

图1 纳米零价铁(A)和纳米Ni/Fe双金属(B)的TEM透射电镜图Figure 1 TEM of nanoscale Fe(A)and nanoscale Ni/Fe(B)
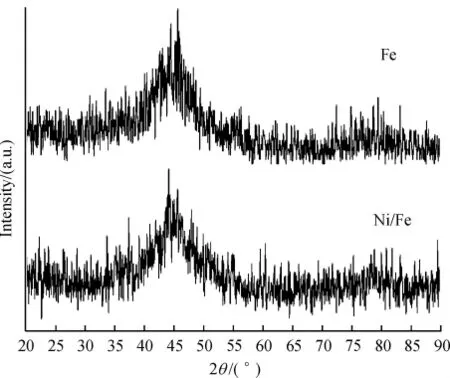
图2 合成纳米Fe0与纳米Ni/Fe双金属颗粒的XRD谱图Figure 2 XRD of nanoscale Fe and nanoscale Ni/Fe
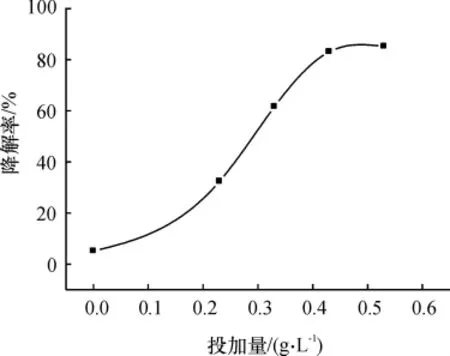
图3 纳米Ni/Fe投加量对盐酸环丙沙星降解的影响Figure 3 Effect of nanoscale Ni/Fe dosage on degradation of CPFX
在 pH=7,[CPFX]0=30 mg/L,t=100 min,避光,摇床温度为25℃,摇速为250 r/min的条件下,通过改变纳米Ni/Fe的投加量,观察盐酸环丙沙星降解率的变化情况.图3表明,随着纳米双金属投加量的增加,盐酸环丙沙星的去除率逐渐提高.当投加量少于0.43 g/L时,增加纳米双金属的投加量在相同反应时间内降解率较大提高.当纳米双金属在一定的投加量范围增加,单位反应体积内反应活性位点增多,使其与盐酸环丙沙星分子发生有效碰撞的几率增大,从而提高降解反应速率[9-10].当投加量超过0.43 g/L时,投加量的增加对去除率的影响不明显,投加量从0.43 g/L增加到0.53 g/L时,两者降解率只相差2.1%.可能是当纳米双金属过量时,反应容器底部有大量纳米双金属的沉积,使其参加反应的有效质量和比表面积减少,反应活性降低,进而使反应速率降低.
2.3 盐酸环丙沙星的初始质量浓度对降解效果的影响
在 pH=7,纳米 Ni/Fe投加量为0.43 g/L,其它条件不变,通过改变CPFX的质量浓度,观察其降解率的变化情况.结果表明,当初始质量浓度小于30 mg/L时,盐酸环丙沙星的降解率随初始质量浓度的升高而增大(图4),在30 mg/L之后,降解率曲线渐趋平缓.纳米Ni/Fe对盐酸环丙沙星的降解属于非均相反应,包括环丙沙星吸附到Ni/Fe表面过程和随后的表面反应过程.反应中过量的纳米Ni/Fe(0.43 g/L)能提供足够的表面活性位,当环丙沙星为10~30 mg/L时,随着其质量浓度的升高,更充分地利用了纳米Ni/Fe的表面活性位,使其在100 min内的降解率从76%提高到83%.质量浓度继续升高,使纳米Ni/Fe的表面活性位被完全利用,甚至环丙沙星分子之间也产生了竞争吸附,导致降解率上升的速率迅速减慢,趋于平缓.综合各种因素,最佳反应初始质量浓度为30 mg/L.

图4 初始浓度对盐酸环丙沙星降解的影响Figure 4 Effect of initial concentration on degradation of CPFX
2.4 初始pH对催化降解反应的影响
在[CPFX]0=30 mg/L,纳米 Ni/Fe投加量为0.43 g/L,其它条件不变条件下,通过改变反应初始pH,观察降解率的变化情况(图5).
盐酸环丙沙星在弱酸性和中性溶液中降解率较高,其中 pH 5.16(原液),降解率为 78.6%;pH 7.0时,降解率最高,在强酸性溶液中次之(pH 3.0,η=56.1%),在强碱性溶液中降解率最低.在弱酸性介质中,溶液中的H+使纳米双金属表面基本上没有被铁的氧化物覆盖,污染物(溶液中的盐酸环丙沙星分子)能直接与纳米Ni/Fe颗粒接触,还原反应所需电子直接来源于纳米Fe0,从而使反应速率更快,降解率更高[10].较低的 pH加快了铁的腐蚀,导致Fe的质量浓度迅速降低,缩小了纳米Ni/Fe的比表面积,从而降低了其对环丙沙星的吸附效果,使降解率降低[11].反应的最佳初始pH为7.

图5 反应初始pH对盐酸环丙沙星降解的影响Figure 5 Effect of initial pH on degradation of CPFX
2.5 反应时间对催化降解反应的影响
相同的反应条件下,在0~50 min内,盐酸环丙沙星的降解率随着反应时间的增加而增加,反应60 min后,降解率达到最大值,然后趋于稳定(图6).反应刚开始时,新制备纳米Ni/Fe的表面反应活性位较多,反应速率快,降解率上升快.在反应过程中,纳米Ni/Fe中Fe0的浓度减少,反应活性随之降低,降解反应达到最大限度.故反应最佳时间为60 min.

图6 盐酸环丙沙星在不同时间下的降解率Figure 6 Degradation rate of CPFX at different time
2.6 纳米Ni/Fe催化降解盐酸环丙沙星的动力学分析
纳米Ni/Fe双金属对盐酸环丙沙星的降解过程属于非均相反应过程.对于非均相反应过程,主要分为以下几个步骤:(1)溶液中的盐酸环丙沙星分子向纳米Ni/Fe双金属表面扩散;(2)扩散到纳米Ni/Fe双金属表面的盐酸环丙沙星分子被纳米双金属吸附;(3)被吸附的盐酸环丙沙星分子在纳米Ni/Fe双金属表面发生反应;(4)被吸附的产物分子从纳米双金属表面脱附;(5)脱附了的产物分子通过内、外扩散作用进入溶液[7,12].
反应在恒温振荡的作用下进行,故较低浓度的盐酸环丙沙星吸附到纳米Ni/Fe双金属表面的速率、产物分子从纳米双金属表面脱附的速率都很快,因此可认为吸附作用和脱附作用都不是主要速率控制步骤,发生在纳米Ni/Fe双金属表面的催化降解反应是主要的速率控制步骤[7,12].
对于表面反应为速率控制步骤的非均相催化反应,通常用Langmuir-Hinshelwood模型进行描述,反应速率公式如下:

式(1)中,b和k都是常数,C是反应物的浓度.
式(1)可简化为表观一级反应动力学,表示如下:

式(2)中,kobs为表观反应速率常数.
利用式(2)作图(图7),ln(Ct/C0)与时间t的线性相关性一般(R2=0.771 61).因为反应速率比较快,取样时间点不恰当,但也可以近似认为纳米Ni/Fe对盐酸环丙沙星的催化降解反应符合表观一级反应动力学规律,表观速率常数为0.022 0 min-1.

图7 纳米Ni/Fe催化降解CPFX的反应动力学曲线Figure 7 Kinetic curves of catalytic degradation of CPFX by nanoscale Ni/Fe

在投加量为 0.43 g/L、[CPFX]0=30 mg/L、反应初始pH为7、反应时间为60 min的条件下,纳米Ni/Fe双金属>纳米零价铁>商业铁粉对CPFX的降解效果见表1.其中,由于比表面积:纳米Ni/Fe(68 m2/g)>纳米零价铁(35 m2/g),故纳米Ni/Fe的反应活性要比纳米零价铁的高,其降解率也高于纳米零价铁;由于普通Fe0不属于纳米级颗粒,故其表面效应可以忽略,反应活性较低,故其对CPFX的降解率也远远低于纳米Ni/Fe和纳米零价铁.

表1 纳米Ni/Fe双金属、纳米Fe0、商业铁粉对CPFX的去除率比较Table 1 Comparison of CPFX removal rates by nanoscale Ni/Fe,nanoscle Fe0 and Fe0
3 结论
采用液相还原法制备了纳米Ni/Fe双金属,其颗粒直径为10~20 nm,比表面积为68 m2/g,并以盐酸环丙沙星作为目标污染物,研究了各种因素对降解效果的影响,初步探讨了降解反应的动力学机理,对比了纳米Ni/Fe、纳米Fe0和普通Fe0对盐酸环丙沙星的降解效果,结果表明:
(1)纳米Ni/Fe投加量、盐酸环丙沙星的初始质量浓度、反应pH和反应时间对水中盐酸环丙沙星的去除效果有着不同的影响.最佳降解工艺条件为盐酸环丙沙星的初始质量浓度30 mg/L,纳米Ni/Fe质量浓度0.43 g/L,反应初始 pH为7,反应60 min,降解效率达 83.3%.
(2)纳米Ni/Fe对盐酸环丙沙星的催化降解反应符合表观一级反应动力学规律.表观速率常数为0.022 0 min-1.
(3)在投加量为0.43 g/L、[CPFX]0=30 mg/L、反应初始pH为7、反应时间为60min的条件下,降解效果:纳米Ni/Fe双金属>纳米零价铁>商业铁粉.
[1]林殷.水环境中典型抗生素的残留水平及其分布[D].广州:中山大学,2008.
[2]王万峰.喹诺酮类物质的定量结构-效应关系及水环境中遗传毒性物质的行为研究[D].河南新乡:河南师范大学,2007.
[3]朱健.盐酸左氧氟沙星对水稻、玉米、小麦生长及生理特性的影响[D].贵阳:贵州师范大学,2009.
[4]巩有奎,张林生.抗生素废水处理研究进展[J].工业水处理,2005,25(12):1-4.
[5]郭延辉.纳米零价铁对染料废水的脱色性能研究[D].河南新乡:河南师范大学,2009.
[6]林海英.纳米零价铁的制备以及在环境有机污染物去除方面的应用研究[D].河南新乡:河南师范大学,2009.
[7]陆敏.纳米Ni/Fe双金属对水中芳香族硝基化合物的降解研究[D].江苏镇江:江苏科技大学,2007.
[8]邱心泓,方战强.修饰型纳米零价铁降解有机卤化物的研究[J].化学进展,2010,22(2/3):291-297.
[9]ZHANGWeihua,QUAN Xie,ZHANG Zhuoyong.Catalytic reductive dechlorination of p-chlorophenol in water using Ni/Fe nanoscale particles[J].J Environ Sci:China,2007,19:362-366.
[10]符彩娟.纳米Fe0处理含染料废水的研究[D].北京:北京工业大学,2008.
[11]张卫华.纳米Ni/Fe及超声辅助纳米Ni/Fe对水中氯代有机物脱氯研究[D].长春:东北师范大学,2008.
[12]ALOK D,RAJEEV CC,CHANDRASHEKHAR V R,et al.Iron-nickel bimetallic nanoparticles for reductive degradation of azo dye Orange G in aqueous soluion[J].Appl Catal B:Environ,2008,79:270-278.

