固相萃取-高效液相色谱法测定紫杉醇脂质纳米粒体外释放度
姚瑶,周卫,丁逸梅(1.南京工业大学药学院,南京10009;.江苏省药物研究所,南京10009)
紫杉醇是从红豆杉属植物红豆杉中提取的一种天然抗肿瘤药物,临床上主要用于卵巢癌、乳腺癌和非小细胞肺癌的治疗。紫杉醇的水溶性极低,目前临床使用的紫杉醇制剂以聚氧乙烯蓖麻油(Cremphor EL)-无水乙醇(1∶1,V/V)为助溶剂。Cremophor EL会引起组胺释放,产生严重的过敏反应[1,2],并且会诱导输液用聚氯乙烯袋中的邻苯二甲酸酯二-(2-乙基己基)(DEHP)泄漏[3~5]。因此,解决紫杉醇水溶性问题在该药上市后引起了广泛关注。
脂质纳米粒作为抗癌药物载体可以提高药物的治疗指数,降低或减少药物的不良反应[6]。对于脂质纳米粒来说,体外释放度是非常重要的评价指标,相应的测定方法成为研究的重点。本研究制备了紫杉醇脂质纳米粒,并参考相关文献,以固相萃取-高效液相色谱(SPE-HPLC)法对其体外释放度进行考察。
1 仪器与试药
HPLC仪,包括2010 HT检测器、LC-Solution色谱工作站(日本岛津公司);透析袋(截留分子量12 000~14 000,南京都英生物科技有限公司);SEP-PAK®C18固相萃取柱(美国Waters公司);BS 21S电子分析天平(德国Sartorius公司);ZRS-8G智能溶出仪(天津天大天发科技有限公司)。
紫杉醇原料药(桂林晖昂生化药业有限公司,批号:JF 20091001);紫杉醇对照品(中国食品药品检定研究院,批号:100382-200301);注射用蛋黄磷脂(上海太伟药业有限公司,批号:1032482);胆固醇(中国医药集团化学试剂有限公司);维生素E(德国Basf有限公司);蔗糖(国药集团化学试剂有限公司);水杨酸钠(上海凌峰化学试剂有限公司);甲醇、无水乙醇(色谱纯,山东禹王实业有限公司);其他试剂均为分析纯。
2 方法与结果
2.1 紫杉醇脂质纳米粒的制备
采用薄膜分散-高压均质法制备脂质纳米粒。称取处方量的紫杉醇、注射用蛋黄磷脂、胆固醇和维生素E,溶解于适量无水乙醇后倒入茄形瓶,将茄形瓶置于旋转蒸发仪上减压蒸干,除去乙醇成均匀薄膜;加入5%蔗糖水溶液水化一定时间后,90 000 kPa高压循环4次得到均匀半透明乳液。0.22 μm微孔滤膜过滤后分装到西林瓶内,冷冻干燥,即得样品。
2.2 紫杉醇脂质纳米粒体外释放度测定方法的建立
2.2.1 释放介质 水杨酸钠可作为紫杉醇体外释放的增溶质[7,8],本文采用水杨酸钠(1 mol·L-1)-PBS(pH 7.4)作为释放介质。
2.2.2 色谱条件 色谱柱:Phenomenex luna C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(80∶20);流速:1.0 mL·min-1;柱温:40 ℃;检测波长:227 nm;进样量:20 μL。
2.2.3 对照品溶液的制备 精密称取紫杉醇对照品约10 mg,置10 mL量瓶中,加流动相溶解稀释至刻度,摇匀,作为对照品贮备液。精密吸取此贮备液1.0 mL,置于10 mL量瓶中,加流动相稀释,定容,摇匀,即得。
2.2.4 空白纳米粒溶液的制备 按处方量称取各辅料制备空白脂质纳米粒。取空白纳米粒约100 mg,精密称定,置于10 mL容量瓶中,加流动相溶解稀释至刻度,作为空白纳米粒溶液。
2.2.5 供试品溶液的制备 精密移取体外释放待处理样品1 mL,加入经活化过的C18固相萃取柱(用5 mL甲醇和5 mL水分别过柱2次),用10 mL蒸馏水冲洗,流速为0.2 mL·s-1,再以5 mL甲醇洗脱,速度为0.1 mL·s-1,收集甲醇滤过液,用氮气吹干,用流动相1 mL溶解,即得。
2.2.6 专属性试验 取释放介质、对照品溶液和空白纳米粒溶液,按“2.2.5”项下方法处理后,在上述色谱条件下分别进样20 μL,记录色谱图。结果,在此色谱条件下,紫杉醇能与释放介质较好的分离,且峰形良好,保留时间适中,辅料和释放介质对主药测定无干扰。色谱见图1。
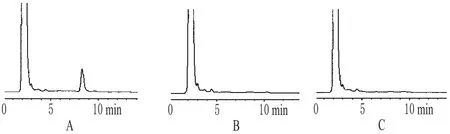
图1 高效液相色谱图A.紫杉醇对照品;B.释放介质;C.空白辅料Fig 1 HPLC chromatogramsA.paclitaxel control;B.release medium;C.blank sample
2.2.7 线性关系考察 取紫杉醇对照品适量,精密称定,加流动相溶解并定量稀释成1.0 mg·mL-1的对照品溶液。分别精密量取对照品溶液0.2、0.4、0.8、1.0、1.2 mL,置10 mL量瓶中,用流动相稀释至刻度,摇匀,进样20 μL,记录色谱图。以紫杉醇的峰面积积分值(A)为纵坐标,检测浓度(c)为横坐标,进行线性回归,得回归方程为A=2.165×104+4.248×104c(r=0.999 3,n=6)。结果表明,紫杉醇检测浓度在2~12 μg·mL-1范围内与峰面积积分值呈良好线性关系。紫杉醇的定量限为0.05 μg·mL-1(S/N=10)。
2.2.8 萃取回收率试验 分别精密量取0.2、1.0、1.2 mL紫杉醇对照品贮备液于10 mL量瓶,用释放介质稀释至刻度,摇匀,得到低、中、高3种不同浓度的溶液,分别取1 mL,置于预先活化好的C18固相萃取柱上,按“2.2.5”项下方法操作,进样20 μL,测定紫杉醇含量,计算萃取回收率。结果,紫杉醇低、中、高3种浓度的回收率分别为96.9%、97.2%、95.7%;RSD分别为1.33%、0.79%、1.46%(n均为3),表明本方法回收率良好。
2.2.9 稳定性试验 分别考察对照品溶液、样品和供试品溶液的稳定性 对照品溶液的稳定性:精密量取1.0 mL紫杉醇对照品贮备液于10 mL量瓶中,用释放介质稀释至刻度,得到10 μg·mL-1的溶液,置于37 ℃水浴保温。分别于0、12、24 h,取1 mL溶液用预先活化好的C18固相萃取柱萃取,按“2.2.5”项下方法处理,进样测定。结果,RSD=0.35%(n=3),表明紫杉醇对照品在37℃的释放介质中24 h内稳定。样品的稳定性:取样品1瓶,加水5 mL,充分振摇,水化5 min后,得到纳米粒混悬液(约2 mg·mL-1),精密吸取此混悬液0.1 mL,置10 mL量瓶中,以释放介质稀释定容,37℃水浴保温。分别于0、12、24 h,取1 mL纳米粒混悬液用预先活化好的C18固相萃取柱萃取,按“2.2.5”项下方法处理,进样测定。结果,RSD=0.21%(n=3),表明样品在37℃释放介质中24 h内稳定。供试品溶液的稳定性:精密量取0.1 mL紫杉醇纳米混悬液于10 mL量瓶中,用释放介质稀释至刻度。取1 mL该溶液以预先活化好的C18固相萃取柱萃取,按“2.2.5”项下方法处理,所得供试品溶液置于自动进样器中,分别于0、12、24 h进样测定。结果,RSD=0.29%(n=3),表明供试品在萃取后24 h内稳定。
2.3 体外释放度的考察
2.3.1 体外释放的方法及释放度测定 采用总体液平衡反向透析法,按照2010年版《中国药典》(二部)项下方法[9]。以200 mL水杨酸钠(1 mol·L-1)-PBS(pH 7.4)为释放介质,将装有2 mL空白释放介质的大小形状相同的透析袋,完全浸入释放介质中平衡2 h,精密吸取用蒸馏水复溶的紫杉醇脂质纳米粒混悬液0.9 mL(相当于紫杉醇约1.8 mg),直接加入到释放介质中,在100 r·min-1和(37±0.5)℃介质温度下进行体外释放试验。分别于0.5、1.0、2.0、3.0、4.0、8.0、12.0、24.0 h从中取出一个透析袋,同时向透析袋外液中补充2 mL的空白释放介质,用SPE-HPLC法分别测定各个取样点透析袋内液中的药物浓度;另取脂质纳米粒混悬液0.1 mL,置10 mL量瓶中,加甲醇定容,摇匀后以HPLC法直接测定总药量。平行操作3份样品,计算累积释放百分率(Q)。同法测定紫杉醇原料药的体外释放度,计算24 h内的Q值,以Q对时间(t)作图,得到体外释放曲线,详见图2。
由图2可知,紫杉醇原料药4 h释放即达到98.84%,表明透析袋对紫杉醇无吸附;而载药的脂质纳米粒在0.5 h之内有突释现象,释放量为30.85%,这可能是未被包封的游离药物和以弱的结合力吸附在纳米粒表面的药物的快速解吸附;在随后的9.5 h内,紫杉醇的释放量随着释放时间的延长而增加;12 h后释放达到平台期,释放量随时间的变化不明显;24 h累积释放104.9%。
2.3.2 释放曲线的拟合 根据2010年版《中国药典》(二部)项下方法[9],分别用零级动力学、一级动力学、Higuchi方程对脂质纳米粒的体外释放数据进行拟合,得到纳米粒体外释药的动力学方程。结果,紫杉醇脂质纳米粒的体外释放符合一级动力学方程。紫杉醇脂质纳米粒体外释放拟合方程见表1。

图2 紫杉醇脂质纳米粒体外释放曲线(n=3)Fig 2 In vitro release profile of Paclitaxel lipid nanoparticles(n=3)

表1 紫杉醇脂质纳米粒体外释放拟合方程Tab 1 Fitted drug release kinetic equation of Paclitaxel lipid nanoparticles in vitro
3 讨论
固相萃取柱是利用固体吸附剂将样品中的目标化合物吸附,使目标化合物与干扰物分离,再用洗脱液洗脱达到分离和富集的目的。笔者选取和液相色谱柱同样填料的固相萃取柱(C18),采用甲醇作为洗脱液进行试验。结果表明,选择5 mL甲醇洗脱可以有效的将待测组分洗脱分离,紫杉醇的回收率达到预期值。
释放度测定时,对加入增溶物如表面活性剂和电解质有一定的要求,不提倡向释放介质中加入醇类溶剂。紫杉醇为难溶药物,在常用的pH 6.8 PBS、pH7.4 PBS等介质中均难溶解。笔者曾尝试以PBS(pH 7.4)-吐温80(0.5%)作为释放介质,结果紫杉醇释放较为缓慢,且体外释放度结果的测定对吐温80的纯度要求很高,否则易产生噪声大、基线不稳、柱压升高、柱效降低等情况。笔者选择水杨酸钠(1 mol·L-1)-PBS(pH 7.4)为体外释放介质,紫杉醇在1 mol·L-1水杨酸钠中的溶解度为28.1 μg·mL-1[8],因而将药物最终释放的浓度定为9 μg·mL-1,以满足漏槽条件。
传统的脂质纳米粒的体外释放研究方法主要为透析法[10]。此方法下纳米粒与透析袋内少量的释放介质接触,药物从纳米粒中扩散至袋内释放介质后,再通过透析袋扩散至大量释放介质中。由于透析袋内外的药物浓度梯度较小,药物的被动扩散进行得较慢,使得释药速率显著偏小。试验中以透析法测得紫杉醇体外释放度24 h仅达到约15%。本文采用总体液平衡反向透析法测定紫杉醇纳米粒的体外释放,由于纳米粒直接与释放介质接触并被大量稀释,故能更好地模拟药物静脉注射后到达体内的状态。
试验发现,透析袋对紫杉醇并无明显阻滞作用,紫杉醇溶液在4 h基本透过透析袋,且透膜速率明显快于纳米粒的释放速率;紫杉醇脂质纳米粒释放均最优拟合为一级释放模型。
由于体外释放的条件与体内血液环境并不相同,因此体外释放的测定结果并不能完全真实反映该脂质体在体内的释放情况,故紫杉醇脂质纳米粒给药系统的体内吸收与体外释放的相关性还有待进一步研究。
[1]Loprevitr M,Roberto EF,Alessandra DC,et al.Interaction between novel anticancer and radia-ton inno-small cell lung cancer cell lines[J].Lung Cancer,2001,33(1):27.
[2]van Zuylen L,Verweij J,Sparreboom A.Role of formulation vehicles in taxane pharmacology[J].Invest New Drugs,2001,19(2):125.
[3]Kim SC,Yoon HJ,Lee JW,et al.Investigation of the release behavior of DEHP from infusion sets by paclitaxel-loaded polymeric micelles[J].Int J Pharm,2005,293(1-2):303.
[4]Donyai P,Sewell GJ.Physicaland chemical stability of paclitaxel infusions in different container types[J].J Oncol Pharm Pract,2006,12(4):211.
[5]张恩娟,陈 琳,曹 健.紫杉醇注射液配套输液器中邻苯二甲酸二辛酯的溶出性考察[J].中国药房,2008,19(9):698.
[6]Sagar RM,Amol BD,Sachin P,et al.Nanoparticles:emerging carriers for drug delivery[J].Saudi Pharmaceutical Journal,2011,19(3):129.
[7]Huh KM,Min HS,Lee SC,et al.A new hydrotropic block copolymermicelle system for aqueous solubilization of paclitaxel[J].J Control Release,2008,126(2):122.
[8]Cho YW,Lee J,Lee SC,et al.Hydrotropic agents for study of invitro paclitaxel release from polymeric micelles[J].J Control Release,2004,97(2):249.
[9]国家药典委员会.中华人民共和国药典(二部)[S].2010年版.北京:中国医药科技出版社,2010:附录85、附录201.
[10]林巧平,郭仁平,王青松,等.注射多西他赛脂质体的制备、体外释放及细胞毒作用[J].中国药科大学学报,2008,39(5):4 171.

