熊胆粉微生物限度检查方法学验证
杨务彬 李元宏 兰 鸿
湖北医药学院附属太和医院药学部,湖北 十堰 442000
熊胆粉为熊科动物黑熊Selenaretos thibetanus Cuvier经胆囊手术引流胆汁而得的干燥品,收载于国家药品标准《新药转正标准》第11册[1],本品有一定的抑菌作用[2],但其微生物限度检查一直采用常规方法检验,根据《中国药典》2010年版的要求,对原用的常规方法进行验证[3]。
1 仪器与试药
1.1 仪器
LDZX-40BI立式自动电热压力蒸气灭菌器(上海申安医疗器械厂),DNP-9162型电热恒温培养箱(上海精宏实验设备有限公司),HH B11 600型电热恒温培养箱(上海跃进医疗器械厂),LRH-150B生化培养箱(广东医疗器械厂),超净台(苏净集团安泰公司)。
1.2 培养基
营养肉汤培养基,改良马丁培养基,营养琼脂培养基,玫瑰红钠琼脂培养基,胆盐乳糖培养基,甘露醇氯化钠琼脂培养基,溴化十六烷基三甲铵琼脂培养基,曙红亚甲蓝琼脂培养基(EMB),四硫磺酸钠亮绿培养基(TTB),胆盐硫乳琼脂培养基(DHL),均购自中国药品生物制品检定所。
1.3 阳性对照菌
金黄色葡萄球菌[CMCC(B)26003],大肠埃希菌[CMCC(B)44102],枯草芽孢杆菌[CMCC(B)63501],铜绿假单胞菌[CMCC(B)10104],乙型副伤寒沙门菌[CMCC(B)50094],白色念珠菌[CMCC(F)98001],黑曲霉菌[CMCC(F)98003],均购自四川省食品药品检验所。
1.4 供试品
熊胆粉(购自四川省新鹿药业有限公司,批号:091203、091204、091205)。
2 方法与结果
2.1 供试液的制备
2.1.1 供试液制备方法1
取供试品10 g,加pH 7.0无菌氯化钠-蛋白胨缓冲液至100 mL,混匀,作为 1∶10 供试液。
2.1.2 供试液制备方法2
取1∶10供试液25 mL加pH 7.0的无菌氯化钠-蛋白胨缓冲液至50 mL,混匀,作为1∶20供试液。
2.2 阳性对照菌液的制备
将大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌的新鲜培养物接种于营养肉汤培养基中,30~35℃培养18 h,用0.9%无菌氯化钠溶液10倍递增稀释制成每1 mL中含菌数为50~100 cfu的菌悬液,备用;接种白色念珠菌的新鲜培养物于改良马丁琼脂培养基中,25℃培养24 h,用0.9%无菌氯化钠溶液10倍递增稀释制成每1 mL中含菌数为50~100 cfu的菌悬液,备用;接种黑曲霉的新鲜培养物于改良马丁琼脂斜面培养基上,25℃培养5 d,加入5 mL含0.05%聚山梨酯80的0.9%无菌氯化钠溶液将孢子洗脱,吸出孢子悬液至无菌试管内,用含0.05%聚山梨酯80的0.9%无菌氯化钠溶液10倍递增稀释制成每1 mL含孢子数50~100 cfu的孢子悬液,备用。
2.3 检查方法验证[4]
2.3.1 试验组
2.3.1.1 常规法 分别取1∶10供试液1 mL和试验菌株的菌悬液 1 mL(50~100 cfu)入平皿中,立即倾注琼脂培养基,待凝固后,置规定温度培养,观察并计数。
2.3.1.2 培养基稀释法1 分别取1∶10供试液0.2、0.1 mL(0.2、0.1 mL/皿)和试验菌株的菌悬液 1 mL(50~100 cfu)入平皿中,立即倾注琼脂培养基,待凝固后,置规定温度培养,观察并计数。
2.3.1.3 培养基稀释法2 分别取1∶20供试液0.1 mL(0.1 mL/皿)和试验菌株的菌悬液 1 mL(50~100 cfu)入平皿中,立即倾注琼脂培养基,待凝固后,置规定温度培养,观察并计数。
2.3.2 菌液组
分别取1 mL试验菌株(50~100 cfu)入平皿中,立即倾注琼脂培养基混匀,待凝固后,置规定温度培养,观察并计数,每种菌各制备2个皿。
2.3.3 供试液本底测定
2.3.3.1 常规法 分别取1∶10供试液1 mL入平皿中,立即倾注琼脂培养基,待凝固后,置规定温度培养,观察并计数。
2.3.3.2 培养基稀释法1 分别取1∶10供试液0.2、0.1 mL入平皿中,立即倾注琼脂培养基,待凝固后,置规定温度培养,观察并计数。
2.3.3.3 培养基稀释法2 分别取1∶20供试液0.1 mL入平皿中,立即倾注琼脂培养基,待凝固后,置规定温度培养,观察并计数。
2.4 回收率测定
2.4.1 常规法测定
常规法测定回收率,白色念珠菌、黑曲霉菌、大肠埃希菌回收率均高于70%,可采用常规法进行霉菌、酵母菌计数;金黄色葡萄球菌、枯草芽孢杆菌回收率低于70%,说明本品对枯草芽孢杆菌和金黄色葡萄球菌有较强的抑菌作用,细菌检查不能采用常规法。见表1。
2.4.2 培养基稀释法测定
2.4.2.1 培养基稀释法(1∶10供试液,0.2 mL/皿)测定回收率 大肠埃希菌、金黄色葡萄球菌回收率高于70%,枯草芽孢杆菌回收率低于70%;采用培养基稀释法(1∶10供试液,0.2 mL/皿)不可消除本品对枯草芽孢杆菌的抑菌作用。见表1。
2.4.2.2 培养基稀释法(1∶10供试液,0.1 mL/皿)测定回收率 枯草芽孢杆菌回收率低于70%;采用培养基稀释法(用1∶10供试液,0.1 mL/皿)不可消除本品对枯草芽孢杆菌的抑菌作用。
2.4.2.3 培养基稀释法(1∶20供试液,0.1 mL/皿)测定回收率 大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌3次独立试验回收率均高于70%;采用培养基稀释法(1∶20供试液,0.1 mL/皿)可消除本品对枯草芽孢杆菌的抑菌作用。见表1。
2.5 控制菌检查法验证[5-6]
2.5.1 大肠埃希菌检查法
分别取1∶10供试液10 mL,加入3瓶100 mL胆盐乳糖培养基中,其中一瓶加入1 mL大肠埃希菌菌液(50~100个/mL)作为试验组,一瓶加入1mL金黄色葡萄球菌菌液(50~100个/mL)作为阴性菌对照组;另取1瓶100 mL胆盐乳糖培养基,加入1 mL大肠埃希菌菌液(50~100个/mL)作为大肠埃希菌阳性对照组。按大肠埃希菌检查法检验,结果见表2。
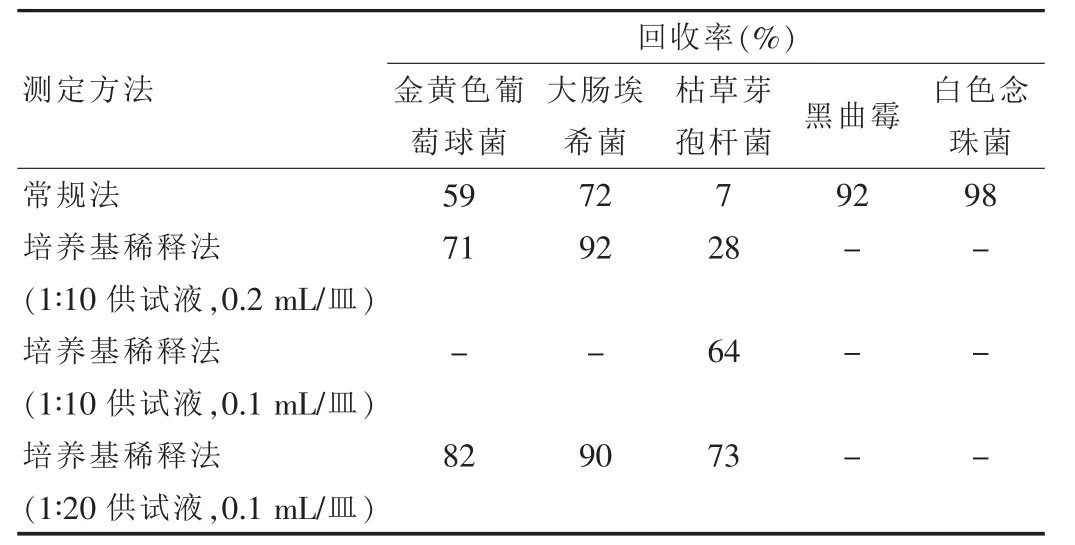
表1 消除供试品抑菌活性回收率试验

表2 大肠埃希菌检查结果
由表2可知,阴性菌对照组未检出大肠埃希菌,试验组检出大肠埃希菌。可采用常规法进行本品的大肠埃希菌检查。
2.5.2 金黄色葡萄球菌检查法
分别取 1∶10供试液 10 mL,加入 3瓶 100 mL营养肉汤培养基中,其中一瓶加入1 mL金黄色葡萄球菌菌液(50~100个/mL)作为试验组,一瓶加入1 mL大肠埃希菌菌液(50~100个/mL)作为阴性菌对照组;另取100 mL营养肉汤培养基,加入1 mL金黄色葡萄球菌菌液(50~100个/mL)作为金黄色葡萄球菌阳性对照组。按金黄色葡萄球菌检查法检验,结果见表3。

表3 金黄色葡萄球菌检查结果
由表3可知,阴性菌对照组未检出金黄色葡萄球菌,试验组检出金黄色葡萄球菌。可采用常规法进行本品的金黄色葡萄球菌检查。
2.5.3 铜绿假单胞菌检查法
分别取 1∶10供试液 10 mL,加入 3瓶 100 mL胆盐乳糖培养基中,其中一瓶加入1 mL铜绿假单胞菌菌液(50~100个/mL)作为试验组,一瓶加入1 mL大肠埃希菌菌液(50~100个/mL)作为阴性菌对照组;另取一瓶100 mL胆盐乳糖培养基,加入1 mL铜绿假单胞菌菌液(50~100个/mL)作为铜绿假单胞菌阳性对照组。按铜绿假单胞菌检查法检验,结果见表4。
由表4可知,阴性菌对照组未检出铜绿假单胞菌,试验组检出铜绿假单胞菌。可采用常规法进行本品的铜绿假单胞菌检查。
2.5.4 大肠菌群检查法
分别取1∶10供试液1 mL,加入3管10 mL胆盐乳糖发酵管中,其中一管加入1 mL大肠埃希菌菌液(50~100个/mL)作为试验组,一管加入1 mL金黄色葡萄球菌菌液(50~100个/mL)作为阴性菌对照组;另取1管10 mL胆盐乳糖发酵管,加入1 mL大肠埃希菌菌液(50~100个/mL)作为大肠菌群阳性对照组。按大肠菌群检查法检验,结果见表5。

表4 铜绿假单胞菌检查结果
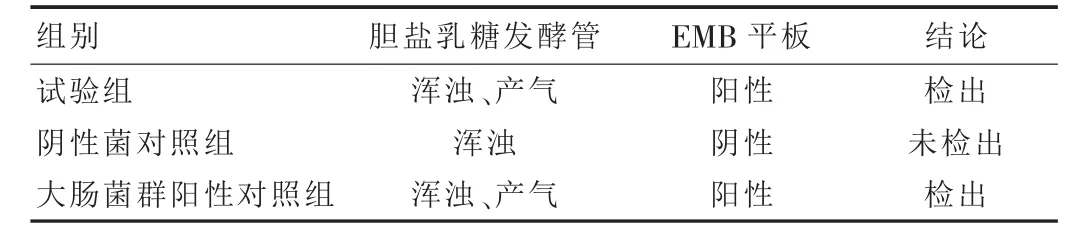
表5 大肠菌群检查结果
由表5可知,阴性菌对照组未检出大肠菌群,试验组检出大肠菌群。可采用常规法进行本品的大肠菌群检查。
2.5.5 沙门菌检查法
分别取本品10 g,加入3瓶200 mL营养肉汤中,其中一瓶加入1 mL沙门菌菌液(50~100个/mL)作为试验组,一瓶加入1 mL金黄色葡萄球菌菌液(50~100个/mL)作为阴性菌对照组;另取1瓶200 mL营养肉汤,加入1 mL沙门菌菌液(50~100个/mL)作为沙门菌阳性对照组,按沙门菌检查法检查。结果提示,阴性菌对照组未检出沙门菌,试验组未检出沙门菌,但沙门菌阳性对照组检出沙门菌,故不能采用常规法进行本品的沙门菌检查。所以沙门菌检查法调整为:分别取本品10 g,加入3瓶400 mL营养肉汤中,其中一瓶加入1 mL沙门菌菌液(50~100个/mL)作为试验组,一瓶加入1 mL金黄色葡萄球菌菌液(50~100个/mL)作为阴性菌对照组;另取1瓶400 mL营养肉汤,加入1 mL沙门菌菌液(50~100个/mL)作为沙门菌阳性对照组。按沙门菌检查法检验,结果见表6。

表6 沙门菌检查结果
由表6可知,阴性对照组未检出沙门菌,试验组检出沙门菌。可采用培养基稀释法进行本品的沙门菌检查。
3 讨论
本品按《中国药典》2010年版一部(附录ⅩⅢC)微生物限度检查法进行方法验证,结果表明,用pH 7.0无菌氯化钠蛋白胨缓冲液制备样品,可采用培养基稀释法(1∶20供试液,0.1 mL/皿)进行细菌计数;采用培养基稀释法(400 mL营养肉汤)进行沙门菌检查;采用1∶10供试液的常规法进行霉菌及酵母菌计数和其他控制菌检查。笔者曾采用薄膜过滤法进行试验,但因供试品无法滤过,故选用培养基稀释法。
[1]国家药典委会.国家药品标准《新药转正标准》[M].11册.中国医药科技出版社,2011:43.
[2]徐愚聪,王野.熊胆粉的研究进展[J].华西药学杂志,2000,15(3):200-202.
[3]国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:附录 79.
[4]颜栋林,李萍,兰茜.柴黄片微生物限度检查法方法验证[J].中国当代医药,2009,16(16):7.
[5]权明吉,金仁顺,朴龙,等.熊胆粉对二甲基亚硝胺诱发大鼠肝纤维化的抑制作用[J].世界华人消化杂志,2005,13(20):88.
[6]国家药典委员会.中国药典[S].一部.北京:化学工业出版社,2005:附录71.

