定量化评价中药对帕金森病睡眠障碍疗效的研究*
吴春岚 潘卫东 李国研 刘 云 孙 燕 郭 伸
上海中医药大学附属曙光医院神经内科(上海200021)
帕金森病(Parkinson’s disease,PD)是一中常见的中老年神经系统变性疾病,主要临床表现为静止性震颤、运动迟缓、肌强直、姿势步态异常等。近年来,随着对PD患者非运动症状研究的逐步深入,PD相关的睡眠障碍日益受到各界关注,但仍缺乏有效治疗措施。目前国内外对PD睡眠障碍疗效评价多采用PD睡眠量表(PDSS量表)[1]但是该量表采用问卷形式,受评价者主观判断和经验以及患者理解、表述等人为因素影响较大。本研究通过便携式加速度记录仪对患者睡眠疗效进行评价,并与PDSS量表评价结果比较,判断使用加速度记录仪定量化评价PD睡眠疗效的敏感性与特异性,对客观定量化评价帕金森病睡眠障碍进行尝试性研究。
临床资料 76例早中期PD患者来自2009年12月~2011年4月间上海中医药大学附属曙光医院神经内科门诊及住院患者。按照1∶1原则随机分组,其中治疗组37例,对照组39例,除7例脱落(治疗组3例,对照组4例)外,其余病例均进入疗效结果分析。两组患者在性别、年龄、病程、疾病严重程度、药物使用剂量和加速度记录仪初始评价参数方面比较,无统计学差异(P>0.05),具有可比性,见表1。
表1 治疗组与对照组治疗前一般情况比较(±s)
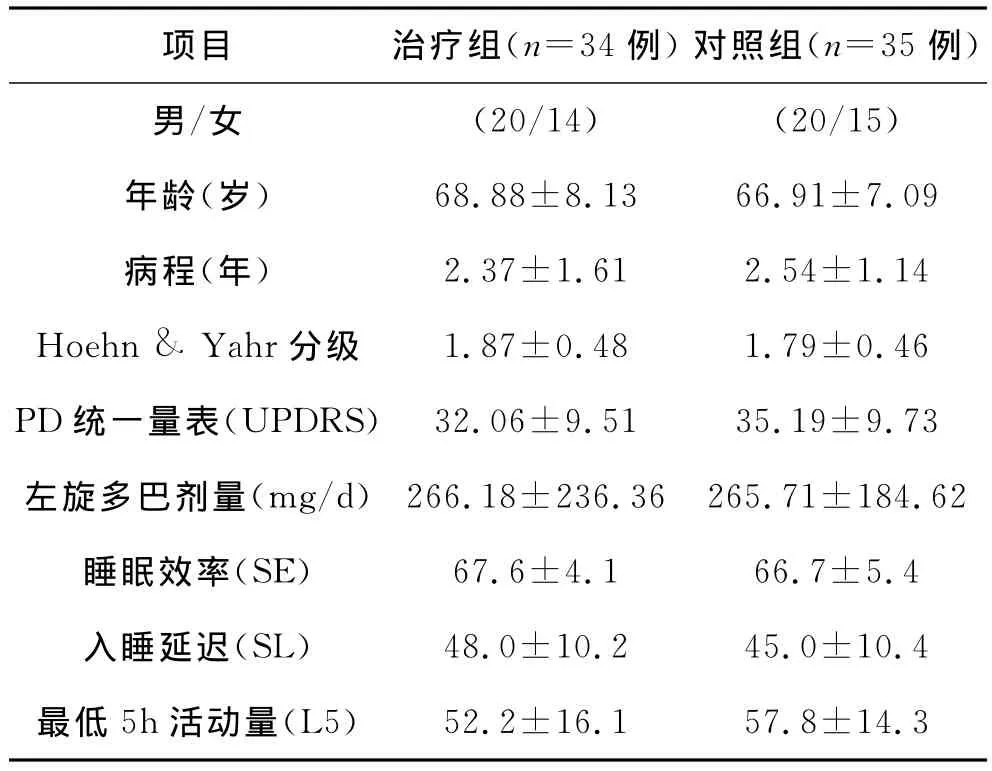
表1 治疗组与对照组治疗前一般情况比较(±s)
项目 治疗组(n=34例)对照组(n=35例)男/女 (20/14) (20/15)52.2±16.1 57.8±14.3年龄(岁) 68.88±8.13 66.91±7.09病程(年) 2.37±1.61 2.54±1.14 Hoehn & Yahr分级 1.87±0.48 1.79±0.46 PD统一量表(UPDRS) 32.06±9.51 35.19±9.73左旋多巴剂量(mg/d) 266.18±236.36 265.71±184.62睡眠效率(SE) 67.6±4.1 66.7±5.4入睡延迟(SL) 48.0±10.2 45.0±10.4最低5h活动量(L5)
纳入标准 符合①原发性帕金森病[2]及其睡眠障碍诊断[3];②修订 Hoehn & Yahr评级I-III级[4];③年龄55~80岁;④未曾服用镇静安眠药物(包括:西药、中成药及中草药)。
排除或剔除标准 ①不符合纳入标准者;②有严重的心、肝、肾内分泌和代谢障碍疾患、造血系统疾患、恶性肿瘤等;③认知损害、痴呆等,或伴有严重精神疾患,无法描述症状者;④近3个月内或入组后曾服用镇静安眠药物(包括:西药、中成药及中草药)或参加其它临床试验者;⑤曾服用多巴胺受体激动剂患者。
治疗方法 入选病例均参照国际“帕金森病治疗指南”[5]给予除多巴胺受体激动剂以外的PD西药开放性治疗,对照组仅使用西药开放治疗,治疗组在此基础上加服安神止颤方(酸枣仁、夜交藤各30g,白芍、郁金、景天三七各15g,天麻、钩藤、姜黄、石菖蒲各10g,远志、甘草各6g),连续服用6周。
疗效标准 帕金森病睡眠量表(PDSS):帕金森病睡眠量表(PDSS)主要针对PD患者总体睡眠质量、失眠、睡眠中断、运动症状、恶梦、幻觉等15个问题,分别涉及该病的发生率、临床特点及相关影响因素,较为全面地评价PD患者所特有的睡眠障碍,其重复性良好,有较强的可信度和灵敏性[6]。所有患者在服药前以及服药6周后由相同医生进行评价。
加速度记录仪睡眠参数解析[7,8]:采用手表型、内镶嵌有微型电脑的记录仪(Ruputer Pro,Seiko Instruments,Chiba,Japan)的运动监视器 ECOLOG(ECOlogical neurobehavior LOGger)量化记录身体活动。该设备的商品化制品为Actigraph Mini-Motionlogger(Ambulatory Monitors Inc.,Ardsley,NY),已经被频繁应用于研究身体运动[2-4,7];在本研究中,设定应用记录仪的ZCM模式第13型Mini-Motionlogger[信号滤过范围2~3Hz,敏感阈值(sensitive threshold):高;获得率(gain):低]。根据 AMI Mini-Motionlogger的设计13模式能够过滤其他频率范围活动,而主要记录2~3Hz内的活动。患者在服药前1周以及服药6周后在非利手侧连续佩戴加速度记录仪1周。数据最后通过特定的连接软件输入电脑进行解析。
①睡眠效率 (sleep efficiency,SE)[7,8]利 用 Action-W,Version2(Ambulatory monitors Inc.,Ardsley,NY)软件检测患者入睡状态下的活动阈值,依据身体活动量粗略计算患者入睡时间,并计算夜间睡眠状态下的时间占熄灯后卧床时间的百分比(睡眠时间/卧床时间×100%);②入睡延迟时间(sleep latency,SL)[7,8]与 计 算 SE 方法 相 同,利 用 Action-W,Version2(Ambulatory monitors Inc.,Ardsley,NY)软件检测患者从熄灯到入睡状态所需要时间(分钟/夜);③最低5h活动量(the least active 5-h,L5)[7,8]计算患者1d中每小时的平均活动量,取其中活动量最小的5h作为最低5h活动量。
相关性研究:将患者治疗前后PDSS总评分的改善率(公式1)分别与睡眠延迟时间、睡眠效率以及最低5h活动量的改善率(公式1)进行相关性分析。

统计学方法 采用SPSS17.0软件进行统计处理,所有统计值均采用双侧检验,P≤0.05即其差异有统计学意义。各次访视的计量资料将采用±SE进行统计描述,治疗前后差异变化采用Wilcoxon秩和检验进行,PDSS与加速度记录仪解析参数改善率之间的相关性比较采用Spearman相关分析。
治疗前后PD睡眠量表(PDSS)变化情况 见表2。
表2 治疗前后PDSS评分比较±s)
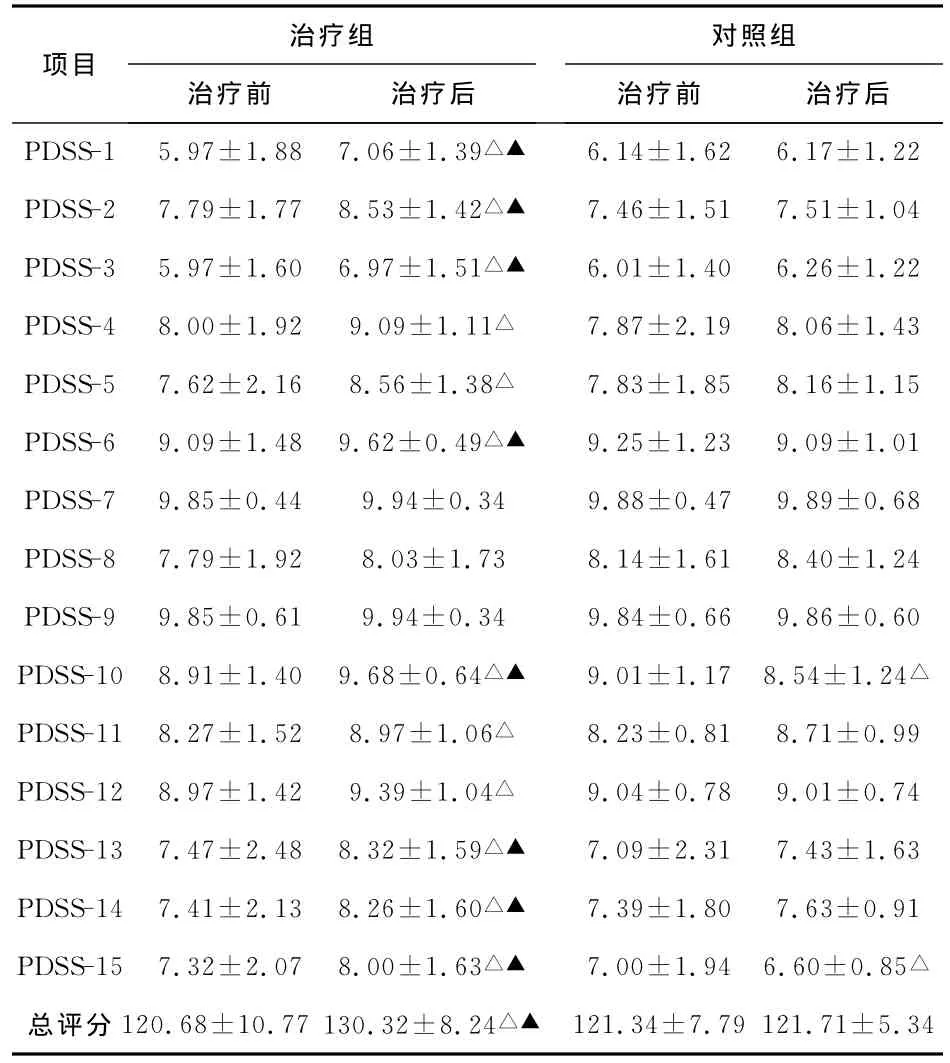
表2 治疗前后PDSS评分比较±s)
注:与治疗前比较,△P<0.05;与对照组比较,▲P<0.05
治疗组 对照组项目6.14±1.62 6.17±1.22 PDSS-2 7.79±1.77 8.53±1.42△▲ 7.46±1.51 7.51±1.04 PDSS-3 5.97±1.60 6.97±1.51△▲ 6.01±1.40 6.26±1.22 PDSS-4 8.00±1.92 9.09±1.11△ 7.87±2.19 8.06±1.43 PDSS-5 7.62±2.16 8.56±1.38△ 7.83±1.85 8.16±1.15 PDSS-6 9.09±1.48 9.62±0.49△▲ 9.25±1.23 9.09±1.01 PDSS-7 9.85±0.44 9.94±0.34 9.88±0.47 9.89±0.68 PDSS-8 7.79±1.92 8.03±1.73 8.14±1.61 8.40±1.24 PDSS-9 9.85±0.61 9.94±0.34 9.84±0.66 9.86±0.60 PDSS-10 8.91±1.40 9.68±0.64△▲ 9.01±1.17 8.54±1.24△PDSS-11 8.27±1.52 8.97±1.06△ 8.23±0.81 8.71±0.99 PDSS-12 8.97±1.42 9.39±1.04△ 9.04±0.78 9.01±0.74 PDSS-13 7.47±2.48 8.32±1.59△▲ 7.09±2.31 7.43±1.63 PDSS-14 7.41±2.13 8.26±1.60△▲ 7.39±1.80 7.63±0.91 PDSS-15 7.32±2.07 8.00±1.63△▲ 7.00±1.94 6.60±0.85△总评分120.68±10.77 130.32±8.24△▲治疗前 治疗后PDSS-1 5.97±1.88 7.06±1.39△▲治疗前 治疗后121.34±7.79 121.71±5.34
6周治疗后,治疗组除 PDSS-7、PDSS-8、PDSS-9项外,其余各项评分及PDSS总分均较前有明显改善(P<0.05),与对照组比较,其中部分评分存在统计学差异(P<0.05);而对照组PDSS-10及PDSS-15项则较前恶化(P<0.05),与对照组比较,其中部分评分存在统计学差异(P<0.05),(见表2)。
治疗前后加速度记录仪参数解析 见表3。
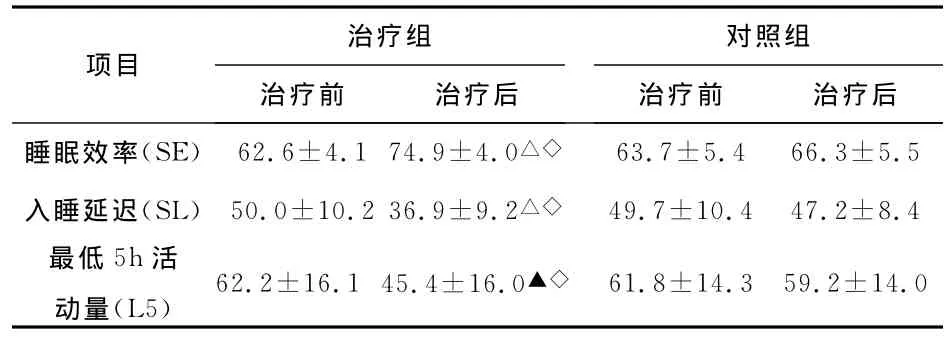
表3 治疗前后加速度记录仪参数比较
6周治疗后,SE、SL和L5均较前有明显改善(P<0.05或P<0.01),与对照组比较,各项均具有显著差异(P<0.05),(见表3)。
PDSS总评分与加速度记录仪睡眠参数的相关性治疗后PDSS总分的改善率与解析加速度记录仪所得的参数SE、SL以及L5的改善率具有较高的相关性(图2),相关系数r分别为:0.696,0.728以及0.793(P<0.05)。
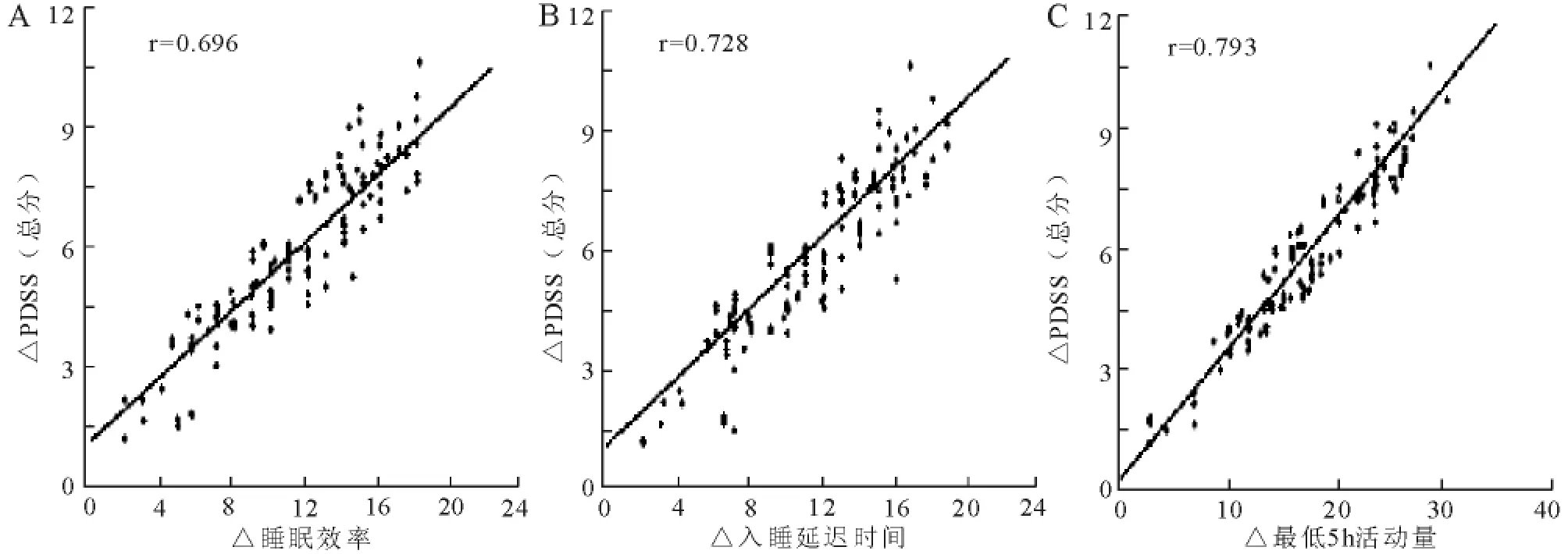
图1 治疗组患者的PDSS改善率与加速度记录仪所得参数的改善率的相关性
讨 论 研究表明,在PD患病早期就可能存在睡眠障碍问题,其发生率高达67%~98%[9],严重影响患者的生活质量。目前对于PD疾病的治疗,仍以补充外源性多巴胺为主。有学者报道[10-12]:多巴胺能替代药物和多巴胺受体激动剂可通过对黑质纹状体区多巴胺通路的作用,影响患者睡眠觉醒周期,且随着病程和药物使用剂量的增长,使用种类的增多,睡眠障碍日趋严重。如多巴胺受体激动剂的使用易诱发PD患者白天嗜睡、睡眠发作等现象;大剂量使用多巴胺能药物会引发睡眠破裂,延长睡眠潜伏期等睡眠障碍表现。中医药在PD治疗中虽然处于非主导地位,但是近年来临床及中药药理研究均证实其确实存在起作用的物质基础[13~15],在帕金森病治疗中能起到延缓疾病进程,改善帕金森病症状,减少并发症,减少美多巴药物剂量等减毒增效的作用。此外,潘卫东等结合加速度记录仪评价观察中药改善帕金森病非运动症状,尤其是PD睡眠障碍疗效显著[8,16]。在此基础上,本研究根据中医“辨证论治”理论,以“滋补肝肾,熄风平颤,安神定志”为治则,运用加速度记录仪评价中医药对于帕金森病睡眠障碍的疗效。
PDSS量表结果显示,治疗组对PD睡眠障碍的总体疗效明显优于对照组,同时结合各单项改善情况进一步分析发现:夜间总体睡眠质量 (PDSS-1)、入睡时间 (PDSS-2)、睡眠维持时间 (PDSS-3)、精神状 况(PDSS-6)、夜 间运动症状 (PDSS-10)、震 颤 (PDSS 13)、醒后精神恢复状况(PDSS-14)及白天过度嗜睡(PDSS-15)等改善情况亦明显优于对照组,证实安神止颤方不仅在整体睡眠质量,包括:入睡困难,睡眠维持、夜间精神状况和肢体运动症状方面疗效显著,同时可在一定程度上有助患者精神恢复,改善白天嗜睡症状,从整体上改善患者睡眠障碍症状,体现中医治疗本病的优势。
结合加速度记录仪睡眠参数分析,我们发现安神止颤方能显著提高睡眠效率,缩短入睡延迟时间,减少最低5h活动量,其对睡眠质量评价的结果基本与PDSS评分相一致,且治疗后PDSS总分的改善率与睡眠效率(SE)、睡眠延迟时间(SL)以及最低5h活动量(L5)的改善率均存在较高的相关性(相关系数r分别为:0.696,0.728以及0.793)。首先,SE与SL能够反映患者总体睡眠质量和入睡延迟时间,与PDSS量表中的睡眠质量 (PDSS-1)、入睡时间 (PDSS-2)、睡眠维持时间 (PDSS-3)等项目临床意义相同,且两者间存在较高的相关性,可用于替代PDSS量表中相关项的评价。其次,L5能够反映患者夜间活动量情况,与睡眠量表中运动症状与震颤相关项及PDSS总分意义相近,且与PDSS总分之间存在较高相关性。因此,我们考虑是否可结合加速度记录仪所得睡眠参数来补充PDSS量表对PD睡眠质量进行评估的不足,提高帕金森病睡眠障碍评价的客观性。
加速度记录仪通过客观性数值对患者睡眠情况进行定量化描述,其在睡眠质量客观评价方面具有较高的可信性,可以避免PDSS量表评价睡眠状况时主观因素干扰,使评价结果更为客观,体现加速度记录仪睡眠参数在PD睡眠障碍评价方法上的优势,因此加速度记录仪睡眠参数可作为适用于临床的睡眠质量评价的新方法,补充目前对睡眠障碍评价时常用量表客观性不足的缺陷。
与客观评价睡眠障碍的多导睡眠仪相比,因其类似手表形式便于佩戴在患者非利手侧,对患者日常生活无明显影响,故而不会人为加重睡眠障碍,便于使用。其次,该仪表记录时间根据需要,可连续记录一周以上,取每日参数均值,较客观真实地记录患者一定时期内的总体睡眠情况。
然而,使用加速度记录仪对PD睡眠障碍进行评价仍有其不足之处。因加速度记录仪是通过记录运动状态来评价睡眠状况,而并非直接通过脑部电生理活动对睡眠状况进行评价,所以患者身体异常活动会对睡眠质量的评价产生干扰,且不能反映睡眠中的快速眼动期、慢波睡眠期等具体睡眠参数。一部分PD患者存在肢体不自主震颤,会对通过身体活动判断睡眠状况的数据产生影响。如何通过一定手段去除运动干扰因素,以提高其对睡眠障碍评价的准确度,值得进一步深入研究。
[1]Chaudhuri KR,Pal S,DiMarco A,et al.The Parkinson's disease sleep scale:a new instrument for assessing sleep and nocturnal disability in Parkinson's disease[J].J Neurol Neurosurg Psychiatry,2002,73(6):629-35.
[2]蒋雨平,王 坚,丁正同,等.原发性帕金森病的诊断标准(2005年)[J].中国临床神经科学,2006,14:40.
[3]Chaudhuri KR,Schapira AH.Non-motor symptoms of Parkinson’s disease:dopaminergic pathophysiology and treatment[J].Lancet Neruol,2009,8(5):464-474.
[4]EI-Agnaf OM,Salem SA,Paleologou KE,et,al.Detection of oligomeric forms of alpha-synuclein protein in human plasma as a potential biomarker for Parkingson’s disease[J].FASEB,2006,20(3):419-425.
[5]Olanow CW,Watts RL,KollerWC.An algorithm(decision tree)for the management of Parkinson ’s disease(2001):treatment guidelines[J].Neurol,2001,56(11):S12S88.
[6]Abe K,Hikita T,Sakoda S.Sleep disturbances in Jap-anese patients with Parkinson′s disease-comparing with patients in the UK[J].J Neurol Scien,2005,234:73.
[7]潘卫东,方正龙,郭 伸,等.增效安神止颤2号方对帕金森病运动与非运动症状疗效评价[J].上海中医药大学学报,2009,23(4):29-34.
[8]潘卫东,方正龙,郭 伸,等.养血清脑颗粒改善帕金森病睡眠障碍疗效评价[J].上海中医药大学学报,2010,24(4):38-41.
[9]Dhawan V,Healy DG,Pal S,et al.Sleep-related problems of Parkinson’s disease[J].Age ageing,2006,35:220-228.
[10]Manni R,Terzaghia M,Sartoria I,et al.Dopamine agonists and sleepiness in PD:Review of the literature and personal findings[J].Sleep Medicine,2004,5(2):189-193.
[11]Schafer D,Greulich W.Effects of parkinsonian medications on sleep[J].J Neurol,2000,247(Suppl 4):24.
[12]Kaynak D,Kiziltan G,Kaynak H,et al.Sleep and sleepiness in patients with Parkinson′s disease before and after dopaminergic treatment[J].Eur J Neurol,2005,12(3):199.
[13]杨小丽,崔 宏,闫 肃.解痉止颤方联合多芭丝肼片治疗肝肾阴虚型帕金森病56例[J].陕西中医,2010,31(10):1335-1336.
[14]王汝铎,安丽芝,姜 华.清心化痰汤治疗帕金森病30例[J].陕西中医,2011,32(2):163-164.
[15]王惠民,吴定怀,刘小红,等.滋肾养肝熄风通络法配合美多芭治疗帕金森病30例[J].陕西中医,2007,28(6):668-669.
[16]Pan W,Kwak S,Liu Y,et al.Traditional Chinese Medicine Improves Activities of Daily Living in Parkinson’s Disease[J].Parkinson’s Disease.2011,doi:10.4061/2011/789506.

