替吉奥联合顺铂与吉西他滨联合顺铂治疗晚期非小细胞肺癌的疗效对比观察
梁 华 张海梅 贺文茜 张清山
非小细胞肺癌是目前世界主要癌症死亡原因之一,虽然近年来肺癌靶向药物的研究取得了突破性进展,但在我国化疗仍然占据了晚期非小细胞肺癌治疗的重要地位。第三代肺癌化疗药物问世以来,其疗效固然肯定,但也不可避免的带来了毒副作用大的问题。尤其对于晚期非小细胞肺癌患者,机体功能多处于较差水平,尽可能选用低毒高效的化疗药物是值得研究的重点。替吉奥是一种由替加氟、吉美嘧啶(CDHP)及奥替拉西钾(OXO)按照1∶0.4∶1摩尔比组成的新型口服抗肿瘤药物[1]。大量Ⅰ期及Ⅱ期临床研究已经证实,单药替吉奥对多种实体瘤具有明显的抑制作用,如胃癌、结直肠癌、乳腺癌、胰腺癌、宫颈癌,包括肺癌[2]。由于其毒性反应较低,使其可以以全量与其他药物组成联合方案。在日本,替吉奥是唯一被批准用于一线治疗晚期非小细胞肺癌的口服化疗药。本文旨在研究替吉奥联合顺铂治疗我国晚期非小细胞肺癌,其有效性和安全性是否不劣于标准化疗GP方案。
1.材料与方法
1.1 材料 共入组95例于2010年8月至2011年4月期间就诊我院的初治ⅢB-Ⅳ期NSCLC患者。其中男性61例,女性34例,年龄38~79岁,中位年龄56岁。所有患者符合以下临床特征:均经病理学确诊,PS评分0~2,有明确的可测量病灶,预计生存期大于3个月,无严重的脏器功能损害,具体见表1。所有患者化疗前均进行基线测定,包括经CT或MRI测得的初始病灶大小、血常规、肝肾功、血凝常规等,并于每两周期化疗后复测。
1.2 治疗方法 44例患者接受A组:替吉奥(商品名维康达,山东新时代药业有限公司,国药准字H20080802),根据体表面积调整剂量:40mg,BSA≤1.25m2;50mg,1.25m2< BSA≤1.5m2;60mg,BSA >1.5m2,口服 2 次/日,d1 ~14,联合顺铂25mg/m2静滴,每天1次,d1~3化疗。51例接受B组:吉西他滨(商品名泽菲,江苏豪森药业有限公司,国药准字H20030104)1000mg/m2静滴d1,d8,联合顺铂25mg/m2静滴每天1次,d1~3化疗,每三周重复。最多接受6个周期化疗。
1.3 评价标准 化疗近期疗效评价根据实体瘤评价标准RECIST1.0分为:完全缓解(CR),部分缓解(PR),稳定(SD),进展(PD),并计算客观有效率(CR+PR)及疾病控制率(CR+PR+SD)。药物不良反应按照CTCAE3.0分级标准进行评判。中位随访期为15个月,进一步计算无疾病进展时间(PFS)及一年生存率。
1.4 统计学方法 使用SPSS17.0统计软件进行数据分析。用卡方检验比较两组近期疗效,用Kaplan-Meier法进行生存分析,并根据Cox回归模型比较两组生存曲线。

表1 95例患者的一般临床资料
2.结果
2.1 疗效分析 所有患者共接受382周期化疗,平均为4周期。其中A、B两组客观有效率(RR)分别为22.7%和25.5%(P=0.15),疾病控制率(DCR)分别为72.7%和74.5%(P=0.32),两组间无统计学差异(表2)。所有患者中位随访时间为15个月,其中死亡39例,存活48例,失访8例。A、B两组一年生存率分别为53.5%和51.9%。中位PFS分别为5.3个月(95%CI,5.091~5.509)和4.8个月(95%CI,,4656 ~4.944)差别无统计学意义(Log-rank P=0.513)(图1)。
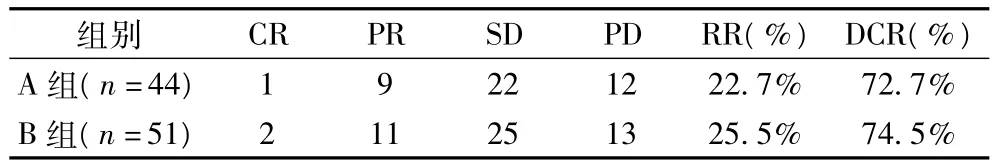
表2 A、B两组近期疗效比较

图1 A、B两组PFS比较
2.2 安全性分析 B组化疗后3~4级骨髓抑制发生率明显高于A组,以中性粒细胞和血小板下降最为显著。A组口腔黏膜反应及末梢神经毒性发生率高于B组。两组不良反应均在可耐受范围内,没有化疗相关致死性事件。

A 组B 组P Total(%)白细胞减少 14.6 50.4 24.2 87.4 0.014* 0.001*粒细胞减少 24.3 52.2 62.4 88.6 0.001* 0.015*血小板减少 27.8 57.5 73.2 89.1 0.001* 0.008*贫血 15.6 74.7 17.4 82.3 0.462 0.191恶心呕吐 3.3 36.5 2.8 40.7 0.581 0.074腹泻 5.0 41.3 4.9 46.8 0.663 0.227口腔黏膜炎 5.2 65.7 3.1 38.7 0.048* 0.014*末梢神经毒性 4.6 56.5 3.2 41.4 0.064 0.042*肝功能损害 2.1 34.2 3.3 38.7 0.374 0.439肾功能损害项目3~4级(%)Total(%)3~4级(%)Total(%)3~4级(%)2.3 22.4 2.7 28.1 0.628 0.552
3.讨论
替吉奥胶囊是一种新型的口服氟尿嘧啶衍生物,它是由由替加氟、吉美嘧啶(CDHP)及奥替拉西(OXO)按照1:0.4:1摩尔比组成。替吉奥胶囊有三方面作用机制:替加氟作为5-Fu的前体药物,是替吉奥胶囊的主要抗肿瘤成分,但由于替加氟代谢后所产生的氟尿嘧啶在体内极不稳定,容易被正常器官和肿瘤组织中的二氢嘧啶脱氢酶(DPD)快速降解达85%以上而失活[3]。吉美嘧啶是一种强力的DPD可逆性竞争抑制剂,能有效减缓氟尿嘧啶的分解,在血浆中长期保持高浓度的5-Fu水平从而提高抗肿瘤效力。奥替拉西口服吸收后可在胃肠道选择性地作用于乳清酸磷酸核糖基转移酶(OPRT),从而阻断5-Fu磷酸化引起的胃肠道毒性,减轻了替加氟的胃肠道副作用。
与胃、肠、乳腺等器官相比,肺组织中DPD活性最高[4]。体外研究表明,5-Fu和卡培他滨对肺癌细胞株的抗肿瘤疗效随着DPD活性升高而降低,而替吉奥作为复方制剂,能有效抑制DPD活性,故其抗肿瘤疗效与肿瘤内DPD浓度无关。因而替吉奥胶囊被尝试用于NSCLC的治疗。
一项Ⅱ期研究证实,替吉奥单药治疗晚期非小细胞肺癌其有效率22%,中位生存时间10.2个月[5]。替吉奥联合治疗方案有效率达23% ~47%,中位生存期达11~18.8个月。日本学者对替吉奥联合铂类治疗晚期非小细胞肺癌进行了Ⅲ期临床随机对照研究,将其与标准的含铂两药方案进行了对比。2010年ASCO会议上发表的LETS研究显示,替吉奥联合卡铂与紫杉醇联合卡铂治疗晚期NSCLC中位生存期为15.2个月对13.3个月,一年生存率为57.3%对55.5%,无统计学差别[6],其疗效不劣于标准含铂两药方案。另有研究发现替吉奥与顺铂联合治疗非小细胞肺癌在各种组织细胞类型中均有效,这与另一种胸苷酸合成酶(TS)抑制剂——培美曲塞不同,后者对鳞癌治疗效果较差[7]。这些研究结论充分证实了替吉奥在非小细胞肺癌治疗中的价值。2004年日本批准替吉奥用于治疗非小细胞肺癌。
本文在我国汉族晚期非小细胞肺癌患者的治疗中同样观察到了替吉奥联合顺铂的不俗疗效,与标准含铂两药方案相比,疗效确定,毒副作用较小,且口服给药方便,患者依从性较好,也便于医务人员根据化疗反应随时调整用量,尤其对老年患者或体质差的患者是一种较为安全的化疗选择。由于观察时间不足,未能统计有效生存期数据,将于后续研究进一步探讨。
1 Shirasaka T,Nakano K,Takechi T,etal.Antitumor activity of1 M tegafur-0.4 M5-chloro-2,4-dihydroxypyridine-1 M potassium oxonate(S-1)against human colon carcinoma orthotopically implanted into nude rats[J].Cancer Res,1996,56:2602 -2606.
2 汪进良,焦顺昌.替吉奥用于非小细胞肺癌治疗的研究及展望[J].中华医学杂志,2010,90(36).
3 Hoff PM.The tegafur-based dihydropyrimidine dehydrogenase inhibitory fluoropyrimidines,UFT/leucovorin(0RZEL)and S-l:a review of their clinical development and therapeutic potential[J].Invest New Drugs,2000,18:331 -342.
4 Fukushima M,Morita M,Ikeda K,et al.Population study of expression of thymidylate synthase and dihydropyrimidine dehydrogenase in patientswith solid tumors[J].Int JMol Med,2003,12:839 -844.
5 Kawahara M,Furuse K,Segawa Y,et al.Phase II study of S-1,a novel oral fluo-rouracil,in advanced non-small-cell lung cancer[J].Br J Cancer,2001,85:939 - 943.
6 Isamu Okamoto,Hiroshige Yoshioka,Phase IIITrial Comparing Oral S-1 Plus Carboplatin With Paclitaxel Plus Carboplatin in Chemotherapy-Naive PatientsWith Advanced Non-Small-Cell Lung Cancer:Results of a West Japan Oncology Group Study[J].JCO VOLUME,20,2010.
7 Yamamoto N,Ichinose Y,Kubota K,Sakai H,Gemma A,Saijo N,et al.Jpn JLung Cancer(Haigan),2008,48:432.

