植酸钠修饰玻碳电极测定铅(Ⅱ)
阮 勇,朱 艳,龙 丽,黄杉生
(上海师范大学生命与环境学院,上海201418)
0 引言
铅是化工企业排放污水中常见的有毒物质,也是对环境危害较重的有毒元素,所以建立相应高灵敏的检测方法对环境监测有着重要的意义。目前,测定水样中铅含量的方法主要有分光光度法[1]、原子吸收光谱法[2~3]、荧光分析法以及电化学方法[4]等。
植酸又称为肌醇六磷酸,是一种环境友好的天然化合物[5],易溶于水。研究证明,植酸是一种广泛存在于植物中有机磷化合物,在抗氧化剂、防腐剂、水质软化剂等方面应用广泛。植酸分子的结构中含有六个不共平面的磷酸键,大量文献已经证明,磷酸基团与金属离子间有强的络合作用。但植酸在与金属离子络合时一般不采取其它配体与金属的络合方式,而是通过环上的磷羟基氧原子与金属离子配位,同时金属离子又与邻近植酸分子中羟基氧原子发生配位,从而形成结构复杂的络合物。该文利用铅离子易于与植酸形成配合物这一特性,探讨铅离子在植酸钠修饰玻碳电极上的电化学行为,建立了一种测定溶液中微量铅的新方法。该分析方法简便、快速,灵敏度较高,选择性好,可用于实际样品中铅的测定。
1 实验部分
1.1 实验试剂和仪器
肌醇六磷酸钠(又名植酸IP6,分析纯,sigma公司,美国);硝酸铅(分析纯);实验用水均为高纯水(>18 MΩ·cm)。
CHI660c型电化学工作站(上海辰华仪器有限公司);三电极体系:IP6/GEC为工作电极,饱和甘汞电极为参比电极,铂电极为对电极;SK2200H超声仪(上海科导超声仪器有限公司);PHS-3C型酸度计(上海伟业仪器有限公司)
1.2 修饰电极的制备
玻碳电极(GCE,Ф=3 mm)先在细金相砂纸(6#)上轻轻打磨,然后用 0.3 μm 的 Al2O3粉末将电极在麂皮上抛光成镜面,之后再将电极依次置于超纯水、乙醇、超纯水中各进行3 min超声清洗。最后,取出电极冲洗后用氮气吹干后待用。取4 μL肌醇六磷酸钠(1 mmol/L)溶液滴涂到玻碳电极表面,自然晾干。为简便计,得到的电极简写为IP6/GEC。
1.3 实验方法
准确称取已计算好质量的硝酸铅于100mL容量瓶中,加pH3.0的盐酸溶液溶解配制为6 mmol/L Pb(Ⅱ)标准溶液,待用。配置 0.1 mol/L 醋酸-醋酸钠溶液,倒入电解池中,加入一定量体积硝酸铅标准溶液,将三电极体系置于电解液中,在-1.1~-0.2 V 之间做循环伏安扫描,测得在-0.5 V处有一还原峰。连续循环扫描3~4次,峰电流强度稳定,再用线性扫描伏安法测定Pb2+的峰电流数值。每次测定后,电极在空白电解液中循环扫描至不再出现还原峰,即可更新电极。
2 结果与讨论
2.1 Pb2+在修饰电极上的电化学行为
图1为Pb2+在裸玻碳电极上(曲线a)和植酸钠修饰电极上(曲线b)的循环伏安曲线图。由图可知,Pb2+在修饰电极上的还原峰电流强度明显大于裸玻碳电极,表明植酸钠修饰电极对铅的还原具有增敏作用,有效提高了Pb2+测定的灵敏度。我们推测,相关反应如下:
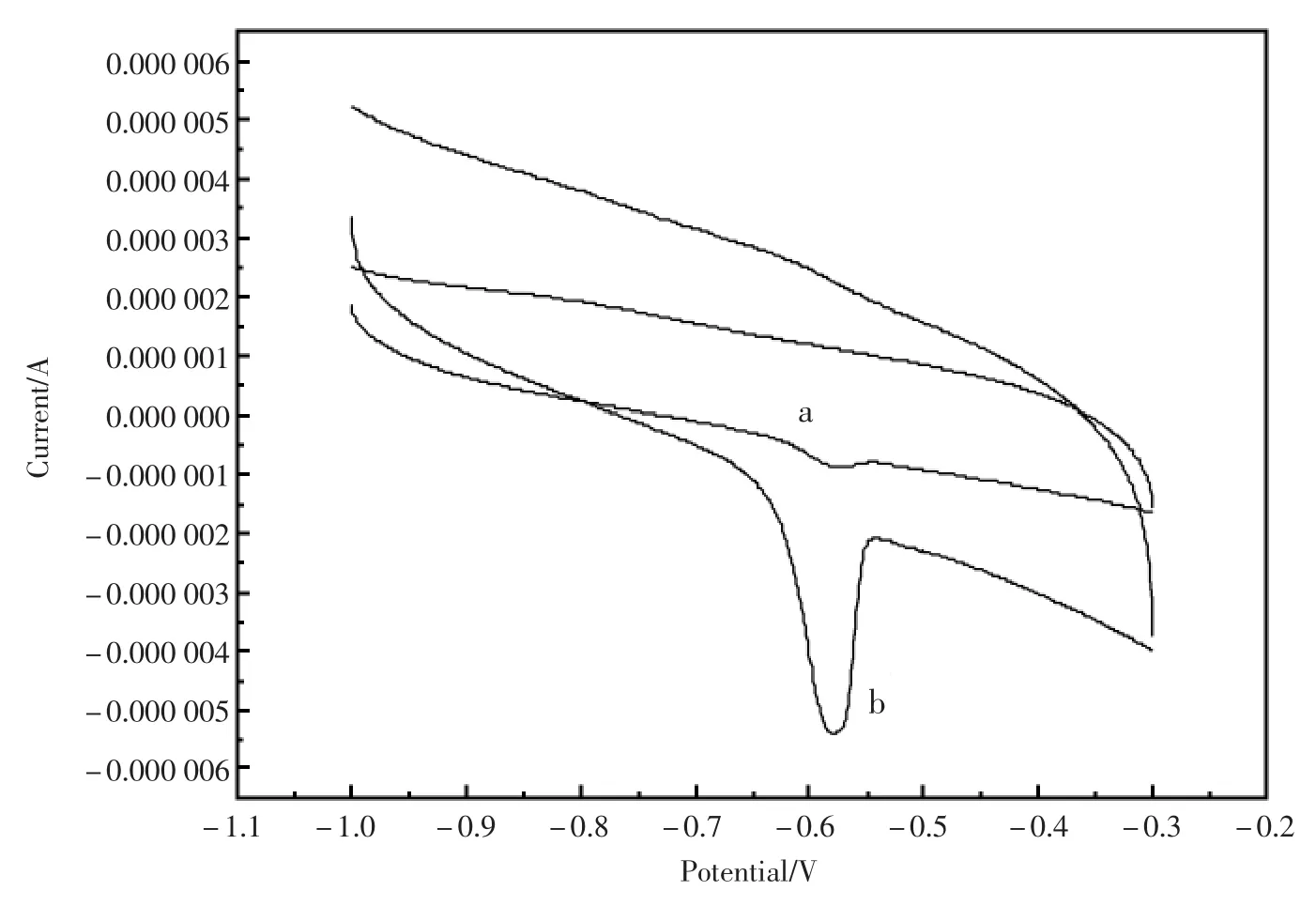
图1 1.0×10-5mol/L Pb2+在裸玻碳电极上(曲线a)和植酸钠修饰电极上(曲线b)的循环伏安曲线图Fig.1 Cyclic Voltammograms of the bare GC electrode(a)and the modified electrode in 0.1mol/L HAc-NaAc with 1.0×10-5mol/L Pb2+
2.2 底液选择
维持溶液中 Pb2+浓度为 1.2×10-5mol/L,底液浓度均为 0.1 mol/L, 考察了 Pb2+分别在 KNO3、NaCl、KCl、NaOH、KHPO 、PBS HAc-NaAc缓冲液为底液时的电化学响应。结果表明,在HAc-NaAc缓冲液溶液中,铅的峰电流强度最大,故选择0.1 mol/L HAc-NaAc缓冲液作为测定Pb2+的底液。
2.3 溶液pH值的影响
在pH4.9到pH8.9范围内依次改变溶液pH值,将修饰电极分别放入含有1.2×10-5mol/L Pb2+的0.1 mol/L HAc-NaAc缓冲液中,分别进行线性伏安扫描。结果表明,其他实验条件不变,当pH=5.6时,还原峰电流强度达到最大(图2),故选择最佳 pH 在 5.6。
2.4 扫描速率对峰电流的影响
考察了电位扫描速度对电极峰电流的影响(图3),由图3可见峰电流是随着扫描速率的增加而变大,其他实验条件不变,在50~500 mV/s之间呈线性关系,说明修饰电极是受吸附作用控制的不可逆过程[6~7]。
2.5 膜的厚度对峰电流的影响
峰电流的大小和电极表面修饰的植酸膜厚度有关(图4)。实验表明,其他实验条件不变,滴加的植酸的量增加,则电极表面与Pb2+的结合位点增加,响应电流增加,但当电极表面滴加植酸溶液(1 mmol/L)超过4 μL时,由于膜的厚度妨碍电子的转移,导致峰电流强度减小,故电极表面滴加 4 μL 植酸溶液(1 mmol/L)为佳。
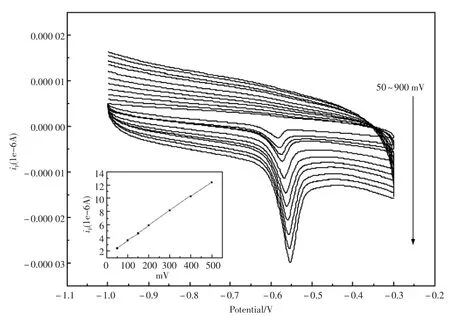
图3 不同扫描速率对Pb2+在IP6/GEC上的峰电流的影响以及峰电流和扫描速率的关系Fig.3 The influence of scan rates on the peak current of lead ion on IP6/GEC Inset:the relationship between peak currents and scan rates
2.6 线性范围和检出限
图5为不同Pb2+浓度在修饰电极的方波伏安响应曲线。实验表明,在最佳实验条件下,以修饰电 极 为 工 作 电 极 ,0.1 mol/L pH=5.6 的 HAc-NaAc缓冲溶液为支持电解质,峰电流随着Pb2+浓度的增加而增大,在 1.2×10-6~1.2×10-5mol/L 范围内呈线性关系,线性方程为: ip=1.555+0.393c,r=0.998,检出限为 8.0×10-7mol/L。
2.7 干扰试验及重复性
Pb2+浓度为 1.2×10-5mol/L 时 100 倍的 Ca2+、Ni2+、K+、Cd2+、Mn2+、Mg2+均不产生干扰,100 倍的NO-3,1000倍的Cl-不产生干扰,并且修饰后的玻碳电极对 Pb2+浓度为 1.2×10-5mol/L的溶液平行测定 10次,峰电流响应 RSD为 1.3%,重复性较好。
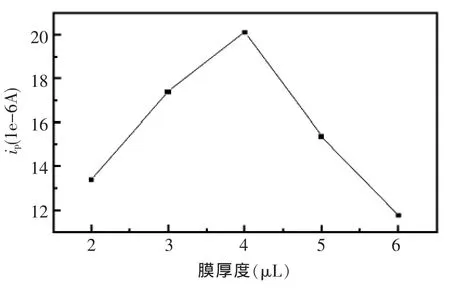
图4 膜的厚度对Pb2+在IP6/GEC上的峰电流的影响Fig.4 The influence of the thickness of the film on the response of IP6/GEC
2.8 样品测定及回收率测定
取合成样品,以方波伏安法测定其Pb2+含量,结果见表1。在试样中加入不同含量的Pb2+标准溶液,测定其回收率,结果亦列入表1。回收率在97.1% ~ 103.3%之间,结果满意。
3 结论
在植酸钠修饰玻碳电极对铅(Ⅱ)离子有良好的电流响应,在优化实验条件下,电极的峰电流强度和一定浓度范围内的铅(Ⅱ)离子呈良好的线性关系,相对于裸玻碳电极而言,峰电流响应大大提高。该修饰电极方法简单,性能稳定,可用于测定痕量铅(Ⅱ)离子。
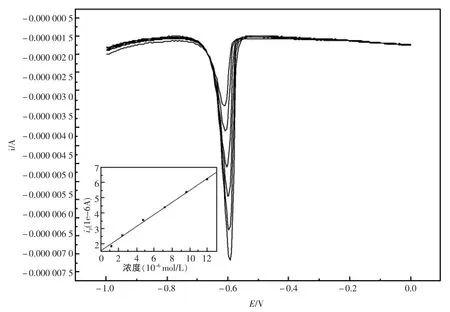
图5 Pb2+在不同浓度时和方波峰电流的线性关系Fig.5 The response of Pb2+at modified electrode Inset:the linear relationship between Pb2+and peak current
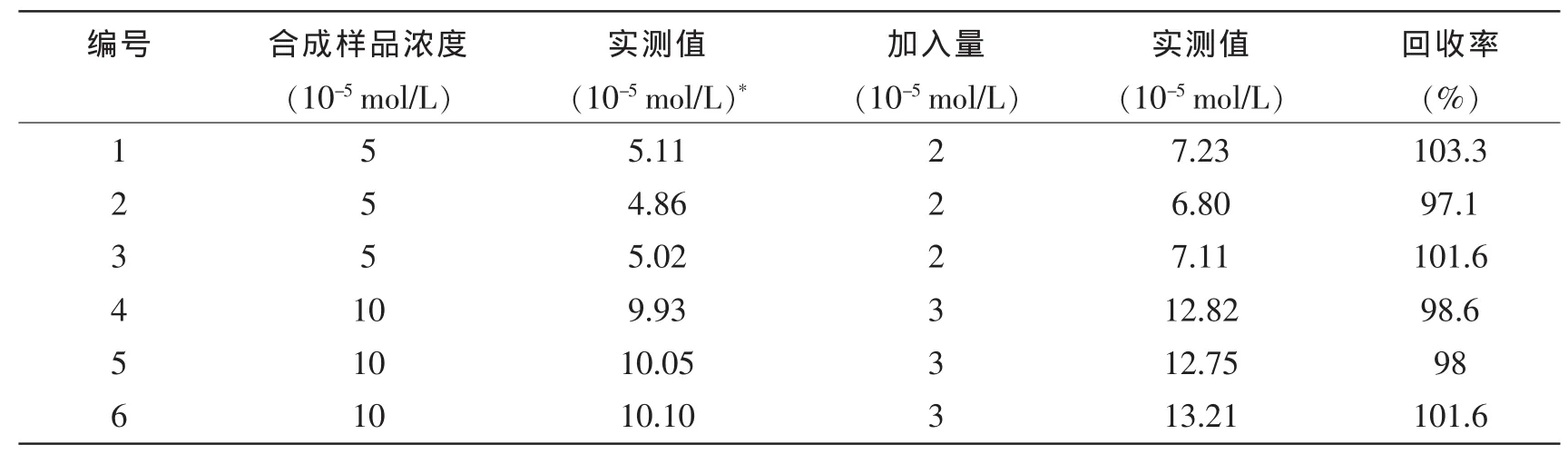
表1 样品及回收率测定Tab.1 Sample and the determination of recovery
[1]谢启明,罗琴,杨光宇,等.磺硝酚偶氮若丹宁固相萃取光度法测定环境样品中的铅[J].分析试验室,2005,24(4):30~32.
[2]高甲友.流动注射在线富集一火焰原子吸收光谱法测定痕量铅[J].冶金分析,2006,26(6):57~59.
[3]吴媛娜,葛菊,李咏梅,等.石墨炉原子吸收光谱法测定水中的微量铅[J].鞍山师范学院学报,2005,7(2):54~55.
[4]袁冬梅,杨玲娟,李一婧.水样中铅的荧光分析[J].辽宁化工,2006,35(2):121~124.
[5]Moraes M L,Oliveira Jr O N,Filho U P R,et al.Phytase immobilization on modified electrodes for amperometric biosensing[J].Sens.Actuators B,2008,131:210~215.
[6]李军,李洪坤,赵艳霞,等.L一半胱氨酸修饰银电极对锌离子的测定[J].化学传感器,2004,24(3):56~58.
[7]白燕,程涛,李继革,等.L一半胱氨酸修饰银电极及其对铜离子的电化学测定[J].分析化学,2002,30(3):383.

