兔源益生菌Tu-115菌株鉴定及其产纤维素酶固体发酵条件优化
尚 伟 姜军坡 王世英 朱宝成
纤维素酶由起协同作用的葡聚糖内切酶、葡聚糖外切酶、β-葡聚糖苷酶等3个主要组分组成,它可将纤维素降解产生葡萄糖,并可进一步发酵生产酒精、SCP饲料蛋白、有机酸等物质,对缓解全球能源危机、饲料资源紧张、保护环境等具有很重要的意义[1-2]。细菌和真菌都可以产生纤维素酶;细菌主要产中性纤维素酶和碱性纤维素酶[3],较真菌纤维素酶具有更好的耐碱、耐热性,更适于工业生产,因此,细菌纤维素酶已成为研究的热点[4]。
通常细菌纤维素酶的产量较少,筛选高产纤维素酶的细菌菌株并采用合理、有效的发酵方式使得纤维素酶各组分呈现较佳的协同作用,提高细菌产生的纤维素酶量,对于细菌纤维素酶的应用具有重要意义。叶明等[5]从土壤中筛选出产纤维素酶的蜡样芽孢杆菌(Bacillus cereus)B1菌株,并通过经微波-硫酸二乙酯复合诱变得到具有较高产纤维素酶活能力的正突变菌株B1-1,优化发酵条件后纤维素酶活可以达到0.436 IU/ml。吕静琳等[6]从腐烂朽木中筛选得到高产纤维素酶的Bacillus cereus LT3菌株,用20 g/l甘蔗渣,pH值7.0、30℃培养120 h,CMC酶酶活为71.17 U/ml,滤纸酶酶活为33.37 U/ml。侯进慧等[7]从农田、农产品果实表面筛选出一株产低温纤维素酶活力较高的Bacillus cereus T34菌株,优化后纤维素酶酶活达到1.43 U/ml。Lee等[8]在7 L的生物反应器中对从海洋中筛选的Bacillus subtilis subsp.subtilis A-53菌株产羧甲基纤维素酶的液体发酵条件进行了优化,在7 L和100 L的生物反应器中产生的纤维素酶的量分别可以达到150.3和196.8 U/ml。胡青平[9]对细菌菌株Z1产纤维素酶的条件进行了优化,CMC酶活力最高可达1325 μg/(ml·min),滤纸酶活力最高可达93.8 μg/(ml·min)。
Tu-115菌株是本研究组从兔子盲肠中筛选得到的一株既具有抑制大肠杆菌活性,又可在胞外大量产生纤维素酶的优良菌株。本研究欲测定Tu-115菌株的生理生化特性,并对其进行16S rDNA序列分析,以鉴定其种属。分别以CMC和滤纸为底物测定纤维素酶比活力,采用单因素试验考察发酵培养基的碳源、氮源、碳氮比例、麸皮粒度、温度、发酵时间等因素对该菌株产纤维素酶的影响;以滤纸为底物测定纤维素酶比活力,采用正交试验考察培养基料水比、接种量、培养基初始pH值及装瓶量等因素对Tu-115菌株产纤维素酶的影响,以确定Tu-115菌株固体发酵产纤维素酶的最适条件,为该菌株应用于纤维素酶生产奠定基础。
1 材料和方法
1.1 材料及仪器
Tu-115菌株,由本实验室分离保存。
Mandel's无机盐营养液及DNS试剂配制方法参考文献[10]。
芽孢杆菌种子培养基:蛋白胨2 g、蔗糖2 g、Mandel′s无机盐营养液 100 ml,自然 pH 值。
基础发酵培养基:蛋白胨 2 g、蔗糖 2 g、Mandel′s无机盐营养液8 ml,自然pH值。
ZHWY-2112B型双层摇床,上海智诚分析仪器有限公司生产;GL-21M型高速冷冻离心机,上海卢湘仪离心机仪器有限公司生产;Labo Autoclave型高压灭菌锅,日本Sanyo公司生产;AIR TECH超净工作台,苏净集团安泰公司生产;SPX-250型智能生化培养箱,宁波海曙赛福实验仪器厂生产;BS 214 D型分析天平,德国Sartorius公司生产;6405紫外-可见分光光度计,英国Jenway公司生产。
1.2 方法
1.2.1 Tu-115菌株鉴定
1.2.1.1 菌株形态特征及生理生化特征的测定
菌株形态特征及生理生化特征测定依据东秀珠等《常见细菌系统鉴定手册》[11]。
1.2.1.2 16S rDNA序列分析
采用通用引物27F/1492R进行16S rDNA的PCR扩增,由上海生工生物工程技术服务有限公司完成并进行测序。将所得序列与GenBank数据库中序列进行BLAST分析,并选取相似性较高的标准菌株用MEGA 4.1以Neighbor-Joining法构建系统发育树。
1.2.2 发酵条件对Tu-115菌株产纤维素酶影响的测定
挑取菌种,接种于种子培养基中,装瓶量为100 ml/250 ml。于200 r/min,37℃,摇床培养12 h后使用。
基础发酵条件为:在250 ml的三角瓶中放入4.0 g发酵底物(除另有说明外,碳源2.0 g和氮源2.0 g),8 ml营养液,Tu-115菌株种子液2 ml,30℃下培养48 h。
测发酵物的质量,与发酵前加入的培养基质量比较。向三角瓶中加入一定体积的蒸馏水,室温下浸泡1 h,期间不断搅拌。混匀后取1 ml加入EP管中,12000 r/min离心5 min,取上清液测定酶活力。取样后,测定三角瓶中残余发酵液的体积。分别测定出每1 g发酵物中含有的纤维素酶活力和每瓶发酵物中含有纤维素酶的总活力。
以CMC为底物测定纤维素酶活力的方法[12]:每1min催化CMC水解生成1 μmol葡萄糖的酶量为一个CMC酶活力单位(IU)。
以滤纸为底物测定纤维素酶活力的方法[13]:每1 min催化滤纸水解生成1 μmol葡萄糖的酶量为一个滤纸酶活力单位(IU)。
每个试验设3次平行,每个平行测定2次,最后取平均值。根据试验结果确定各因素的最适水平。每一个因素的优化都在上一个因素最优水平上进行。
1.2.2.1 单因素试验分析
改变试验条件,对产纤维素酶活力进行单因素分析:①分别以葡萄糖:麸皮(1:1)、麦芽糖:麸皮(1:1)、蔗糖:麸皮(1:1)、糖蜜:麸皮(1:1)、蔗糖、麦芽糖、葡萄糖、糖蜜、麸皮作为碳源,考察发酵培养基碳源的影响;②取最优碳源,按碳源:营养液=1:2加入Mandel's营养液,分别以尿素、NH4Cl、(NH4)2SO4、KNO3、NaNO3、NH4NO3、蛋白胨、酵母膏和豆饼粉作为氮源,称取0.3 g,考察发酵培养基氮源的影响;③取最优碳源,按碳源:营养液=1:2加入Mandel′s营养液,再分别称取最优氮源 0.05、0.10、0.15、0.20、0.25、0.30、0.35、0.40、0.45、0.50 g,考察发酵培养基碳氮比例的影响;④取最优碳源、氮源及碳氮比例,将麸皮粉碎,依次过20目、40目、60目和100目筛,按麸皮粒度从大到小的次序依次编号为1号、2号、3号、4号、5号麸皮粉末,分别取相应的麸皮粉末作为碳源,配制成发酵培养基,考察发酵培养基麸皮粒度的影响;⑤取最优碳源、氮源及碳氮比例,麸皮取最适宜粒度,接种后分别在28、30、32、35、37、40 ℃环境中培养,考察发酵温度的影响;⑥取最优碳源、氮源及碳氮比例,麸皮取最适宜粒度,在最适温度下发酵,从发酵24 h开始,每隔24 h抽样进行酶活测定,直至240 h,考察发酵时间的影响。
1.2.2.2 正交试验优化发酵条件
选取培养基料水比、接种量、培养基初始pH值、装瓶量4个因素,设计4因素3水平L9(34)正交试验进行产纤维素酶发酵条件优化。培养后,以滤纸为底物测定纤维素酶比活力,并进行比较。各试验组数据均为3次平行试验的平均值。
采用SPSS软件对正交试验结果进行极差(Range)分析和一般线性模型(General Linear Model,GLM)分析,以得出最佳培养基组成。若优化的最佳发酵条件未在正交表中出现,则平行测定最佳发酵条件和正交表中最佳条件下对应的纤维素酶比活力,重复6次,进行验证。
2 结果与分析
2.1 Tu-115菌株鉴定结果
2.1.1 菌株形态特征及生理生化特征测定结果
Tu-115菌株生理生化特征测定结果(见表1)表明,该菌株呈现典型的芽孢杆菌属生理生化特征。Tu-115菌株为革兰氏阳性杆菌,菌体两端平整,芽孢中生,见图1(a)。在NB培养基上菌落为圆形,乳白色,表面光滑,有火山状凸起,边缘锯齿状,见图1(b)。综合以上结果可以初步将Tu-115菌株鉴定为芽孢杆菌。

表1 Tu-115菌株生理生化试验的结果

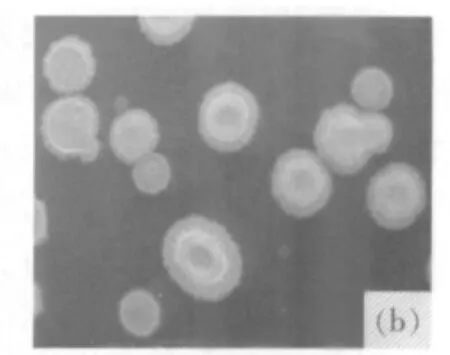
图1 Tu-115菌株革兰氏染色结果及其菌落形态
2.1.2 16S rDNA序列系统发育分析
基于与Tu-115菌株同源性高的菌株和芽孢杆菌属其他种的菌株构建系统发育树,图2所示,其中与解淀粉芽孢杆菌(Bacillus amyloliquefaciens)同源性最高。Tu-115菌株与解淀粉芽孢杆菌的相似性高达99.16%(见表2)。结合其生理生化特征,可确定Tu-115菌株为解淀粉芽孢杆菌。

图2 芽孢杆菌Tu-115菌株的系统进化树

表2 Tu-115菌株与几种标准菌株的相似性比较
2.2 发酵条件优化结果
2.2.1 单因素试验分析各因素对Tu-115菌株产纤维素酶的影响
由图3(a)可知,在各个碳源组合中,麸皮对应的两种纤维素酶比活力均较高,同时发酵物具有较高的纤维素酶总活力。由图3(b)可知,同一氮源下分别采用CMC和滤纸为底物测定纤维素酶比活力,其结果相差较大,以两种纤维素酶比活力同时较高者作为氮源较为适宜,故选取豆饼粉为最适宜氮源,此时发酵物呈现中等的纤维素酶总活力。由图3(c)可知,当碳氮比为4:1时对应的两种纤维素酶比活力均较高,此时发酵物呈现较高的纤维素酶总活力。

图3 碳源、氮源及碳氮比对Tu-115菌株产纤维素酶的影响
由图4(a)可知,当以1号麸皮粉末为碳源时,对应的两种纤维素酶比活力均较高,并表现出较高的纤维素酶总活力;由图4(b)可知,当培养温度为35℃时,对应的两种纤维素酶比活力均最高,同时具有较高的纤维素酶总活力;由图4(c)可知,当发酵时间为144 h时,对应的两种纤维素酶比活力均最高,并具有较高的纤维素酶总活力。
综上所述,Tu-115菌株产纤维素酶的适宜条件为:以麸皮为碳源,豆饼粉为氮源,碳氮比为4:1,麸皮粒度在20目以上,在35℃静置培养144 h。在此基础上用正交试验优化Tu-115菌株产纤维素酶固体发酵条件。

图4 麸皮粒度、培养温度及发酵时间对Tu-115菌株产纤维素酶的影响
2.2.2 正交试验优化Tu-115菌株胞外产纤维素酶固体发酵条件
改变培养基料水比、培养基初始pH值、接种量、装瓶量,进行正交试验,对其结果进行极差分析和GLM分析,分析结果见表3、表4。
由表3可知,各因素水平影响的强弱顺序为A2>A3>A1,B2>B1>B3,C2>C3>C1,D2>D3>D1;各因素的主次顺序为D>B>C>A,即装瓶量>培养基初始pH值>接种量>培养基料水比。由表4可知,因素D和B,即装瓶量和培养基初始pH值对试验结果影响显著,而因素A和C对试验结果影响不显著,各因素的主次顺序为D>B>C>A。综上所述,A2B2C2D2为产纤维素酶的最佳发酵条件,与A1B2C2D2进行验证试验(见表5),结果表明,以滤纸为底物时,A2B2C2D2对应的平均纤维素酶比活力为64.06 IU/g(n=6),以CMC为底物时,A2B2C2D2对应的平均纤维素酶比活力为73.35 IU/g(n=6);以滤纸为底物时,A1B2C2D2对应的平均纤维素酶比活力为60.95 IU/g(n=6),以 CMC 为底物时,A1B2C2D2对应的平均纤维素酶比活力为72.65 IU/g(n=6)。综上所述,正交试验优化出的发酵条件对应着较高的纤维素酶比活力,即最佳发酵条件为培养基料水比为1:1、培养基初始pH值4.0、接种量20%、装瓶量4 g/250 ml。

表3 发酵条件正交试验结果的极差分析

表4 发酵条件正交试验结果的一般线性模型分析
3 结论与讨论
3.1 结论
经鉴定,可在胞外产纤维素酶的Tu-115菌株为解淀粉芽孢杆菌。以麸皮为碳源,豆饼粉为氮源,碳氮比4: 1,料水比1: 1,接种量20%,初始pH值4.0,麸皮粒度大于20目,装瓶量4 g/250 ml,在35℃静置培养144 h时,可以达到较高的纤维素酶比活力。
3.2 讨论
Tu-115菌株具有胞外产纤维素酶的特性,具有这种特性的细菌可以通过发酵条件的优化,增加其胞外分泌的纤维素酶量,增大其应用于工业生产的可行性。纤维素酶是一种多组分的酶系,各组分间又存在着协同作用。根据纤维素酶水解的协调理论,水解过程首先由内切葡聚糖酶作用于纤维素酶分子的非结晶区内部的β-1,4-糖苷键,产生的β-寡聚糖再被外切葡聚糖酶作用生成纤维二糖[14],所以内切葡聚糖酶活力的大小很重要。以CMC为底物测定的纤维素酶活力表征的是内切葡聚糖酶活力;滤纸结构中包括结晶型纤维素和非结晶型纤维素,所以通常用以滤纸为底物测定的纤维素酶活力表征纤维素酶复合体系的总活力[15];单因素优化中,同时采用分别以CMC、滤纸为底物测定的两种纤维素酶比活力为指标,可以较好地评价纤维素酶的活力;正交试验中,采用以滤纸为底物测定的纤维素酶比活力为指标,可以更真实地表征优化条件下产纤维素酶复合体系的活力。

表5 发酵条件正交试验结果的验证
解淀粉芽孢杆菌具有广泛的抑制真菌和细菌的活性[16],这和本研究组前期的结果相一致,Tu-115菌株具有抑制大肠杆菌等病原菌的活性。Lee等[17]从土壤中筛选出1株胞外产纤维素酶的解淀粉芽孢杆菌DL-3菌株,并对其胞外产生的纤维素酶进行了纯化和表征。国内尚未见该种属细菌胞外产纤维素酶的报道。本研究采用固体发酵的方式,利用廉价的麸皮,在最优发酵条件下以CMC、滤纸为底物测定的两种纤维素酶比活力分别可达73.35 IU/g和64.06 IU/g,CMC酶和滤纸酶活力基本相当,说明Tu-115菌株产的纤维素酶中内切葡聚糖酶和其他几种纤维素酶组分的比例较为适宜,表现出较佳的协同作用,具有很高的应用潜力。
[1]谷嵩,刘昱辉.纤维素酶的研究进展[J].安徽农业科学,2007,35(25):7736-7737,7747.
[2]Russell J.Jerusik.Fungi and paper manufacture[J].Fungal Biology Reviews,2010,24(1/2):68-72.
[3]陈春岚,李楠.细菌纤维素酶研究进展[J].广西轻工业,2007,23(1):18-20.
[4]张喜宏,刘义波,高云航.纤维素酶及纤维素酶产生菌选育的研究进展[J].饲料工业,2009,30(22):14-16.
[5]叶明,叶崇军,胡士明,等.纤维素酶益生菌的选育及产酶条件[J].合肥工业大学学报(自然科学版),2009,32(11):1730-1734.
[6]吕静琳,黄爱玲,郑蓉,等.一株产纤维素酶细菌的筛选、鉴定及产酶条件优化[J].生物技术,2009,19(6):26-29.
[7]侯进慧,孙会刚,郑宝刚,等.一株产低温纤维素酶细菌的初步分析[J].生物学通报,2010,45(8):44-46.
[8]Bo-Hwa Lee,Bo-Kyung Kim,You-Jung Lee,et al.Industrial scale of optimization for the production of carboxymethylcellulase from rice bran by a marine bacterium,Bacillus subtilis subsp.subtilis A-53[J].Enzyme and Microbial Technology,2010,46(1):38-42.
[9]胡青平.产纤维素酶细菌菌株Z1发酵条件优化 [J].中国粮油学报,2010,25(9):111-114,122.
[10]白洪志.降解纤维素菌种筛选及纤维素降解研究 [D].哈尔滨:哈尔滨工业大学,2008.
[11]东秀珠,蔡妙英.常见细菌系统鉴定手册 [M].北京:科学出版社,2001:43-69.
[12]NY/T 912—2004.饲料添加剂纤维素酶活力的测定—分光光度法[S].中国农业出版社,2005.
[13]GB/T 23881—2009.饲用纤维素酶活力的测定—滤纸法 [S].中国标准出版社,2009.
[14]Natividad Ortega,María D Busto,Manuel Perez-Mateos.Kinetics of cellulose saccharification by Trichoderma reesei cellulases[J].International Biodeterioration&Biodegradation,2001,47(1):7-14.
[15]程抒劼,郑兰娟,林俊芳,等.纤维素酶活力测定研究进展[J].食品工业科技,2009(7):334-336,342.
[16]车晓曦,李校堃.解淀粉芽孢杆菌(Bacillus amyloliquefaciens)的研究进展[J].北京农业进展,2010(3):7-10.
[17]You-Jung Lee,Bo-Kyung Kim,Bo-Hwa Lee,et al.Purification and characterization of cellulase produced by Bacillus amyoliquefaciens DL-3 utilizingricehull[J].Bioresource Technology,2008,99(2):378-386.

