碘酸钾氧化合成3-碘对氨基苯磺酸的研究
孙 涛,孟庆朝,董玉环,刘兴顺
(1. 唐山师范学院 化学系,河北 唐山 063000;2. 迁安夏官营高级中学 化学组,河北 迁安 064409)
碘酸钾氧化合成3-碘对氨基苯磺酸的研究
孙 涛1,孟庆朝1,董玉环1,刘兴顺2
(1. 唐山师范学院 化学系,河北 唐山 063000;2. 迁安夏官营高级中学 化学组,河北 迁安 064409)
以对氨基苯磺酸和碘化钾为原料,碘酸钾为氧化剂,合成了3-碘对氨基苯磺酸,并对影响合成3-碘对氨基苯磺酸的一系列因素进行了研究。研究结果表明,对氨基苯磺酸用量为0.008 mol,碘酸钾用量为1.05 g,以30 mL水作为溶剂,加入4 mL醋酸,温度为70~80 ℃,反应4 h,3-碘对氨基苯磺酸的产率可达到90.05%。
对氨基苯磺酸;碘化钾;碘酸钾;3-碘对氨基苯磺酸
在众多的有机化合物中,碘代芳烃有着独特的地位,它们广泛应用于医药、农药以及材料等领域,是合成药物活性和生物活性化合物的重要中间体[1-4]。
芳香化合物的碘化基本上可分为两类。一类是间接碘化,如用重氮化反应由苯酚制对碘苯酚,需经过硝化、还原、重氮化和置换等步骤,整个过程比较繁杂,每步均有副产物,需经多次萃取、洗涤,产率通常不高于70%,并且产生的大量副产物对环境污染比较大,现在日益被其他方法所取代[5]。另一类是直接碘化,即将单质碘或含碘化合物在一定条件下与芳香化合物反应而直接碘化。它的特点是反应步骤少、条件温和、选择性较好、产率高。如果用单质碘来碘化芳香化合物,因为碘是一种不太活泼的亲电试剂,也难于直接在芳环上发生碘化反应,常常要有氧化剂(如硝酸、双氧水、次氯酸、氯酸钾等)参与才能进行[6-9]。例如以硝酸为氧化剂进行的碘化反应[10]。
本实验采用无水对氨基苯磺酸作为底物,碘化钾代替碘,用碘酸钾作氧化剂,以水作溶剂合成3-碘对氨基苯磺酸。反应方程式如下:

这些反应条件与传统方法相比表现出两个优点:(1)反应效率高,选择性好,单碘取代物收率较高;(2)副产物少,环境污染小。
1 实验部分
无水对氨基苯磺酸、碘化钾、碘酸钾、冰乙酸、硫代硫酸钠等均为市售分析纯试剂。
将1.4 g(0.008 mol)无水对氨基苯磺酸和1.4 g(0.008 4 mol)碘化钾加入100 mL三口烧瓶中并加入30 mL水溶解,加入4 mL冰醋酸,搅拌加热至70~80 ℃,分两次(间隔半小时)向其中加入碘酸钾1.05 g(0.005 mol),保持温度为70~80 ℃,反应4 h,反应结束后在冰水中静置半小时,逐滴加入10%(质量分数)的硫代硫酸钠溶液直至溶液不会使淀粉碘化钾试纸显蓝色,将此混合物抽滤并用蒸馏水洗涤,得到褐色晶状粗产品。用95%乙醇重结晶得浅色针状晶体。计算产率。
2 结果与讨论
2.1 温度对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾的量为1.4 g,碘酸钾用量为1.05 g并分两次间隔半小时加入,加入4 mL冰醋酸,反应4 h,水用量为30 mL。改变温度,考查温度对3-碘对氨基苯磺酸产率的影响,结果见表1。

表1 温度对3-碘对氨基苯磺酸产率的影响
由表1可看出,温度过低在规定时间内反应不完全甚至不反应,温度过高可能发生副反应或碘挥发使产率偏低,由此可确定反应最佳温度为70-80 ℃。
2.2 碘酸钾用量对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾用量为1.4 g,温度保持70-80 ℃,反应4 h,加入4 mL冰醋酸,水的量为30 mL,碘酸钾分两次间隔半小时加入。改变碘酸钾用量,考查碘酸钾用量对3-碘对氨基苯磺酸产率的影响,结果见表2。

表2 碘酸钾用量对3-碘对氨基苯磺酸产率的影响
由表2可看出,随着碘酸钾用量的增加,3-碘对氨基苯磺酸的产率会升高,当碘酸钾用量达到1.05 g时,3-碘对氨基苯磺酸的产率也随之达到最高值90.05%,随后,继续增加碘酸钾用量3-碘对氨基苯磺酸的产率迅速下降。实验过程中也发现,当氧化剂用量高于1.05 g时,副产物增多,这就造成了3-碘对氨基苯磺酸产率的下降。由此选择氧化剂碘酸钾用量为1.05 g。
2.3 反应时间对3-碘对氨基苯磺酸产率的影响
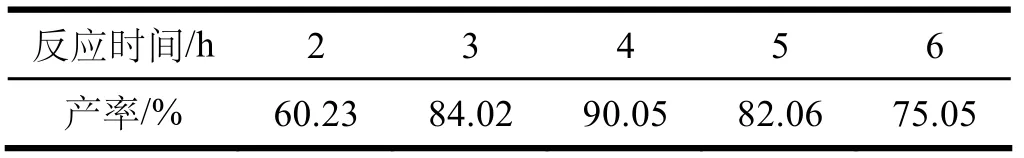
表3 反应时间对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾用量为1.4 g,温度保持70~80 ℃,碘酸钾用量为1.05 g并分两次间隔半小时加入,加入4 mL冰醋酸,水用量为30 mL。改变反应时间,考查反应时间对3-碘对氨基苯磺酸产率的影响,结果见表3。
由表3可见,该反应4 h时3-碘对氨基苯磺酸的产率达到最高的90.05%。反应时间太短造成反应不够充分,致使3-碘对氨基苯磺酸的产率较低;而当反应时间太长时,由于副产物的生成,同样也会造成对3-碘对氨基苯磺酸的产率降低。由此选择反应时间为4 h。
2.4 各种酸对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾用量为1.4 g,温度保持70~80 ℃,氧化剂碘酸钾用量为1.05 g并分两次间隔半小时加入,水用量为30 mL,反应4 h。改变酸的种类(均加入4 mL),考查各种酸对3-碘对氨基苯磺酸产率的影响,结果见表4。
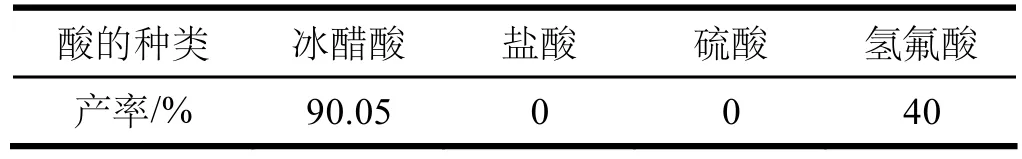
表4 酸的种类对3-碘对氨基苯磺酸产率的影响
由表4可知,加入冰醋酸时3-碘对氨基苯磺酸的产率最高为90.05%。换用其他酸时,3-碘对氨基苯磺酸的产率会降低,这可能是由于强酸释放大量的氢离子,氢离子与氨基结合成铵正离子,大大降低了苯环上亲电反应的活性;弱酸由于不能释放足够的氢离子,不能有效提高氧化剂的氧化性,致使产率降低。由此可见,选用冰醋酸为宜。
2.5 冰醋酸的用量对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾用量为1.4 g,温度保持70~80 ℃,氧化剂碘酸钾用量为1.05 g并分两次间隔半小时加入,水用量为30 mL,反应4 h。加入冰醋酸,考查不同的酸用量对3-碘对氨基苯磺酸产率的影响,结果见表5。
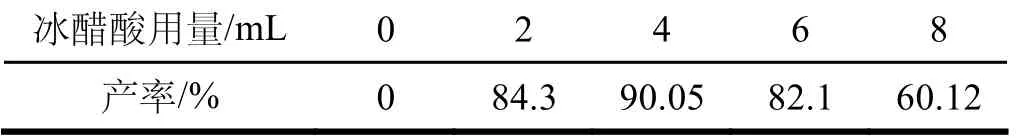
表5 冰醋酸用量对3-碘对氨基苯磺酸产率的影响
由表5可见,冰醋酸的最佳用量为4 mL,此时3-碘对氨基苯磺酸的产率达到最高为90.05%。换作其它量时,3-碘对氨基苯磺酸的产率会降低,这可能是由于酸浓度较高时,氨基转变为铵正离子,使苯环上亲电反应的活性降低,而酸浓度较低时不能有效地提高氧化剂的氧化性,导致产率降低。由此可见,冰醋酸用量以4 mL为宜。
2.6 氧化剂加入方式对3-碘对氨基苯磺酸产率影响

表6 氧化剂加入方式对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾的量为1.4 g,温度保持70~80 ℃,水用量为30 mL,反应4 h,加入冰醋酸4 mL,氧化剂碘酸钾用量为1.05 g,考查氧化剂的不同加入方式对3-碘对氨基苯磺酸产率的影响,结果见表6。
由表6可见,分两次间隔0.5 h加入氧化剂碘化钾时,3-碘对氨基苯磺酸的产率达到最高为90.05%。换用其它加入方式时,3-碘对氨基苯磺酸的产率都会降低,这可能是由于氧化剂一次加入反应过于激烈,副反应增多;当间隔时间较长时,由于不能发生连续的氧化反应,也会使产率降低。由此确定氧化剂以分两次间隔半小时加入为宜。
2.7 溶剂对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾用量为1.4 g,温度保持70~80 ℃,氧化剂碘酸钾用量为1.05 g并分两次间隔半小时加入,反应4 h,加入冰醋酸4 mL,考查不同溶剂(用量为30 mL)对3-碘对氨基苯磺酸产率的影响,结果见表7。

表7 溶剂种类对3-碘对氨基苯磺酸产率的影响
由表7可见,以水为溶剂时3-碘对氨基苯磺酸的产率达到最高为90.05%。换用其它溶剂时,3-碘对氨基苯磺酸的产率都会降低,这可能是由于碘酸钾在水中溶解度较大且冰醋酸在水溶液中有更好的效果。由此确定以水为溶剂。
2.8 溶剂用量对3-碘对氨基苯磺酸产率的影响
固定无水对氨基苯磺酸用量为0.008 mol,碘化钾的量为1.4 g,温度保持70~80 ℃,氧化剂碘酸钾用量为1.05 g并分两次间隔半小时加入,反应4 h,加入冰醋酸4 mL,以水为溶剂,考查溶剂的不同用量对3-碘对氨基苯磺酸产率的影响,结果见表8。

表8 溶剂的量对3-碘对氨基苯磺酸产率的影响
由表8可见,溶剂水的用量为30 mL时,3-碘对氨基苯磺酸的产率达到最高为90.05%。因此溶剂用量以30 mL为宜。
3 产品检测
在TENSOR37傅立叶红外光谱仪上做产品的红外光谱图,主要吸收峰有:499.95 cm-1为C-I键伸缩振动频率;1 546.76 cm-1为S=O双键的伸缩振动频率;1 453.67 cm-1,1 632.23 cm-1和1 600.15 cm-1为苯环骨架振动频率;829.26 cm-1和689.32 cm-1是三取代苯环的特征吸收频率;1 155.91 cm-1是C-N的伸缩振动。
4 结论
以无水对氨基苯磺酸作为底物,碘化钾为碘代试剂,碘酸钾为氧化剂,以水作溶剂合成了3-碘对氨基苯磺酸,最佳反应条件为(以对氨基苯磺酸用量为0.008 mol为基准):反应温度为70~80 ℃,氧化剂用量为1.05 g(分两次间隔半小时加入)、反应时间为4 h、冰醋酸用量4 mL,30 mL水为溶剂,在此条件下,3-碘对氨基苯磺酸的产率可达90.05%。该碘代方法具有环境污染少、产物与反应物易分离、产品后处理简单、产率高等优点,具有良好的应用前景。
[1]AMEGADZIE A K, BECKJ P, GARDINIER K M, et al. Preparation of thiazolopyridinones as MCH receptor antagonists for treating and preventing symptoms assocd with obesity and related diseases: WO, 2006066174[P]. 2006-06-06.
[2]SATO M, MOTOMURAT, ARAMAKIH, et al. Novel HIV1 integrase inhibitors derived from quinolone antibiotics[J]. J. Med. Chem., 2006, 49(5): 1506-1508.
[3]许丹红,孙楠,胡宝祥,等.碘代芳烃的合成研究[J].浙江工业大学学报,2008,36(1):20-21.
[4]李辉,高永民.3,5-二碘水杨酸合成新工艺[J].精细与专用化学品,2009(11):21-22.
[5]陈红艳,吴兆民.一氯化碘乙酸溶液对芳香化合物碘化的研究[J].山西师大学报,2003,17(3):43.
[6]杨桂春,陈祖兴,黄锦霞等.载氯化磷树脂的制备及其对活泼芳香化合物的碘化研究[J].有机化学,2000,20(1): 98-101.
[7]李龙章,马美玲,谢明贵.4-碘苯氧乙酸合成方法的改进[J].四川大学学报(自然科学版),1995,32(6):752-754.
[8]李绮云,曾昭钧,刘巧云.碘化酚合成工艺条件考察[J].中国药物化学杂志,2002,4(4):286-288.
[9]王华.去活化芳香化合物的电解-碘化反应初探[J].惠阳师专学报,1988(1):56-57.
[10]毕维笳.合成5,7-二氯吲哚类化合物的新方法[D].天津:天津大学,2007.
(责任编辑、校对:琚行松)
Studies on the Synthesis of 3-Iodine Sulfanilic Acid Using Potassium Iodate as Oxidant
SUN Tao1, MENG Qing-zhao1, DONG Yu-huan1, LIU Xing-shun2
(1. Department of Chemistry, Tangshan Teachers College, Tangshan 063000, China; 2. Group of Chemistry, Qian’an Xia Guanying Senior High School, Qian’an 064409, China)
Sulfanilic acid and potassium iodide are used as raw materials and potassium iodate is used as the oxidant in order to get 3-iodine sulfanilic acid, and a number of factors were studied during the synthesis of 3-iodine sulfanilic acid. The result shows that the yield of 3-iodine sulfanilic acid is 90.05% under the optimum operation conditions that, the temperature is between 70 ℃ and 80 ℃, the amount of anhydrous sulfanilic acid is 0.008 mol and the amount of acetic acid is 4 mL, the oxidant is 1.05 g, the reaction time is 4 hour, the solvent is water with the amount of 30 mL.
sulfanilic acid; potassium iodide; potassium iodate; 3-iodine sulfanilic acid
TQ031.7
A
1009-9115(2012)05-0011-03
2012-03-20
孙涛(1977-),男,河北唐山人,实验师,研究方向为有机化学。

