双水相萃取法分离生活污水中重金属离子和机理研究
刘玉玲,卓 馨,陈红玲
(宿州学院 自旋电子与纳米材料安徽省重点实验室培育基地,安徽 宿州 234000)
双水相萃取法分离生活污水中重金属离子和机理研究
刘玉玲,卓 馨,陈红玲
(宿州学院 自旋电子与纳米材料安徽省重点实验室培育基地,安徽 宿州 234000)
研究了生活污水中铅(II)、铁(III)、铬(III)、锰(II)等金属离子在聚乙二醇(PEG)-Na2SO4-邻苯二酚紫(PV)体系中的萃取行为。探讨了萃取酸度、萃取剂用量、硫酸铵浓度对金属离子萃取率的影响。实验结果表明,通过控制一定的条件,可以实现铬(III)、铅(II)与部分混合金属离子之间的萃取分离。
重金属离子;聚乙二醇;邻苯二酚紫;萃取分离
含有多种有害重金属离子的生活污水排入江河,会对水体产生严重污染,对环境和人类造成很大危害。传统的污水处理方法有化学沉淀法、电解法、氧化还原法、离子交换法、生物吸附法等,这些方法对处理含有高浓度重金属离子的工业废水能达到一定效果,而用于处理重金属离子浓度较低的生活污水时,就存在着运行费用和原材料成本相对较高的问题。利用水溶性高聚物水溶液在无机盐存在条件下可分为两相的性质,选择常见的有机试剂作为萃取剂,实现部分金属离子间的定量萃取分离[1-4],该方法不使用挥发性有机溶剂,具有分相速度快、安全无毒、操作简单等特点。本文研究了生活污水中铅(II)、铁(III)、铬(III)、锰(II)金属离子在聚乙二醇(PEG)-Na2SO4-邻苯二酚紫(PV)体系中两相间的分配行为。通过控制一定的条件,实现了铬(III)、铅(II)与部分混合金属离子之间的萃取分离。
1 实验部分
1.1 仪器与试剂
TU1201双光束扫描紫外分光光度计(北京通用仪器有限公司);722型分光光度计;pHS-3C精密酸度计(上海雷磁仪器厂);116R型恒温水浴锅。
PV溶液:3.250×10-4mol·L-1;金属标准溶液:按文献[5]配成40 mg·L-1;PEG溶液:300 g·L-1,缓冲溶液:pH1.0~2.5(用HCl配制),pH3.0~6.5(用HAc-NaAc配制),pH7.5~13.0(用氨水-NH4Cl配制)。试剂为分析纯或优级纯,水为二次蒸馏水。
1.2 实验方法
分别在60 mL分液漏斗中,加入不同pH值的缓冲溶液5.0 mL,PV溶液1 mL和一定量的金属离子溶液,加水至10 mL,加入PEG溶液10 mL,硫酸钠2 g,振荡2~3 min,静置。待分层清晰后,过量的PV及金属络合物进入上层PEG相,弃去下层水相,保留上层PEG萃取相。另取一分液漏斗,除不加金属离子外,按上述步骤进行,得试剂空白萃取相。以试剂空白萃取相作参比,用PAR做显色剂的光度分析法测定残留金属离子量[6],根据加入量计算出金属离子萃取率(E%)。
2 结果与讨论
2.1 金属离子萃取条件的选择
2.1.1 酸度对金属离子萃取率的影响
根据实验方法,固定其它条件(金属离子20 μg),改变溶液酸度,分别测定酸度对铅(II)、铁(III)、铬(III)、锰(II)萃取率的影响,结果如图1。

图1 酸度对萃取率的影响
Mn(II)在研究酸度范围内萃取率较低,几乎不被萃取;Pb(II)在pH4.5~8.5、Fe(III)在pH4.5~7.5萃取率都较高(在95%以上),可认为被定量萃取到PEG相;而Cr(III)在pH3.5~8.5范围内,萃取率在50%~66%之间。同一金属离子,溶液的酸度影响其与萃取剂形成的络合物形态、稳定性及表面电荷等,从而影响高聚物相对金属离子的萃取,因此可借控制溶液酸度,实现金属离子之间的定量分离。
2.1.2 萃取剂用量对金属离子萃取率的影响
按实验方法,固定溶液pH值,其他条件不变,改变PV的用量,分别测定萃取剂用量对几种金属离子萃取率的影响,结果如表1。由表1可以看出,不加萃取剂,金属离子的萃取率很低,说明简单金属离子本身难被PEG相萃取,只有与萃取剂形成络合物才有可能被PEG相萃取,当萃取剂用量在1~2.0 mL时各种金属离子萃取率都最高,说明在此范围金属离子与PV之间达到合适络合比;PV量少时金属离子络合不完全,而PV过量会使金属络合物稳定性降低,都会减少金属离子萃取率,所以本实验选择萃取剂用量为1.0 mL。

表1 PV用量对萃取率的影响(E %)
2.1.3 盐析剂的用量对金属离子萃取率的影响
按实验方法,固定溶液酸度(萃取率最大时的pH值)和PV用量,其他条件不变,改变硫酸钠用量,分别测定盐析剂的用量对金属离子萃取率的影响。实验结果表明,当硫酸钠用量少于2.0 g时,溶液不分层或萃取不完全,萃取率低;而盐析剂的用量在2.2~3.5 g时,萃取率最高。硫酸钠用量再增大时,由于盐效应增强,影响配合物的稳定性,使吸光度有所下降。所以本实验选择盐析剂的加入量为2.5 g。
2.2 混合离子的分离
按实验方法进行实验,在pH4.5时,铬(III)可从铬(III)、铅(II)、铁(III)、锰(II)混合离子中分离,pH3.5时,锰(II)可从锰(II)、铅(II)、铁(III)、铬(III)混合离子中分离,结果见表2和表3。

表2 Cr(II)在混合溶液中分离结果(pH=4.5)
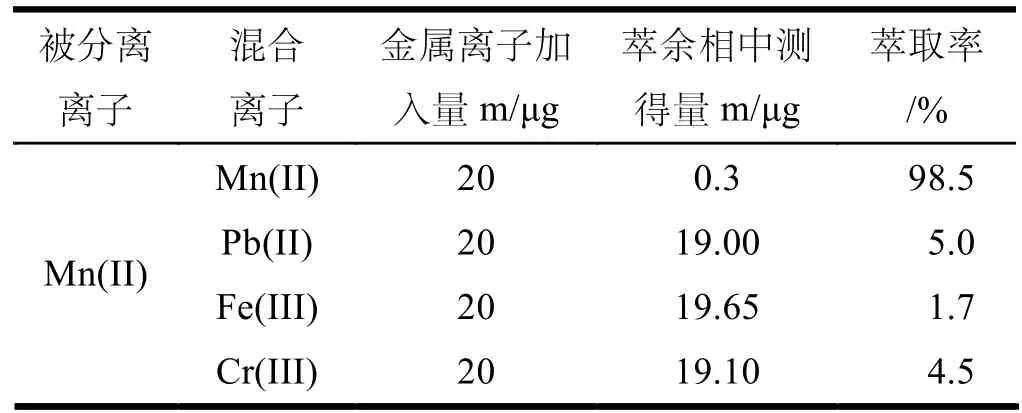
表3 Mn(II)在混合溶液中分离结果(pH=3.5)
3 结论
试验结果表明,生活污水中铁(III)在pH4.0~7.0范围内可以被PEG相几乎完全萃取,铬(III)在pH1.0~7.0、锰(II)在pH1.0~4.5则不被萃取。从而实现将铬(III)(pH3.5)、铁(III)(pH5.0)与铬(III)、铁(III)混合离子的定量分离。
[1]邓凡政,石影,李霞,等.从混合离子中分离Fe、Al、Cd[J].
应用化学,1997,14(1):68.
[2]邓凡政,石影,刘延美.PEG-Na2SO4-PAR体系中Pd(II), U(VI),Mo(VI)的萃取分离[J].光谱学与光谱分析,2000, 20(3):440.
[3]邓凡政,石颖,汪玉波,等.双水相体系中钛,锆的分离[J].稀有金属,2001,25(6):471.
[4]蔡红,张春莉,许秀丽,等.光度法研究聚乙二醇-硫酸铵-邻苯三酚红体系中铋,铁,铜,镍,钴,铅的萃取分离[J].光谱学与光谱分析,2003,23(2):345.
[5]杭州大学化学系分析化学教研室.分析化学手册:第三分册[M].北京:化学工业社,1989:439.
[6]Z·马欣科.郑用熙,任奇钰,冯艺聪,等译.元素的分光光度测定[M].北京:地质出版社,1983:211,180,370,484.
(责任编辑、校对:琚行松)
Study on Extraction Separation of Heavy Metal Ions in Wastewater with Visible Spetrophotometry
LIU Yu-ling, ZHUO Xin, CHEN Hong-ling
(Anhui Key Laboratory of Spin Electron and Nanomaterials (Cultivating Base), College of Suzhou, Suzhou 234000, China)
The distribution behavior of the two alternates of Pb(II), Fe(III), Cr(III), Mn(II) metal ion in sewage in the polyethylene glycol(PEG)-((NH4)2SO4)- pyrocatechol violet (PV) system was studied. The effect of the solution acidity, the amount of the extractant and the (NH4)2SO4concentration on the degree of extraction rate of metal ions was investigated.Through the control of certain conditions, extraction and separation of the Cr(III), Pb(II) and part of the mix between metal ions was realized.
heavy metal; polyethylene glyeol (PEG); pyrocatechol violet; separation extraction
O652.62
A
1009-9115(2012)05-0014-02
安徽省教育厅自然科学重点项目(KJ2011Z369),宿州学院科研平台开放课题(2011YKF04),高校省级自然科学研究项目(KJ2011B174),宿州学院一般项目(2011yyb14)
2012-06-04
刘玉玲(1967-),女,安徽宿州人,实验师,研究方向为分析化学。
——酸度

