2010年12月FDA安全警告
2012-05-17 09:55
药学与临床研究 2012年3期
阿瓦斯汀(贝伐单抗)删除治乳癌适应症 12/16/2010
FDA提醒医生和患者将建议取消阿瓦斯汀(Avastin,贝伐单抗)治疗乳腺癌的适应症,因为没有证据表明这种治疗方法是安全有效的。该药品并没有被撤出市场,并且这个决定不会即刻影响该药用于治疗乳腺癌,同时也不会影响该药品用于治疗结肠、肾、脑和肺的癌症。
FDA的上述决定是在审查了4个关于阿瓦斯汀治疗妇女乳腺癌的临床研究后作出的。研究数据显示该药品并没有延长乳腺癌患者的生存期,相对于该药品的风险而言,其在减缓乳腺癌发展方面也没明显益处。4个研究中没有一个能证明患者接受阿瓦斯汀治疗后可以延长生存期,相反会显著增加严重副反应。这些风险包括严重高血压,流血和出血,鼻、胃、肠等穿孔,心脏病发作或者心力衰竭。
2 关键词:Anzemet(甲磺酸多拉司琼) 心律失常 12/17/2010
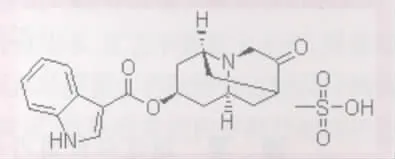
FDA提醒医生一个禁忌症正在被添加到Anzemet(甲磺酸多拉司琼)注射剂的处方信息中:甲磺酸多拉司琼不再用于预防小儿和成人患者由于癌症化疗引起的恶心和呕吐(CINV)。新的数据显示Anzemet注射剂有导致尖端扭转型室速(一种心律失常)的风险,在某些情况下可能致命。有心脏病或者有心率或心律问题的患者特别危险。Anzemet会产生剂量依赖性心电图 QT、PR及 QRS间隔延长。结构如图。
3 关键词:重组人生长激素(生长激素) 可能增加死亡风险12/22/2010
FDA告知公众,来自法国的一项 “生长激素与健康”(SAGhE)的研究发现,在儿童期和随后较长时间以重组人生长激素(recombinanthuman growth hormone)治疗某些种类矮小症(特发性生长激素缺乏症、先天性或妊娠身材短小)的患者,其死亡风险与法国普通人群相比有小幅增高。FDA目前正在审查关于潜在风险的所有可用资讯,一旦完成审查将立即与公众沟通。
猜你喜欢
中国典型病例大全(2022年9期)2022-04-19
中国医院用药评价与分析(2022年1期)2022-02-21
家教世界·创新阅读(2022年1期)2022-02-19
南方周末(2021-02-04)2021-02-04
天津医科大学学报(2021年1期)2021-01-26
健康之家(2019年3期)2019-12-14
阅读(快乐英语高年级)(2019年3期)2019-09-10
健康必读·下旬刊(2019年5期)2019-06-03
中国计算机报(2018年16期)2018-10-08
小学生·多元智能大王(2014年5期)2014-07-24