天然楮果色素提取工艺的优化
李 洋,李海亮,张 媛,李 琳,钦传光
(西北工业大学生命学院,陕西 西安 710072)
随着科技的发展和人民生活水平的提高,人们对色素安全问题日益重视。人工合成色素因具有毒性[1],应用受到限制,尤其是在食品、药品、化妆品等行业;而来自自然界的天然色素因无毒副作用,产销量逐年增长[2],2005年天然色素的产量已达10 680 t[3]。目前,我国允许使用的食用天然色素有40多种[4],开发利用无毒副作用的天然色素已成为色素产业的发展趋势。
楮果(BroussonetiapapyriferaL.Vent.)是桑科构树属植物构树的果实,在我国民间用作中药材。楮果橙红色素色泽鲜艳、性质稳定、安全性好[5],且构树适应性强,在我国分布广泛,来源充足。因此,楮果色素具有潜在的工业实用价值和经济价值,适合作为天然色素进行大规模生产和应用研究。徐子婷等[6]探讨了用纯水作溶剂的提取工艺条件,但采用纯水作溶剂进行提取时,楮果富含的可溶性成分如果胶、糖类、蛋白质等也同时被大量地提取出来,严重干扰分析结果,并且对色素的进一步精制和纯化带来不利影响,步骤繁琐,成本和能耗较高。
为此,作者在此以乙醇为溶剂从楮果中提取色素,测定了楮果色素的最大吸收波长及pH值稳定性,优化了提取工艺条件,拟为开发利用楮果色素资源奠定基础。
1 实验
1.1 材料、试剂与仪器
新鲜的成熟楮果,七月份采摘于西安地区,塑料袋(桶)封装,冷藏备用。
无水乙醇、36%盐酸、氯化钾、甘氨酸、磷酸氢二钠、柠檬酸、氢氧化钠均为分析纯。
不同pH值的缓冲溶液(mol·L-1):
pH值1:盐酸+氯化钾(0.04+0.05);
pH值3:甘氨酸+盐酸(0.05+0.0114);
pH值5:磷酸氢二钠+柠檬酸(0.103+0.0485);
pH值7:磷酸氢二钠+柠檬酸(0.1647+0.01765);
pH值9:甘氨酸+氢氧化钠(0.05+0.0088);
pH值11:甘氨酸+氢氧化钠(0.05+0.052)。
U-3310型紫外可见分光光度计,日本日立公司;PB-10型pH计,德国Sartorius公司;N-1001型旋转蒸发仪、SB-2000型水浴锅,日本东京理化器械株式会社。
1.2 方法
1.2.1 楮果色素的提取
选取新鲜、成熟的楮果,去核,按料液比1∶30(g∶mL,下同)加入80%(体积分数,下同)乙醇,室温浸提4 h;浸提液用滤纸过滤除去残渣后,置于旋转蒸发仪在30 ℃水浴减压蒸馏,得到浓缩液;低温避光保存。
1.2.2 楮果色素最大吸收波长的测定
将楮果色素浓缩液用80%乙醇稀释5倍,使吸收波长位于紫外可见分光光度计的线性范围内,在200~800 nm扫描,测定楮果色素的最大吸收波长。
1.2.3 楮果色素pH值稳定性的考察
取0.2 mL楮果色素浓缩液,分别用不同pH值的缓冲溶液稀释10倍,在200~800 nm扫描,测定楮果色素的pH值稳定性(以相应缓冲溶液作参比)。
1.2.4 楮果色素提取的单因素实验
1.2.4.1 乙醇体积分数对浸提效果的影响
称取5 g去核楮果,分别浸于50 mL 0%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%的乙醇中,40 ℃浸提2 h,过滤,于485 nm下测定吸光度进行比较。
1.2.4.2 料液比对浸提效果的影响
称取2 g去核楮果,与80%乙醇分别按料液比1∶10、1∶15、1∶20、1∶25、1∶30、1∶35、1∶40、1∶45、1∶50混合,40 ℃浸提2 h,过滤,于485 nm下测定吸光度进行比较。
1.2.4.3 浸提时间对浸提效果的影响
称取2 g去核楮果,与80%乙醇按料液比1∶35混合,于40 ℃分别浸提1 h、2 h、3 h、4 h、5 h,过滤,于485 nm下测定吸光度进行比较。
在工程项目管理当中应用价值工程分析方法,可以将其作为整体系统,对项目进行功能性分析,还可以创造和评价方案,详细分析用户所需功能。因此,从某种意义上看,价值工程得本质在于采用低成本获得高性能的建设项目。其次,价值工程主要在于功能性分析,所以在项目具体实施期间需要全面分析工程的功能性。由于价值工程借助集体智慧实现,所以属于一项具备领导组织的活动。
1.2.4.4 浸提温度对浸提效果的影响
称取2 g去核楮果,与80%乙醇按料液比1∶35混合,分别于20 ℃、30 ℃、40 ℃、50 ℃、60 ℃、70 ℃浸提2 h,过滤,于485 nm下测定吸光度进行比较。
1.2.5 楮果色素提取的正交实验
在单因素实验的基础上,采用正交实验进一步研究楮果色素的最优提取工艺条件。选择浸提温度、浸提时间、料液比、乙醇体积分数为考察因素,进行L16(44)正交实验,其因素与水平见表1。

表1 正交实验的因素与水平
2 结果与讨论
2.1 楮果色素的最大吸收波长
楮果色素在80%乙醇中的紫外可见吸收光谱如图1所示。

图1 楮果色素的紫外可见吸收光谱
由图1可看出,楮果色素的可见光区最大吸收波长为485 nm。由比尔定律可知,吸光度与色素浓度成正比,因此本实验采用485 nm处的吸光度间接表示色素浓度。
2.2 楮果色素的pH值稳定性
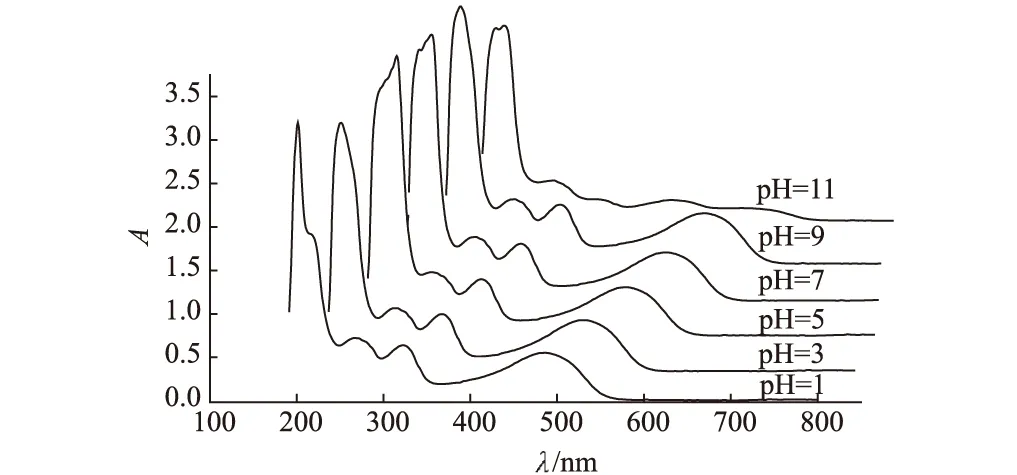
图2 楮果色素在不同pH值缓冲溶液中的紫外可见吸收光谱
由图2可看出,楮果色素在pH值 1、3、5、7、9的缓冲溶液中均稳定存在,分子结构没有发生变化;而在pH值为11的缓冲溶液中的吸收光谱变化较大。表明楮果色素在pH值1~9的溶液中稳定性良好。
2.3 楮果色素提取的单因素实验结果
2.3.1 乙醇体积分数对浸提效果的影响(图3)
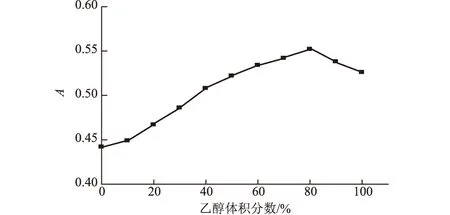
图3 乙醇体积分数对浸提效果的影响
由图3可知,乙醇体积分数达到80%时,吸光度最大、浸提效果最好;其次为70%和90%乙醇。这是因为,乙醇体积分数较低时,会在提取过程中引入部分果胶、糖类、蛋白质等杂质,增大色素纯化难度,增加成本。因此,选择80%左右乙醇作浸提液,既可减少色素浸提液中的杂质含量,又能方便色素浸提液浓缩及回收乙醇。
2.3.2 料液比对浸提效果的影响(图4)

图4 料液比对浸提效果的影响
由图4可知,料液比在1∶35时,吸光度最大、浸提效果最好。这是因为,料液比较高(溶剂用量较少)时,色素溶出量少,浸提效果差;料液比过低(溶剂用量过多)时,溶出的杂质相应增多[7],增大了后续浓缩工作量。因此,料液比选择1∶35左右较为适宜。
2.3.3 浸提时间对浸提效果的影响(图5)
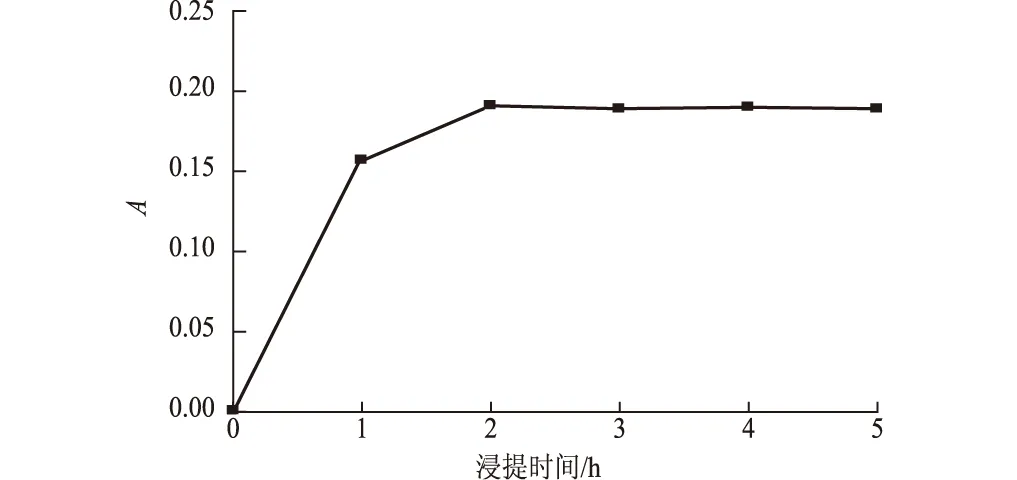
图5 浸提时间对浸提效果的影响
由图5可知,浸提时间短于2 h,色素浓度随时间的延长逐渐升高;2 h后色素浓度趋于平稳,不再升高。因此,浸提时间选择2 h左右较为适宜。
2.3.4 浸提温度对浸提效果的影响(图6)

图6 浸提温度对浸提效果的影响
由图6可知,浸提温度为40 ℃时,吸光度最大、浸提效果最好;继续升高温度,吸光度略有降低。因此,浸提温度选择40 ℃左右较为适宜。
2.4 楮果色素提取的正交实验结果(表2)

表2 正交实验结果与分析
由表2可知,各因素对楮果色素浸提效果的影响大小依次为:乙醇体积分数>浸提温度>浸提时间>料液比,其中乙醇体积分数对楮果色素浸提效果的影响最大,料液比对提取效果的影响最小。最优提取工艺条件为A3B2C3D3,即80%乙醇作浸提液、料液比1∶35(g∶mL)、浸提时间2 h、浸提温度40 ℃。
以料液比为误差,在α=0.10水平进行方差分析,结果见表3。

表3 正交实验方差分析(α=0.10)
由表3可知,因素D差异有显著性。
3 结论
在乙醇溶液中,楮果色素在可见光区的最大吸收波长为485 nm,并在pH值为1~9的溶液中具有良好的稳定性。通过单因素实验和正交实验确定楮果色素的最优提取工艺条件为:以80%乙醇作浸提液、料液比1∶35(g∶mL)、浸提温度40 ℃、浸提时间2 h。为大规模开发利用天然楮果色素资源奠定了基础。
参考文献:
[1] 李家玉,王海斌,林志华,等.合成色素的危害及其分析方法[J].中国园艺文摘,2009,25(10):165-167,178.
[2] 李崇瑛,王安,杨涛,等.食用天然色素的纯化与研究进展[J].中国调味品,2007,(9):18-22,38.
[3] GB 2760-2011,食品添加剂使用标准[S].
[4] 卢雪华,成坚,白卫东.我国食用色素工业的现状及对策[J].中国调味品,2010,35(5):35-39.
[5] 钦传光,丁焰,张湘潇.楮果色素的提取和性质研究[J].食品与机械,1998,(5):33-34.
[6] 徐子婷,周文美.楮果色素提取条件的研究[J].安徽农业科学,2010,38(27):14946-14947,14960.
[7] 陈合,李世玉,舒国伟,等.黄姜色素提取条件的研究[J].陕西科技大学学报(自然科学版),2009,27(4):52-54,72.

