硫化氢在磷酸溶液中溶解度的实验研究
黎铉海,卢渝文,张燕娟,文衍宣
(广西大学化学化工学院,广西南宁530004)
硫化氢在磷酸溶液中溶解度的实验研究
黎铉海,卢渝文,张燕娟,文衍宣
(广西大学化学化工学院,广西南宁530004)
摘 要:在用过量的五硫化二磷净化磷酸的工艺中,为确定五硫化二磷的最佳投加量和净化的工艺条件,采用气相单循环法,测定了常压下不同温度和不同硫化氢分压下硫化氢气体在磷酸溶液中的溶解度数据。结果表明,在实验范围内,硫化氢的溶解度随温度的升高和磷酸浓度的增加而降低,随硫化氢分压的增加而增加,且呈线性关系,符合一般气体的溶解度规律。用I.H.Cho模型对溶解度数据进行了关联和计算,关联式的显著性水平达0.01,实验值与理论值的平均偏差为1.60%。该结果对磷酸的净化工艺有一定的指导意义。
关键词:硫化氢;磷酸溶液;磷酸净化;溶解度
在热法磷酸的净化过程中,通常用加入过量五硫化二磷(P2S5)的方法,利用其在磷酸溶液中产生的硫化氢(H2S)与磷酸中的金属离子反应,生成难溶的金属硫化物沉淀,经过滤后达到净化的目的[1-2]。但过量的H2S不但导致资源浪费,还会造成环境污染、增加企业成本。为准确计算P2S5的投加量,必须确定H2S在磷酸中的溶解度,但这方面的数据未见报道。虽然可用相近体系溶解度的方法计算,但偏差较大。因此,根据目前磷酸净化的工艺条件,测定和关联常压下H2S气体在磷酸溶液中的溶解度数据,对磷酸净化的生产工艺有一定的参考价值。
1 实验部分
1.1 实验原料及分析方法
实验所用磷酸为食品级磷酸(广西越洋化工有限公司),按要求配成不同浓度的磷酸溶液。实验前先对其进行真空搅拌脱气处理。H2S气体由肇庆市高能达化工有限公司提供,纯度为99.9%。
H2S在磷酸和气相中含量的测定均采用定量取样法。用一定浓度的NaOH溶液将其转化成非挥发性物质后,用亚甲蓝分光光度法测定样品中的硫化物含量,然后计算出H2S的溶解度及其对应的分压。
1.2 实验装置与测定过程
测定气液平衡的方法有静态法、循环法和流动法。气体溶解度测定的困难往往在于对气液两相取样时,容易破坏已有的平衡而导致误差。在参照和比较前人研究[3-6]的基础上,根据现有磷酸净化的工艺条件和实验条件,采用气相单循环法来测定H2S在磷酸溶液中的溶解度,实验装置如图1所示。

图1 H2S溶解度测定原理示意图
先用真空法对系统进行气密性实验,并对液相取样恒流泵和气相取样管进行标定。将一定浓度的磷酸试样置于三口烧瓶中,打开恒温搅拌系统,溶液达设定的温度并稳定后,关闭液封装置阀门,将系统抽至一定的真空度。通入H2S气体,至系统压强接近大气压强时,开启液封装置阀门和气相循环系统。通过观察液封装置的液位差来调节H2S的加入量,使系统始终稳定在与大气相同的压力下3~4 h。当液封装置的液位差恒定不变时,即可认为气液两相达到平衡。此时,关闭气相取样管两端的阀门,获得一定体积的气相样品,并通过二级NaOH溶液吸收装置将其转变为非挥发性的Na2S。与此同时,启动液相取样恒流泵,取少量液相样品(约1mL)并用NaOH溶液吸收。吸收瓶吸收前后的质量之差即为所取样品的质量。分别对气液相样品定容,利用亚甲蓝分光光度法分析样品中硫化物的浓度,即可获得不同实验条件下H2S的溶解度数据。
2 结果与讨论
2.1 实验装置的可靠性检验
为了检验实验装置的可靠性,以水为溶剂,用相同的方法测定了101.19 kPa时H2S在水中的溶解度(x,%),并与文献[7]的测定值比较,如表1所示。由表1可知,实验所得的实验数据与文献[7]的结果比较吻合,平均偏差约为1.57%,说明该装置所测定的溶解度数据可用于计算误差≤2%的工业设计。

表1 H2S在水中溶解度的测定值与文献值比较
2.2 H2S分压对溶解度的影响
图2为在体系总压为101.19 kPa、磷酸浓度为85.3%(质量分数)的条件下,不同平衡温度时H2S气体分压(p)对溶解度的影响。由图2可知,H2S在磷酸溶液中的溶解度均随平衡分压的增大而增大,表明H2S在磷酸中的溶解过程是物理溶解比较显著的过程,且有较好的线性关系,与亨利定律较为吻合。在工业生产中,在相同条件下提高体系压力可增加H2S在磷酸中的溶解度,更有利于磷酸中金属离子的净化。
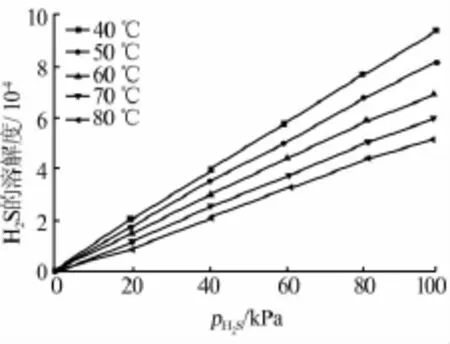
图2 不同分压下H2S在85.3%磷酸溶液中的溶解度
2.3 温度对溶解度的影响
图3为在体系总压为101.19 kPa、H2S的平衡分压为80.41 kPa时,温度对H2S溶解度影响。由图3可知,在磷酸浓度和气体分压相同的条件下,H2S的溶解度随着温度的升高而减小,基本呈线性关系。这表明H2S在磷酸溶液中的溶解是放热过程,升高温度会降低其溶解量。因此在磷酸净化工艺中,需在较低温度下才能确保净化效果。

图3 不同平衡温度下H2S在磷酸溶液中的溶解度
2.4 磷酸浓度对溶解度的影响

图4 H2S在不同浓度磷酸中的溶解度
图4为在体系总压为101.19kPa、H2S的平衡分压为40.10kPa的条件下,不同温度下磷酸浓度对H2S溶解度的影响。由图4可知,当平衡温度相同时,H2S的溶解度随着磷酸浓度的增加而减小。由于相对水分子来说磷酸是大分子物质,混合溶液与纯水相比,对H2S的排斥作用更加强烈,故在相同条件下其在磷酸溶液中的溶解度比在纯水中小。根据实验结果,磷酸在低浓度净化时比高浓度净化时更有利。
2.5 溶解度的关联
气体溶解度属于气液平衡范畴,常用的关联和计算方法有亨利系数法、非对称活度系数法和状态方程法等,但它们的计算复杂,需要的物性参数较多。从工程应用角度出发,学者们提出不少气体溶解的模型,如吕秀阳模型[8]、周金汉模型[9]和I.H.Cho模型[10]等,这些模型具有参数简单、无明显物理意义和方便计算等特点。采用上述模型对实验的数据进行关联、比较和方差分析,结果发现I.H.Cho模型关联H2S在磷酸溶液中的溶解度数据时,显着性水平可达0.01,其方差分析见表2,其关联式为:
ln x=a1ln p+α/(T+a)+a4ln w+a5
式中:x为H2S的物质的量分数,%;p为H2S的气体分压,Pa;T为温度,℃;w为磷酸的质量分数,%;a1~a5为模型参数,与平衡温度、分压和磷酸浓度无关。经数据拟合,各参数分别为:a1=0.948、a2=1.908、a3=-94.977、a4=-0.853、a5=1.666。

表2 方差分析表
用上述关联式对H2S在不同条件下的溶解度进行计算,并与实验测定值进行比较,结果如图5所示。经比较发现,计算值与理论值的平均偏差为1.60%,能够满足工业设计计算的要求。

图5 H2S溶解度的计算值与实验值比较
3 结论
1)常压下用气相单循环法测定H2S气体在磷酸中溶解度的方法是可行的,用水作溶剂时,所得的实验数据与文献值比较吻合,平均偏差约为1.57%,表明实验装置是可靠的。2)H2S气体在磷酸中的溶解度与温度、压力和磷酸浓度有关,它随H2S分压的增加而增大,随温度和磷酸浓度的增加而减小,呈线性变化,符合一般气体在液相中的溶解度规律。3)用I.H.Cho模型对H2S在磷酸溶液中的溶解度数据进行关联,其关联式的显著性水平达到0.01,计算值与实验值平均偏差为1.60%,可用于指导磷酸净化的工艺计算。
参考文献:
[1] 骆德池.浅谈连续热法食品磷酸生产[J].贵州化工,2005,30(4):43-45.
[2] 黄平,李军,尤彩霞.净化精制磷酸深度脱氟研究[J].无机盐工业,2008,40(11):4-6.
[3] 艾宁,李保红,陈健,等.CO2在碳酸二甲酯溶剂中溶解度的测定[J].化学工程,2005,33(3):51-54.
[4] 焦真,骆培成,吴有庭,等.低分压CO2在有机胺水溶液中的溶解度[J].化学工程,2006,34(9):43-46.
[5] Fonseca IM A,Almeida JPB,Fachada H C.Automated apparatus forgassolubilitymeasurements[J].J.Chem.Thermodynamics,2007,39(10):1407-1411.
[6] Jou F Y,Mather A E.Solubility of hydrogen sulfide in[bmim][PF6][J].International Journal of Thermophysics,2007,38(2):490-495.
[7] 刘光启,马连湘,刘杰.化学化工物性数据手册无机卷[M].北京:化学工业出版社,2002,84-85.
[8] 吕秀阳,吴兆立,侯虞钧.一个气体在液体中溶解度的关联式[J].化学工程,1993,21(6):69-71,76.
[9] 周汉金,王成习.二氧化碳在乙醇水溶液中的溶解度[J].化学工程,1996,24(1):63-67,75.
[10] Cho IH,Cho D L,Yasuda H K,et al.Solubility of propylene in aqueoussilver nitrate[J].JChem.Eng.Data,1995,40(1):102-106.
联系方式:xuanhli@gxu.edu.cn
中图分类号:TQ125.12
文献标识码:A
文章编号:1006-4990(2012)02-0030-03
收稿日期:2011-08-19
作者简介:黎铉海(1958— ),男,博士,教授,博士生导师,主要从事无机盐和湿法冶金的教学和科研工作,已公开发表文章90多篇。
Study on solubility of H2S in phosphoric acid solution
LiXuanhai,Lu Yuwen,Zhang Yanjuan,Wen Yanxuan
(SchoolofChemistry and ChemicalEngineering,GuangxiUniversity,Nanning 530004,China)
Abstract:In order to determine the optimum dosage of P2S5and technological conditions in purification processofphosphoric acid by using excessive amountP2S5asgenerating agent,the solubility data ofH2S in phosphoric acid wasmeasured by single gas circlemethod in different temperatures and H2S partial pressures under atmospheric pressure.Results showed that the solubility of H2S decreased with increasing temperature and concentration of phosphoric acid,but increased with increasing the partial pressure of H2S.The data had linear relationship and agreed with normal gas solubility rule.Solubility data were related and calculated by using I.H.Chomodel and the significance level of correlation reached 0.01.The average deviation between experimentaland calculated valueswas1.60%.The resultshave a guiding significance for the purification technology ofphosphoric acid.
Keywords:H2S;phosphoric acid solution;phosphoric acid purification;solubility

