CMC稳定的Ni/Fe双金属催化体系的制备及对PCB77原位脱氯降解
刘长光,赵 林,丁 舒,谭 欣,,余舜雷
(1.天津大学化工学院,天津 300072; 2.天津大学环境科学与工程学院,天津 300072)
多氯联苯(PCBs)是一类含有1~10个氯原子的化合物,能够形成209种可能的同属化合物。原子共面的多氯联苯是多氯联苯同属化合物中的一部分,其具有极高的引发酶变异的潜在可能性,如酶CYP1A1[1]。PCB77(3,3’,4,4’-四氯联苯)是原子共同面多氯联苯中的一种,由于在1979年以前被广泛的应用,在环境中可以很容易检测到它的存在。由于其自身的高稳定性和对有机物高亲和性,极难被降解且易在生物体内富集,严重威胁环境和生物圈的安全。如何高效的降解环境中的多氯联苯的方法成为近年来的热门研究课题。
在过去的10年中,0价纳米铁(NZVI)在降解含氯的有机化合物的过程中扮演着越来越重要的角色。在处理地下水和沉淀物中氯化化合物的过程中,0价纳米铁显示出高效的降解效率。降解反应机理如下[2]。
2Fe0→2Fe2++4e-
(1)
3H2O→3H++3OH-
(2)
2H++2e-→H2(g)
(3)
RCl+H++2e-→RH+Cl-
(4)
虽然0价纳米铁在有机氯化化合物的降解去除过程中的作用越来越显著,但是已经证实它对一些稳定的氯化化合物的脱氯降解存在一些不足之处。多氯联苯就是其中的一种。比如多氯联苯的去除效率非常低[3],0价纳米铁容易被氧化,在表面形成铁的氧化物和氢氧化物会严重的影响它的活性。为了解决这些问题,0价铁的表面被引入了痕量的第二金属形成纳米双金属体系,例如镍,铜和钯等。纳米铁充当电子给体,而镍、铜等则扮演电子受体的角色[4],可以加速纳米铁的腐蚀放出氢气,起到加速氯化化合物的催化降解的作用。此外第二金属的出现还能很好的防止纳米铁暴露在空气的时候被氧化。
纳米双金属体系一定程度上保护0价纳米铁不被氧化,加速催化降解的效果,并且双金属纳米体系的高比表面积决定了其具有优异的催化活性,这在一定的程度上减少了贵重金属催化剂的应用。然而由于范德华力和磁性力的普遍存在,纳米颗粒会很快的趋于团聚[5-6],导致纳米粒在很短的时间内失去其具有高的化学反应活性和高的流动性,这一技术壁垒限制了0价纳米铁在工业界的广泛应用。为了降低纳米粒的团聚效应,在纳米铁制备的过程中引入了一种稳定剂,将其附着在纳米粒的表面以达到降低团聚的目的。采用聚丙烯酸(PAA)作为一种新型的稳定剂,发现PAA提高了纳米粒在土壤中的可运输性[7]。最近,一种环境友好的可食用的化合物羧甲基纤维素钠(CMC)被用于制备高稳定性和分散性的0价纳米铁,并可通过调节CMC和亚铁离子的比例很好的控制制备所得0价纳米粒的粒径[8]。羧甲基纤维素钠是纤维素衍生物的一种,该高分子聚合物分子内含有相当数量的羧基基团和大量的羟基基团,这些基团可以与0价纳米铁之间形成很强的相互作用[9]。
目前铁的纳米双金属颗粒已经被广泛的应用于多氯联苯的降解,但用羧甲基纤维素钠作稳定剂稳定的CMC-Ni-Fe纳米双金属体系的制备和降解PCB77都未曾被报道。本研究通过正交试验,以PCB77降解率为指标,考察了催化体系中不同CMC与铁的用量比、镍化率以及制备温度对制备纳米双金属颗粒的影响,确定最适宜的工艺条件,并对其进行了分析。
1 试剂和方法
1.1 药品试剂
无水乙醇、七水合硫酸亚铁、氯化镍和硼氢化钠,均为分析纯,天津市科密欧化学试剂有限公司;PCB77,GC/MS,J&K Scientific中国有限公司(CAS 32598-13-3);羧甲基纤维素钠(CMC,M.W.=90 k,degree of substitution D.S.=0.7)。
1.2 CMC-Ni-Fe纳米双金属颗粒的制备
羧甲基纤维素钠稳定的镍铁纳米颗粒的制备参考湿法制备0价纳米铁技术[8]并加以改进。试验在不同温度下,在配有机械搅拌和氮气保护装置250 mL的四口烧瓶中进行。往四口烧瓶中分别加入70 mL的不同质量分数的羧甲基纤维素钠溶液和10 mL新配置的0.2 mol/L硫酸亚铁溶液,并氮气保护下搅拌15 min以形成稳定的CMC-Fe2+的螯合物。然后按照n(BH4-)/n(Fe2+)为2∶1的比例逐滴滴加适量的硼氢化钠溶液。反应为:
Fe(H2O)62++2BH4-→Fe↓+2B(OH)3+7H2↑
(5)
当四口烧瓶中不再有氢气放出后,继续搅拌10 min,确保亚铁离子被还原成0价铁。随后滴加适量的0.03 mol/L氯化镍溶液,制备不同镍化率的催化颗粒。镍离子在0价纳米铁表面被还原成0价的镍,形成纳米镍铁双金属颗粒。
Ni2++Fe0→Fe2++Ni↓
(6)
制备的纳米颗粒分别用去离子水和无水乙醇清洗,去除其中残留的化合物,重复操作2次。将所得纳米双金属颗粒储存于4 ℃乙醇中以用于PCB77降解试验。
1.3 PCB77的降解试验
往60 mL锥形瓶中加入50 mL初始浓度为5 mg/L PCB77溶液(体积比为50%的乙醇和水混合溶液)。用制备的CMC-Ni/Fe双金属颗粒对PCB77进行降解。通入氮气,用量为3 g/L。排出锥形瓶中上部空隙中的空气。试验在转速为180 r/min,温度(30±1) ℃的水浴摇床上进行。在预先设计好的取样时间间隔点取样,用注射器从封闭的锥形瓶中取出1 mL的样品,置于10 mL的离心管,用1 mL的正己烷萃取。 震荡5 min,随后在5 000 r/min下离心2 min。收集上层有机相。重复萃取操作3次。充分混合3次萃取的有机相,从中取出1.5 mL在30 ℃下烘干。加入0.5 mL的正己烷溶解烘干的PCB77,在4 ℃下保存。
1.4 分析方法
采用带有电子捕获检测器Hewlett Packard (HP, USA) 6890N气相色谱仪(GC/ECD)对样品中的PCB77进行分析。A BD-5柱(J&W scientific Inc., China) 规格30.0 m×0.32 mm×0.25 μm。每次的进样量为1 μL。载气的流量为1.5 mL/min。注入温度250 ℃,检测器温度270 ℃。烘箱的温度保持在150 ℃持续1 min,以10 ℃/min的速率升至200 ℃,然后5 ℃/min升至280 ℃。最后280 ℃保存2 min。
采用日本D/max2500X-射线粉末衍射仪检测CMC-Ni-Fe的晶型。电压和电流分别为40 kV和100 MA。
CMC-Ni/Fe双金属纳米颗粒的电子显微镜图片和粒度分布分别用扫描电镜(SEM)和粒度分析仪检测。
2 结果与讨论
2.1 CMC-Ni/Fe纳米双金属颗粒制备条件优化
以对PCB77的降解率为指标,考察CMC与Fe的质量比(A),反应温度(B)以及加入m(Ni)/m(Fe)(C),即加入硫酸盐铁中铁的含量与加入的氯化镍中镍的含量的比值,3个因素对PCB77降解的影响。由于指标较多,全部操作试验量大,故通过正交试验进行优化,确定CMC-Ni/Fe双金属体系制备的最适宜条件。
降解率=[1-(取样样品中PCB77浓度)/
(PCB77的初始浓度)]×100%
试验因素与水平如表1 所示。
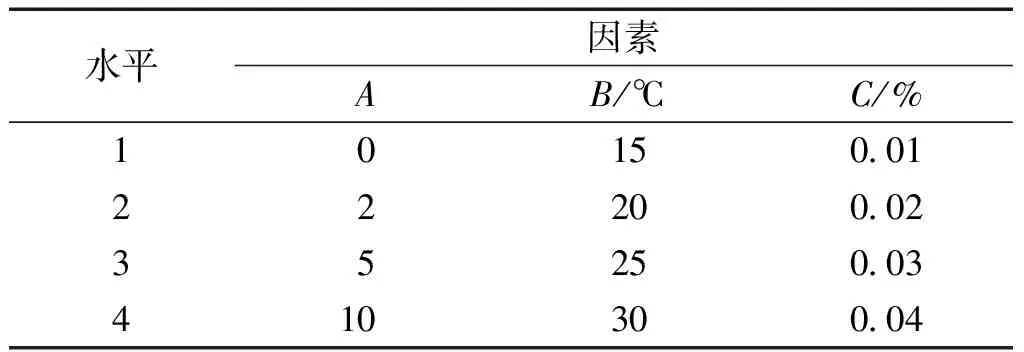
表1 正交试验因素水平表
表2为30 ℃温度下,不同配比的Ni/Fe双金属体系对PCB77进行48 h的降解后,PCB77的降解率。
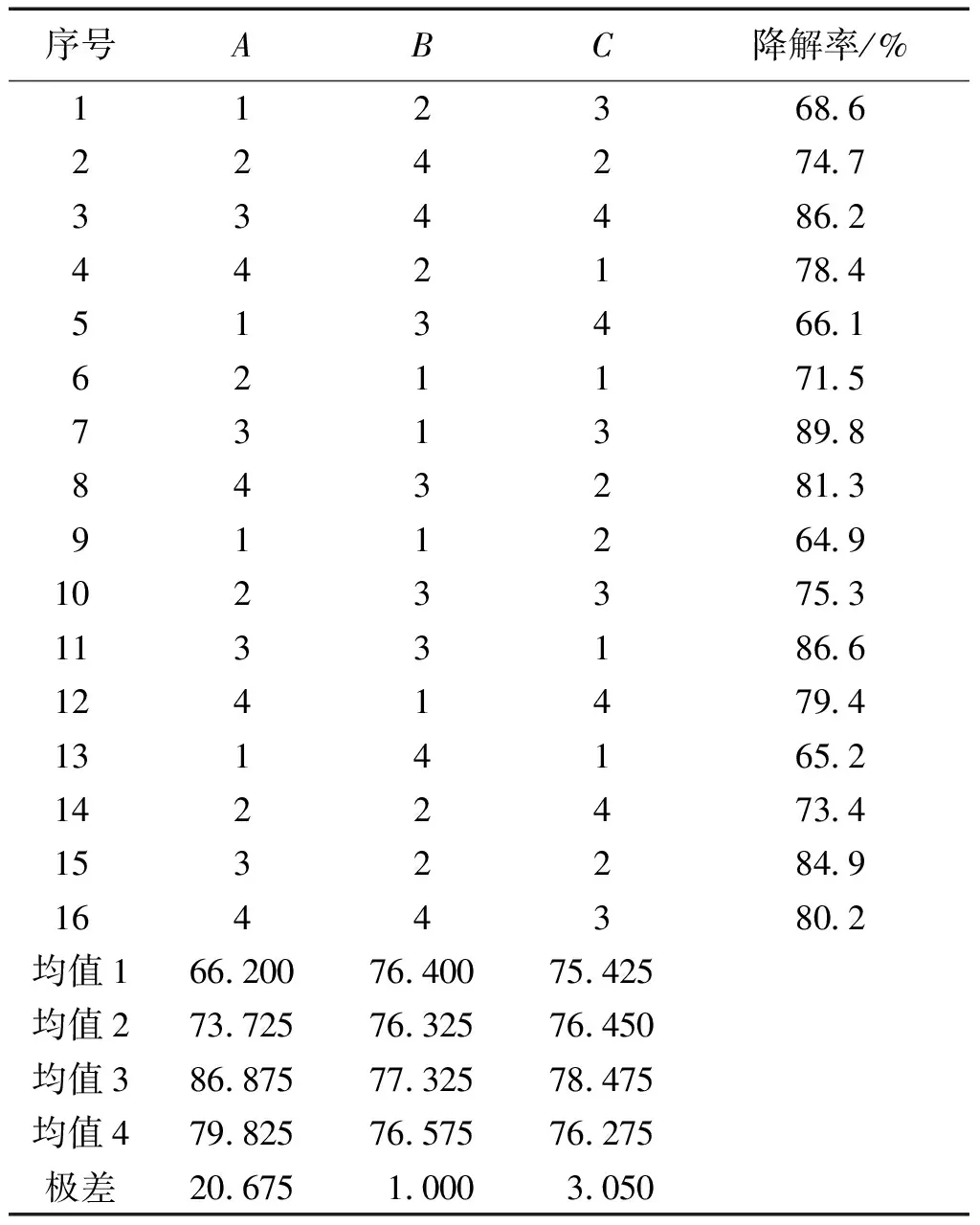
表2 正交试验结果
对表2进行分析,表观上可以看出制备CMC -Ni/Fe纳米双金属颗粒的最适宜条件是A3B3C3。
可以看出A因素(CMC与Fe的质量比)的极差RA最大为20.675,是影响PCB77降解的主要因素。随着CMC加入,降解率先升高,在m(CMC)/m(Fe)=5时达到最高,其后CMC加入的量在增加则降解率由有所下降。这可能是由于加入的CMC分子中含有一定数量的COO-基团,可以与溶液中的Fe2+螯合,有效地防止还原过程中因范德华力和磁力引起的团聚,形成较小粒径的纳米颗粒,从而增加活性位点。开始时溶液中的Fe2+离子过量,只有部分发生螯合,形成小颗粒,随CMC增加,CMC分子中的COO-恰好跟Fe2+完全发生螯合,此时完全形成小颗粒,活性位点达到最高,降解活性也达到最高。继续增加CMC的量,则溶液中过量的COO-与铁发生螯合,在纳米颗粒表面分散,增大了PCB77靠近纳米颗粒的空间位阻,出现降解率下降的现象。
其次为镍的加入量RC=3.050,随着镍的加入量增加,也出现降解率先增大后减小的现象,这可能是因为加入的镍在铁的表面形成一层镍层,开始只有部分覆盖,加速电子传递,达到加速降解的效果。随着镍的加入量增加,镍化层变厚,影响到纳米铁跟PCB77接触,出现降解速率变慢的现象。
温度的影响最小RB=1.000,可能是因为温度低,CMC与Fe2+的螯合过程比较慢,未能充分利用CMC中的COO-。温度太高,可能导致纳米颗粒因范德华力和磁力作用团聚,降低活性。
A3B3C3该组数据没有在正交试验表中出现,故制备该组催化颗粒及对应的无CMC的镍铁双金属体系,并对PCB77进行降解。降解结果如图1所示。
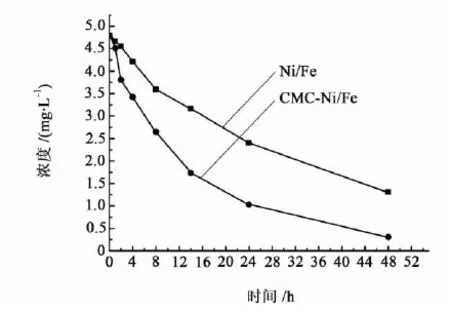
图1 PCB77的浓度随时间的变化Fig.1 Reduction of PCB77 by Ni-Fe and CMC-Ni/Fe bimetallic nanoparticles
经过48 h的降解,CMC-Ni/Fe纳米双金属体系对PCB77的降解率达到94%,而没有加稳定剂CMC,镍化率相同的Ni/Fe双金属体系的降解率只有71%左右。加入CMC的体系纳米颗粒的活性显著提高。这可能是由于加入稳定剂CMC后制备的纳米颗粒变小,活性位点增多的缘故。对数据进行分析,降解过程符合一阶指数模型。
2.2 粒径分布与扫描电镜分析
对样品进行了粒径分布和扫描电镜分析,结果见图2和图3。
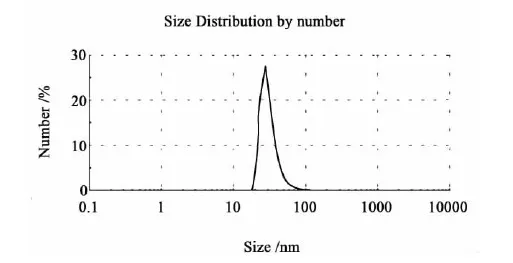
图2 CMC-Ni/Fe纳米双金属颗粒的粒径分布图Fig.2 Size distribution of CMC-stabilizer Ni-Fe bimetallic nanoparticles

图3 扫描电镜图:a)分散在乙醇中的CMC-Ni/Fe纳米双金属颗粒;b)干燥的CMC-Ni/Fe双金属纳米颗粒;c)干燥的Ni/Fe纳米颗粒Fig.3 SEM pictures:a)CMC-Ni/Fe bimetallic nanoparticles dispersed in ethanol; b) dried CMC-Ni-Fe bimetallic nanoparticles;c)dried Ni/Fe bimetallic nanoparticles
如图2所示,CMC-Ni/Fe纳米双金属颗粒的粒径分布比较均匀,分布范围为18~90 nm,主要集中在23.94 nm。图3c干燥的Ni/Fe双金属颗粒的粒径大约在100 nm左右。体系中加入CMC后,平均粒径明显减小,说明CMC的加入确实减小了纳米颗粒的粒径。
如图2所示,CMC-Ni/Fe纳米双金属颗粒的粒径分布比较均匀,颗粒小。这可能是因为羧甲基纤维素钠分子中含有相当数量的羧基基团,可以捕捉溶液中的亚铁离子,形成稳定的CMC-Fe2+;此外CMC还含有大量的羟基基团,同样起到捕捉亚铁离子的作用。该效应可以有效地阻止亚铁离子被还原成单质铁的过程中,因纳米微粒之间范德华力和磁力所引起的团聚效应,从而有效地控制纳米颗粒粒径。
图3为不同形态的纳米双金属体系扫描电镜图。从图3中可以看出,图3a)为分散在乙醇中的纳米双金属颗粒,具有规整的颗粒形状,粒径大约有60 nm左右,明显大于其平均粒径23.94 nm。图3b)所示为干粉纳米双金属颗粒,具有规整的球形形貌,粒径大约为120 nm。比分散在乙醇中的粒径大。图3c)所示为干燥的Ni/Fe纳米双金属颗粒粒径在100 nm左右。
图3a)现象可能是因为在收集CMC-Ni/Fe的过程中,有一定数量的羧甲基纤维素钠跟随纳米双金属颗粒一起沉淀下来。虽然用去离子水和无水乙醇清洗2次,但是仍有部分羧甲基纤维素钠残留。当CMC-Ni/Fe双金属颗被分散在乙醇中时,由于羧甲基纤维素钠不溶于乙醇,在表面张力的作用下羧甲基纤维素钠链状结构收缩,在纳米Ni/Fe表面形成了一层的羧甲基纤维素钠壳层。从而导致CMC-Ni/Fe双金属体系粒径变大。
图3b)粒径为120 nm左右,大于没加CMC的Ni/Fe双金属颗粒粒径100 nm。可能是因为干粉扫面电镜表征时,CMC-Ni/Fe双金属颗粒经过研磨过程,由于较强的外力的作用,使得多个覆盖有羧甲基纤维素钠壳层的纳米双金属颗粒被挤压在一起,形成一个粒径较大的颗粒,从而导致其粒径比没有加CMC的镍铁双金属颗粒粒径还要大。虽然其表观粒径有所增大,但是可以看出并没有发生明显团聚,同时由于CMC分子在水中的溶解度很大,其收缩的链状结构会在溶液中分散开来,颗粒变小。而Ni-Fe纳米双金属颗粒由于其明显的团聚效应,丧失大量活性位点,虽然颗粒比干燥的CMC-Ni-Fe纳米双金属颗粒小,故其降解效率依然要低很多。
2.3 XRD衍射分析
图4所示的为CMC-Ni/Fe双金属纳米颗粒的衍射图。

图4 CMC-Ni/Fe双金属纳米颗粒的衍射图Fig.4 XRD of CMC-Ni/Fe bimetallic nanoparticles
由图4可看出,在2θ=44.9° 的位置出现1个响应峰,此峰为纳米铁的衍射峰[10]。图4中并没有出现Fe2O3或者 Fe3O4的衍射峰,说明纳米铁并没有被氧化。65.0°所对应的α-Fe0的(200)位面也未被检测到[11],这可能是由于纳米铁的表面被CMC包裹住,导致对此峰没有响应。镍所对应的衍射峰同样没有被检测出来,这可能是因为含量太低造成的。
3 结论
主要以CMC作为稳定和分散剂,研究了制备羧甲基纤维素钠稳定的纳米镍铁双金属体系的最适宜条件,并对其应用性能进行了研究,得到如下结论。
1)通过正交试验,以PCB77降解率为指标,考察了CMC与Fe的质量比,加入m(Ni)∶m(Fe),以及制备温度对纳米双金属颗粒制备的影响。对制备过程中的反应参数进行优化,确定最适宜条件为:m(CMC)/m(Fe)=5,m(Ni)/m(Fe)=0.03,制备温度25 ℃。m(CMC)/m(Fe)为主要影响因素,其次为m(Ni)/m(Fe),制备温度影响最小。
2)通过粒径分析仪,扫描电镜和XRD检测,结果表明合成的颗粒为集中在23.94 nm的CMC稳定的纳米镍铁颗粒。镍在XRD检测中没有被检测出来,这可能是因为含量太低的缘故。
3)通过制备的双金属纳米体系对PCB77进行降解实验。发现CMC-Ni/Fe对PCB77显示出非常高的降解活性。经48 h降解,有94%的PCB77被去除。
参考文献:
[1]VENKATACHALAM K,ARZUAGA X,CHOPRA N,etal.Reductive dechlorination of 3,3′,4,4′-tetrachlorobiphenyl (PCB77) using palladium or palladium/iron nanoparticles and assessment of the reduction in toxic potency in vascular endothelial cells[J].Journal of Hazardous Materials,2008,159(2/3):483-491
[2]VARANASI P,FULLANA A,SIDHU S.Remediation of PCB contaminated soils using iron nano-particles[J].Chemosphere,2007,66(6):1 031-1 038
[3]DEVOR R,CARVALHO-KNIGHTON K,AITKEN B,etal.Mechanism of the degradation of individual PCB congeners using mechanically alloyed Mg/Pd in methanol[J].Chemosphere,2009,76(6):761-766
[4]SMULEAC V,BACHAS L,BHATTACHARYYA D.Aqueous-phase synthesis of PAA in PVDF membrane pores for nanoparticle synthesis and dichlorobiphenyl degradation[J].Journal of Membrane Science,2010,346(2):310-317
[5]RAYCHOUDHURY T,TUFENKJI N,GHOSHAL S.Aggregation and deposition kinetics of carboxymethyl cellulose-modified zero-valent iron nanoparticles in porous media[J].Water Research,2012,46(6):1 735-1 744
[6]PHENRAT T,SALEH N,SIRK K,etal.Aggregation and sedimentation of aqueous nanoscale zerovalent iron dispersions[J].Environmental Science & Technology,2007,41(1):284-290
[7]ZHOU H,HUA J,ALIBAIG S,etal.Dechlorination of 2,4-dichlorophenoxyacetic acid by sodium carboxymethyl cellulose-stabilized Pd/Fe nanoparticles[J].Journal of Hazardous Materials,2011,198:7-12
[8]DONG T,LUO H,WANG Y,etal.Stabilization of Fe-Pd bimetallic nanoparticles with sodium carboxymethyl cellulose for catalytic reduction of para-nitrochlorobenzene in water[J].Desalination,2011,271(1/3):11-19
[9]CAO J,XU R,TANG H,etal.Synthesis of monodispersed CMC-stabilized Fe-Cu bimetal nanoparticles for in situ reductive dechlorination of 1,2,4-trichlorobenzene[J].Science of the Total Environment,2011,409(11):2 336-2 341
[10]FANG Z,QIU X,CHEN J,etal.Debromination of polybrominated diphenyl ethers by Ni/Fe bimetallic na noparticles:Influencing factors, kinetics, and mechanism[J].Journal of Hazardous Materials,2011,185(2/3):958-969
[11]ZHENG Z,YUAN S,LIU Y,etal.Reductive dechlorination of hexachlorobenzene by Cu/Fe bimetal in the presence of nonionic surfactant[J].Journal of Hazardous Materials,2009,170(2/3):895-901

