低参数超声乳化治疗晶状体半脱位白内障患者临床观察△
王 乐 陈 伟 邵 毅 叶向彧 毛益辉
晶状体悬韧带在本身因素或直接(间接)外力等作用下,均可发生离断,造成晶状体半脱位。部分由外伤、青光眼、葡萄膜炎、先天性因素等导致晶状体半脱位的白内障患者,由于容易造成晶状体悬韧带断离,可使晶状体坠入玻璃体内,并可由多种原因引起青光眼而危及视力,给手术带来很大难度。随着白内障超声乳化吸出手术技巧的不断提高,尤其是特殊类型白内障手术技术的不断丰富,临床治疗白内障的手术适应证不断拓宽,并在实践中取得了较为满意的效果。目前白内障超声乳化手术一般采用高参数设置,即高负压、高能量比、高流速,其手术安全性及有效性得到广泛认同。但伴有晶状体半脱位的白内障中,如采用高参数设置,将对晶状体悬韧带产生较大二次损伤,不利于术后人工晶状体植入、视力恢复等[1]。而如果采用低参数设置进行手术,晶状体悬韧带压力减轻,提高了手术安全性,术后恢复快、人工晶状体居中性好,无明显并发症发生[2]。为探讨Infiniti低参数设置(Alcon公司)对晶状体半脱位性白内障治疗的有效性和安全性,我们采用前瞻性临床研究方法对2010年3月至2011年6月在厦门眼科中心白内障科确诊的10例晶状体半脱位性白内障患者进行低参数超声乳化手术,现将结果报告如下。
1 资料与方法
1.1 一般资料 收集我院2010年3月至2011年6月收治的白内障患者1856例,术前检查裸眼视力、最佳矫正视力、眼压、角膜屈光状态、角膜内皮计数、角膜地形图、眼部B超、IOLmaster等,其中晶状体半脱位患者17例(17眼),男11例(14眼),女6例(3眼);年龄52.3~78.5(65.4±15.3)岁。17例患者中确诊为白内障伴晶状体半脱位10例10眼,其中男7例,女3例,年龄47.0~68.0(59.3±6.7)岁。白内障程度按照 Emery核硬度分级标准进行分级[3]。具有外伤史和青光眼手术史者7眼,马凡综合征患者2眼,剥脱综合征1眼。术前裸眼视力:数指~0.02者2眼,0.03~0.1者5眼,0.1~0.2者3眼;散瞳验光:最佳矫正视力≤0.2者7眼,≥0.3者3眼;眼压为9.2~17.1 mmHg(1 kPa=7.5 mmHg)。散瞳检查晶状体脱位情况:晶状体半脱位位于颞上侧者2眼,颞下侧者3眼,鼻下侧者2眼,鼻上侧者3眼;散瞳检查晶状体脱离范围:脱位范围90°~180°者8眼、脱位范围<90°者2眼。6眼在脱位的晶状体与睫状沟之间可见细而密的晶状体悬韧带;2眼晶状体赤道部向中心凹陷呈缺损畸形;马凡综合征患者眼底均表现为高度近视的视盘颞侧弧形斑和纹理状视网膜改变。所有晶状体半脱位均位于后房。术前排除晶状体半脱位以外的手术禁忌证。
1.2 手术方法 术前常规准备,采用球后、球旁麻醉。于角膜曲率最大方位选择上方或颞侧行角膜缘隧道切口入前房,主切口顺时针3个钟点方位角膜缘内1 mm做辅助切口,前房内注入黏弹剂(应用Alcon公司的DiscVisc以及Bausch&Lomb的透明质酸钠软壳技术)。在晶状体脱位范围中央做晶状体前囊膜小瓣,使用撕囊镊将晶状体前囊膜小瓣向左右方向分别进行具有对抗力的连续环形撕囊,直径约5.5 mm,水分离晶状体核。进入Infiniti超声乳化程序,OZIL扭动模式,采用低参数设置(瓶高75 cm,负压150 mm-Hg,流速20 mL·min-1,能量30%~80%),原位超声乳化吸出混浊的晶状体[4];术中应用chop钩对抗囊袋牵拉张力以保护囊袋及减轻悬韧带张力[5]。然后植入囊袋张力环(直径13 mm)以稳定囊袋[6],进入I/ A程序(瓶高70 cm,负压250~400 mmHg,流速20 mL·min-1),吸出残留皮质。向前房及囊袋内注入眼内黏弹剂,采用人工晶状体推注器植入人工晶状体(Alcon:SA60AT)于囊袋内。人工晶状体目标屈光为正视。清除眼内黏弹剂。根据情况采用不同方法关闭手术切口。术后地塞米松静脉输液,局部妥布霉素地塞米松、普拉洛芬眼液滴眼等处理。手术均由同一经验丰富术者实施。本研究所涉及的全部研究方法均遵循《赫尔辛基宣言》,符合医学伦理学原则,并获得南昌大学医学院医学伦理委员会批准。全部受试患者均签署知情同意书。
1.3 观察指标 术后观察患者视力、最佳矫正视力、眼压、人工晶状体位置、角膜内皮细胞计数等。随访时间为3~6个月。
2 结果
2.1 治疗一般情况 10例患者手术均按计划顺利摘出了晶状体,术中无一例核或皮质坠入玻璃体内,操作时晶状体稳定,操作顺利,消除了晶状体坠入玻璃体内的危险。所有患者均一期植入人工晶状体。治疗3~6个月后,患者视力有显著提高,人工晶状体居中性良好,治愈率达100%。
2.2 治疗前后各项检测指标评定结果 患者治疗前及术后1个月的视力、眼压及角膜内皮计数情况见表1,由表1可以看出:术后未矫正远视力(uncorrected distance visual acuity,UCDVA)、最佳矫正远视力(best corrected distance visual acuity,BCDVA)较治疗前明显改善;患者视力从术前的数指/眼前~0.2 (UCDVA)及数指/眼前~0.6(BCDVA)提高到术后6个月的0.05~1.0(UCDVA)及0.1~1.0(BCDVA)。患者术前与术后眼压无明显差异,未出现高眼压等严重并发症。患者术后角膜内皮细胞计数均较治疗前有所减少,但术后角膜内皮细胞丢失率低,术后3 d为(9.87±2.72)%,术后1个月为(9.53±2.59)%,术后6个月为(9.91±3.19)%。
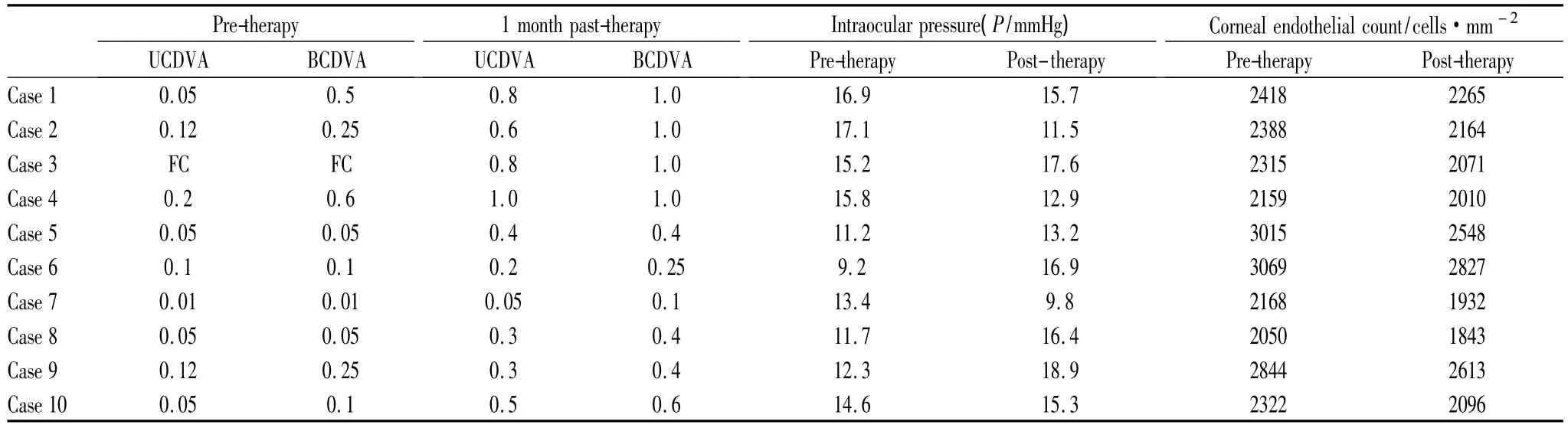
表1 患者治疗前及术后1个月的视力、眼压及角膜内皮细胞计数情况Table 1 Visual acuity,intraocular pressure and corneal endothelial cells count before and at 1 month after therapy
2.3 并发症 患者在术后未见明显角膜水肿、前房反应、眼压升高、黄斑水肿等严重并发症。术后裂隙灯显微镜下观察人工晶状体居中性好,未发现人工晶状体明显偏心、角膜内皮失代偿等并发症。
3 讨论
晶状体脱位在临床上并不少见。晶状体脱位的原因有先天性及后天性,先天性晶状体脱位常见于发育不良的马凡综合征、同型胱氨酸尿症、Marchesani综合征及Ehlers-Danlos综合征,后天性晶状体脱位分外伤性和自发性,外伤性晶状体脱位常伴外伤性白内障形成,自发性晶状体脱位是由于眼内病变引起悬韧带机械性伸长,如牛眼、葡萄肿、玻璃体条索牵引,眼内肿瘤推挤,眼内炎症或变性所致。
晶状体脱位的治疗方法因脱位晶状体所处位置的不同而异[7]。传统的手术方法是前路大切口囊内或囊外摘出,包括冷冻、硅胶、晶状体圈匙或塑料滑板,其结果是伤口大,术中、术后并发症多,诸如玻璃体大量丢失,玻璃体与切口广泛粘连,继发青光眼、黄斑囊样水肿、视网膜脱离及瞳孔改变等。常规白内障超声乳化吸出术对硬核处理由于能量较大,容易损伤角膜内皮等。
低参数白内障超声乳化吸出术的出现和逐步完善提前推进了屈光性白内障手术时代的到来,不仅解决了前房稳定性差的问题,还减少了手术切口,有利于控制眼压和浅前房的发生。采用低参数超声乳化技术取出脱位的晶状体,整个手术过程中眼压控制良好,类似闭合性玻璃体切割,手术切口小,前房稳定性好,并发症明显减少[8]。本研究采用低参数来评价手术方案前后一系列检测指标差异,探讨一种更完美的、能够重建或恢复眼正常生理功能和屈光状态的个性化白内障手术模式。
目前手术参数常规采用高参数设置(高流量、高负压、高灌注、高能量),高效快速处理不伴有晶状体半脱位白内障,然而对于伴有晶状体半脱位的白内障而言,高参数设置可能存在以下风险:(1)更大的囊袋张力,从而导致晶状体悬韧带二次损伤;(2)黏弹剂吸除过快,缺乏对角膜内皮保护;(3)前房浪涌现象明显等。而低参数超声乳化技术的主要优点是:(1)前房扰动小,减少术中浪涌现象、浅前房及玻璃体脱出几率;(2)降低黏弹剂吸除速度,有效保护角膜内皮;(3)缓慢粉碎晶状体核,增加手术安全性; (4)低灌注压减少对晶状体悬韧带张力,减少悬韧带二次损伤。超声乳化吸出半脱位晶状体需要手术技巧相对较高,本研究采用超声乳化吸出半脱位的晶状体,术中采用低参数设置(低流量、低负压、低灌注、低能量),低流量及低负压具有更稳定的浅前房,低灌注减少对囊袋压力,避免玻璃体脱出前房[9-10]。而此手术的关键及手术技巧有:(1)晶状体半脱位超声乳化时,水分离核应充分,尽力将核娩出囊袋,防止再行超声致囊袋受力不均,从而扩大脱位面积; (2)晶状体核前、后面注入黏弹剂,即充分保护角膜内皮及晶状体囊袋,也可阻止部分玻璃体脱出;(3)对于晶状体核硬度较小者,超声乳化粉碎应主要依靠强有力的吸引力,以明显缩短手术时间;(4)根据晶状体核硬度,控制术中超声能量,手术中最高输出超声能量设定为55%~60%,实际输出超声能量为25%~35%;(5)术中应综合眼部情况决定人工晶状体植入方式、类型和时期。本研究中10例患者悬韧带离断范围<180°,随访发现植入囊袋张力环效果显著,而离断范围过大者宜行囊内摘出而不主张施行张力环植入[11-12]。
综上所述,随着白内障手术观念的转变,手术技巧、手术设备的不断改进与完善以及相关眼科光学检查与评价技术的迅速发展,超声乳化仪参数设计与白内障患者的关系越来越密切。本研究发现,在年龄较轻的、无严重的角膜水肿、葡萄膜炎或玻璃体混浊的晶状体半脱位合并白内障患者中,低流量、低负压、低灌注超声乳化技术联合囊袋张力环及后房型人工晶状体植入是可行的,能减轻术后炎症反应,并可获得较好的术后视力。
1 Tjia K.Unexpected IFIS cases:what should you do[J]?Cataract Refract Surg Today,2009,4(3):54-55.
2 Salehi-Had H,Turalba A.Management of traumatic crystalline lens subluxation and dislocation[J].Int Ophthalmol Clin,2010,50(1):167-179.
3 张志辉.同级硬核白内障超声乳化术两种能量模式的应用观察[J].眼科新进展,2009,29(4):294-296.
4 薛文娟,宋旭东,闫 岩,杨文利,钱 进.先天性晶状体半脱位手术治疗临床研究[J].中国实用眼科杂志,2010,28(6):615-618.
5 Waiswol M,Kasahara N.Lens subluxation grading system:predictive value for ectopia lentis surgical outcomes[J].Einstein,2009,7(1):81-87.
6 Richard S,Hoffman I,Howard Fine,Mark Packer.Primary anterior chamber intraocular lens for the treatment of severe crystalline lens subluxation[J].J Cataract Refract Surg,2009,35 (10):1821-1825.
7 Johansson C.Optimizing vacuum settings in torsional phacoemulsification employing lower vacuum setting with torsional facilitates the use of microincision surgery[J].Cataract Refract Surg Today,2008,3(4):24-27.
8 宋念东,宋旭东.囊袋内张力环植入治疗中重度晶状体半脱位临床研究[J].眼科新进展,2010,30(9):860-862.
9 李文超,刘钢生,侯正玉.超声乳化术在外伤性晶状体半脱位中的应用[J].眼外伤职业眼病杂志,2010,32(7):506-507.
10 Suven B.Use of nucleus as temporary capsular tension device to delay capsular tension ring placement in subluxed hard cataract[J].Tech Ophthalmol,2010,8(2):66-68.
11俞晓艺,赵 岐,王 星,林 郁.超声乳化吸出联合人工晶状体植入术治疗晶状体半脱位的技术探讨[J].国际眼科杂志,2009,9 (7):1276-1278.
12 Das P,Ram J,Singh-Brar G,Dogra MR.Results of intraocular lens implantation with capsular tension ring in subluxated crystalline or cataractous lenses in children[J].Indian J Ophthalmol,2009,57(6):431-436.

