经导管主动脉瓣植入术并发症研究进展
徐先增综述 黄 凯审校
(广西医科大学第一附属医院心研所,广西南宁市 530021)
经导管主动脉瓣植入术(transcatheter aortic valve implantation,TAVI)目前已经广泛地应用于严重主动脉瓣狭窄但又不适于传统开胸的主动脉瓣置换的病人。现阶段TAVI仍属于复杂高危介入手术,对各类TAVI相关并发症全面地了解和规避,是安全开展TAVI手术的必要条件。我国开展TAVI的经验不多,而且目前尚未见到有关TAVI并发症的专题阐述,现就国内外相关文献进行汇总,对各类TAVI手术并发症以及相应处理综述如下。
1 TAVI简介
2002年法国医生Cribier报道了首例TAVI病人,虽然术后17周死于非心脏原因,但术后即刻瓣膜功能良好,心功能显著改善[1]。目前TAVI在世界范围内已蓬勃开展,截至目前手术病人已超过5万例。我国则起步较晚,最近国内学者葛均波报道了3例TAVI,初步效果良好[2]。TAVI时支架瓣膜输送途径主要有3种:经股静脉途径、经心尖途径和经股动脉途径,其中经股动脉途径最常应用。目前市场上获得欧盟CE标志认证的TAVI主流输送系统有两种,即Edwards SAPIEN支架释放系统(图1A)和CoreValve支架释放系统(图1B)。Edwards SAPIEN支架释放系统为球囊膨胀瓣膜,由牛心包来源的生物瓣膜附着于可膨胀金属支架,该瓣膜可前向经静脉、逆向经股动脉和经心尖途径置入。CoreValve支架释放系统为自膨胀瓣膜,由猪心包来源的生物瓣膜附着于自膨胀镍钛合金支架而制成,该瓣膜只能逆行经股动脉路径置入,对于此血管路径严重闭塞的患者,可考虑经左腋动脉或锁骨下动脉途径置入。
2 TAVI并发症
2.1 房室传导阻滞 主动脉瓣环与房室传导系统解剖关系毗邻,TAVI的手术期间和术后可以发生不同程度的传导阻滞。置入CoreValve支架系统后不同程度的房室传导阻滞和左束支阻滞发生率均明显增加,心内电生理发现AH和HV间期均较术前延长,最终术后有19%~46%的病人接受了永久起搏器治疗[3,4]。术前存在右束支阻滞、高手术风险积分(logistic EuroSCORE)、室间隔增厚、术前QRS波群宽度、主动脉瓣环偏大、支架置入过深、应用CoreValve支架系统、置入经验不足等均是TAVI术后需要安置永久起搏器的危险因素,而Edwards SAPIEN支架置入系统则不易发生传导阻滞。术中传导阻滞近半数(46%)发生在支架置入前球囊预扩张时,其次依次发生于支架扩张时(29%)、支架定位时(12%)、球囊定位时(6%)和导丝穿过主动脉瓣时(4%)[5]。术后第4天是发生传导阻滞最明显的时期,之后有逐渐恢复的趋势,但出院后1个月仍有发生完全房室传导阻滞的可能性。安置永久起搏器是治疗症状性房室传导阻滞的有效方法,起搏器的安置有近半数发生在术后7 d内,另外有35%和18%的患者发生在术后7 d至30 d和术后30 d以后[6]。
2.2 主动脉瓣返流 引起主动脉瓣返流的原因主要为瓣周漏,极少部分为支架瓣膜撕裂或不能活动。瓣周漏几乎见于所有TAVI术后病人,但多数为轻度(返流程度小于2级),中重度瓣周漏(返流程度大于或等于2级)则见于约20%~40%的术后病人。多因素分析发现,主动脉瓣环偏大、置入水平过低(支架下缘至无冠窦瓣最佳距离应在10 mm左右)、外周血管疾病、左心室流出道至降主动脉角度过大以及严重主动脉瓣膜钙化是术后发生中重度瓣周漏的独立危险因素[7]。一旦发生严重主动脉瓣膜返流,死亡率明显增加。但远期随访结果发现,瓣周漏发生后瓣膜返流程度一般不会增加。发生严重瓣周漏后,可以采取以下几种方法减轻瓣周返流程度:①支架内后扩张(作用效果明显,是最常用的处理技术);②在原支架瓣膜内再次置入支架瓣膜(或称之为“瓣种瓣”技术);③当置入水平过低时可以考虑使用套圈技术,将支架瓣膜拉向近端;④保守方法。瓣膜撕裂或不能活动导致的主动脉瓣膜返流往往会引发严重的血流动力学症状,必须进行补救性地在原瓣膜内再次置入瓣膜[8]。
2.3 冠状动脉开口闭塞 冠状动脉开口闭塞是TAVI的少见并发症(约占1%),但如发生其后果往往是灾难性的,必须及时采取措施,如紧急经皮冠状动脉介入治疗(Percutaneous coronary intervention,PCI),但导引钢丝如不能穿过闭塞冠状动脉开口,则需要进行外科搭桥。Stabile等[9]报道了5例TAVI术后冠状动脉阻塞患者,均为左主干开口受阻,4例成功进行了PCI,1例冠状动脉开口阻塞为一过性,未进行进一步处理。Crimi等[10]也处理了1例类似患者,成功进行急诊PCI后,患者于TAVI后6个月仍然存活。
2.4 支架脱落 Tay等[11]报道了7例支架脱落病人,全部发生在支架释放后即刻,支架脱落后的位置2例位于主动脉弓内近左锁骨下动脉处,2例位于降主动脉左锁骨下动脉开口以远处,3例位于腹主动脉。7例患者中4例在同一次手术中置入第2枚支架,2例患者在第2次手术中置入第2枚支架,1例患者进行了传统外科主动脉瓣置换。所有患者的脱落支架均未进行处理。远期随访(平均随访时间为1 085 d)结果显示,除1例患者死于非相关原因外,其他患者心功能稳定于NYHA分级Ⅰ~Ⅱ级,并且CT检查发现脱落支架内瓣膜持续保持开放状态。
2.5 心包积液和心包填塞 较大样本的临床研究发现,心包积液的发生率为12.8%,心包填塞的发生率大约为2% ~3%,后者是导致术中死亡最常见的原因[12]。TAVI患者均为老年人,心脏脆弱,容易合并穿孔,TAVI中最容易引起心包填塞的步骤是在进输送鞘、置入瓣膜时,加硬导丝在向前的冲力下可刺破左室,另外头端直硬的指头导丝经狭窄主动脉瓣口进入左心室时,亦可使主动脉窦部或者左心室穿孔。我国学者葛均波避免心包填塞的经验是:①将加硬导丝头端塑型,使其在左心室内形成圆圈以减少冲力,进输送鞘管时应固定好加硬导丝;②直头导丝进左心室时,应避免用力过猛,以免主动脉窦部或者左室穿孔;③加硬导丝塑形后应轻柔缓慢送入左心室(经猪尾巴导管送入)[2]。
2.6 卒中 经股动脉TAVI的卒中发生率约为4%,加上一过性脑缺血(Transient ischemic attack,TIA)发作的发生率约为11%。实际上TAVI术中脑的微栓塞相当常见,并且在送入导丝、扩张自体瓣膜、释放支架瓣膜过程中均有微栓塞发生[13]。与经心尖途径相比,经股动脉途径可能可以进一步降低术后卒中的发生率[14]。因此认为TAVI相关的脑卒中是输送系统经过主动脉时损伤主动脉导致主动脉粥样斑块脱落引起的。然而,PARTNER-A研究中[15],经心尖途径与经股动脉的脑卒中发生率相同。因此,有些专家认为脑卒中产生原因还可能为球囊扩张使得主动脉瓣上钙化物质脱落造成。
2.7 血管损伤 包括穿刺部位血管损伤和血管路径损伤,两者均易发生于经股动脉途径,血管损伤后术后30 d死亡率会增加,其发生率与术者经验、股动脉钙化程度和鞘管与股动脉直径比相关[16]。穿刺部位血管损伤相对常见。Kahlert等[17]报道了101例TAVI患者,其中60例采取了经股动脉途径,有19例(占32%)发生了穿刺部位并发症,包括腹膜后血肿(2例)、髂/股动脉夹层(10例)、假性动脉瘤形成(3例)和动脉缝闭装置导致的血管狭窄(6例)。6例患者采取外科干预,8例采取经对侧血管介入治疗,5例采取保守治疗。血管路径损伤(包括主动脉夹层和穿孔)相对少见,但往往更加致命。Alsac等[18]报道了3例沿途大血管损伤,占所有血管损伤的1/3,2例为主动脉夹层,1例为主动脉破裂(最后导致死亡)。Aminian等[19]也报道了1例降主动脉破裂的病例,病人经股动脉途径TAVI后顽固性休克,最后也不治死亡。
2.8 肾功能损伤 TAVI患者有较高的慢性肾功能受损发生率。根据不同的诊断标准,急性肾功能损伤的发生率在10%~70%之间。发生急性肾损伤的独立危险因素包括心肌梗死病史、围手术期输血、术后白细胞计数、高手术风险积分(logistic EuroSCORE)、慢性阻塞性肺病、高血压[20,21]。因为术中要应用对比剂,因此术后有较高的急性肾功能受损发生率,部分患者需要血液透析。对比剂用量大于100 mL的TAVI患者术后肾功能受损更严重,需要血液透析的比率更高,ICU监护时间和住院时间更久,中远期预后更差[22,23]。
2.9 出血 出血是TAVI较常见的并发症,有报道为31%[24],但致命性出血较为少见,仅为4.9% ~8.5%[25,26]。致命性大出血和输血可使TAVI患者在住院期间和术后6个月的死亡率明显增加[25]。
2.10 其他少见并发症 经股动脉途径TAVI可能造成乳头肌断裂,导致二尖瓣大量返流[27]。另外,经心尖途径TAVI则可能导致左心室假性室壁瘤[28]。
3 TAVI并发症导致的死亡
各种TAVI相关并发症均可导致死亡,是发生TAVI并发症最严重的后果。多数文献将其分为术中、术后1个月和术后1年等3个不同阶段,因患者均为超高龄,术后更长时间的随访结果少见。TAVI术中死亡率在2%左右,最常见死亡原因依次为心包填塞(39%)、心力衰竭(21%)、心脏骤停(18%)、血管/出血并发症(18%),主要为心脏相关性死亡[12]。术后30 d死亡率在8% ~10%之间,最常见死亡原因依次包括心衰/多脏器功能衰竭(24%)、猝死/心脏骤停(17%)、血管/出血并发症(17%)、卒中(11%)、脓毒血症(11%)和心包填塞(10%),心脏相关性死亡和非心脏相关性死亡大体相当。经心尖途径和经股动脉途径之间30 d死亡率差别不明显[14],两者死亡构成比包括瓣膜相关性、心脏相关性和非心脏相关性分别为25%、25%、50%和31%、13%、56%,差别也未达到统计学意义。Edwards SAPIEN和CoreValve两种支架瓣膜释放系统术后30 d死亡率也无明显差别[29],但两种系统的死亡构成比却存在差异。相比Edwards SAPIEN系统,CoreValve系统的血管并发症和出血发生率低(3%vs 22%),心包填塞和主动脉瓣返流发生率则较高(分别为26%vs 6%和10%vs 0%)[12]。TAVI术后1年死亡率超过20%[30],死亡原因中心脏相关性死亡所占比例较小,非心脏相关性死亡以及不明原因死亡所占比例较大,非心脏相关死亡原因主要包括肺脏并发症、肾脏衰竭、肿瘤和卒中,另外经心尖途径1年死亡率略高于经股动脉途径[30]。
4 减少TAVI并发症的方法
4.1 严格筛选患者 Logistic EuroSCORE评分和 STS (Society of Thoracic Surgeons)评分是两个常用的评估TAVI风险的指标,术后死亡病人相比存活病人其 Logistic EuroSCORE评分和STS评分均明显增高[31]。根据评分严格筛选TAVI病人对降低并发症、改善术后生存率非常重要。
4.2 操作水平的提高 单中心的经验发现,随着TAVI技术的逐步开展,经过学习曲线后,TAVI的成功率增加,并发症减少。德国医生Wendt将40例TAVI患者分成前后两部分进行对比,后20例患者较前20例的手术时间、X光应用时间和对比剂用量均明显减少,而术后30 d死亡率则显著降低[32]。加拿大学者Gurvitch报道了更大样本量的TAVI患者(270例),亦分为前135例和后135例两组,总体手术成功率从92.6%提高到97.8%,而术后30 d死亡率从13.3%降低至5.9%,并且发现操作经验是术后30 d生存率的独立预测因子[33]。
4.3 手术器械的改进 为了减少TAVI并发症的出现,已经有多种TAVI新产品出现。ACURATE TATM支架瓣膜系统(图2A)属于经心尖途径置入的自膨胀生物瓣,初步经验发现其瓣周漏较少[34]。JenaValveTM支架瓣膜系统(图2B)也属经心尖途径的自膨胀生物瓣,因采取了独特设计,使支架释放非常精准,释放过程中不需要快速起搏心室,血流动力学平稳,并且无冠脉开口阻塞和严重主动脉瓣返流发生,永久起搏器置入的比率也较低(9.1%)[35]。Claret CE ProTM滤网装置(图3)用于预防TAVI术中栓塞,54.3%的TAVI患者中可在滤网中发现组织碎屑,可预防术中TIA、小面积卒中或大面积卒中的发生[36]。
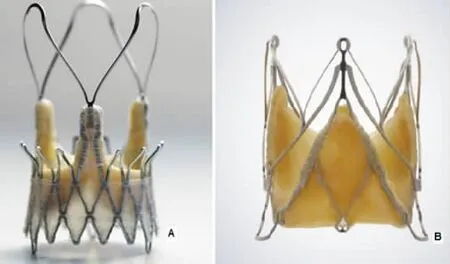
图2 两种经心尖途径自膨胀生物瓣支架系统(A:ACURATE TATM瓣膜,B:JenaValveTM瓣膜)
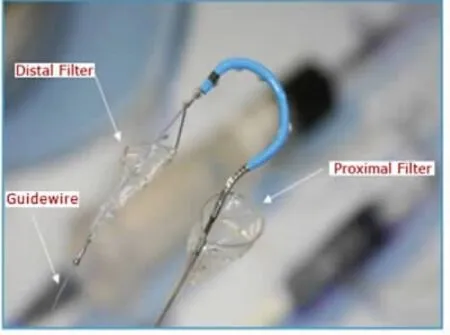
图3 Claret CE ProTM滤网装置
综上所述,TAVI虽然是一种正在广泛开展的介入手术,但目前仍然是一种高风险手术,半数以上的手术患者可能合并各类并发症。要减少并发症的发生,必须从严格筛选患者、术者的经验积累以及手术器械的进一步完善等方面进行严格要求。
[1] Cribier A,Eltchaninoff H,Bash A,et al.Percutaneous transcatheter implantation of an aortic valve prosthesis for calcific aortic stenosis: first human case description[J].Circulation,2002,106(24): 3006-3008.
[2] 葛均波,周达新,潘文志,等.经导管主动脉瓣置入术的初步经验[J].中华心血管病杂志,2011,39(11):989-992.
[3] Akin I,Kische S,Schneider H,et al.Surface and intracardiac ECG for discriminating conduction disorders after CoreValve implantation[J].Clin Res Cardiol,2012,101(5):357-364.
[4] Rubin JM,Avanzas P,del VR,et al.Atrioventricular conduction disturbance characterization in transcatheter aortic valve implantation with the CoreValve prosthesis[J].Circ Cardiovasc Interv,2011,4(3):280-286.
[5] Nuis RJ,Van Mieghem NM,Schultz CJ,et al.Timing and potential mechanisms of new conduction abnormalities during the implantation of the Medtronic CoreValve System in patients with aortic stenosis[J].Eur Heart J,2011,32(16):2067-2074.
[6] Piazza N,Nuis RJ,Tzikas A,et al.Persistent conduction abnormalities and requirements for pacemaking six months after transcatheter aortic valve implantation[J].EuroIntervention,2010,6(4):475-484.
[7] Takagi K,Latib A,Al-Lamee R,et al.Predictors of moderate-to-severe paravalvular aortic regurgitation immediately after CoreValve implantation and the impact of postdilatation[J].Catheter Cardiovasc Interv,2011,78(3):432-443.
[8] Pagnotta P,Ferrante G,Presbitero P.Rescue“valve in valve”implantation after late onset corevalve cusp rupture leading to acute massive aortic insufficiency.LID-10.1002/ccd.23155[doi][J].Catheter Cardiovasc Interv,2011.[Epub ahead of print]
[9] Stabile E,Sorropago G,Cioppa A,et al.Acute left main obstructions following TAVI[J].EuroIntervention,2010,6(1):100-105.
[10]Crimi G,Passerone G,Rubartelli P.Trans-apical aortic valve implantation complicated by left main occlusion[J].Catheter Cardiovasc Interv,2011,78(4):656-659.
[11]Tay EL,Gurvitch R,Wijeysinghe N,et al.Outcome of patients after transcatheter aortic valve embolization[J].JACC Cardiovasc Interv,2011,4(2):228-234.
[12]Moreno R,Calvo L,Salinas P,et al.Causes of peri-operative mortality after transcatheter aortic valve implantation:a pooled analysis of 12 studies and 1223 patients[J].J Invasive Cardiol,2011,23(5): 180-184.
[13]Reinsfelt B,Westerlind A,Ioanes D,et al.Transcranial Doppler microembolic signals and serum marker evidence of brain injury during transcatheter aortic valve implantation[J].Acta Anaesthesiol Scand,2012,56(2):240-247.
[14]Bleiziffer S,Ruge H,Mazzitelli D,et al.Survival after transapical and transfemoral aortic valve implantation:talking about two different patient populations[J].J Thorac Cardiovasc Surg,2009,138(5): 1073-1080.
[15]Smith CR,Leon MB,Mack MJ,et al.Transcatheter versus surgical aortic-valve replacement in high-risk patients[J].N Engl J Med,2011,364(23):2187-2198.
[16]Hayashida K,Lefevre T,Chevalier B,et al.Transfemoral aortic valve implantation new criteria to predict vascular complications[J].JACC Cardiovasc Interv,2011,4(8):851-858.
[17]Kahlert P,Al-Rashid F,Weber M,et al.Vascular access site complications after percutaneous transfemoral aortic valve implantation[J].Herz,2009,34(5):398-408.
[18]Alsac JM,Zegdi R,Blanchard D,et al.Complications of the access during aortic valve implantation through transfemoral access[J].Ann Vasc Surg,2011,25(6):752-757.
[19]Aminian A,Lalmand J,El NB.Perforation of the descending thoracic aorta during transcatheter aortic valve implantation(TAVI):an unexpected and dramatic procedural complication[J].Catheter Cardiovasc Interv,2011,77(7):1076-1078.
[20]Bagur R,Webb JG,Nietlispach F,et al.Acute kidney injury following transcatheter aortic valve implantation:predictive factors,prognostic value,and comparison with surgical aortic valve replacement[J].Eur Heart J,2010,31(7):865-874.
[21] Nuis RJ,Van Mieghem NM,Tzikas A,et al.Frequency,determinants,and prognostic effects of acute kidney injury and red blood cell transfusion in patients undergoing transcatheter aortic valve implantation[J].Catheter Cardiovasc Interv,2011,77(6):881-889.
[22]Madershahian N,Scherner M,Liakopoulos O,et al.Renal impairment and transapical aortic valve implantation:impact of contrast medium dose on kidney function and survival[J].Eur J Cardiothorac Surg,2012,41(6):1225-1232.
[23]Sinning JM,Ghanem A,Steinhauser H,et al.Renal function as predictor of mortality in patients after percutaneous transcatheter aortic valve implantation[J].JACC Cardiovasc Interv,2010,3(11): 1141-1149.
[24]Nuis RJ,Piazza N,Van Mieghem NM,et al.In-hospital complications after transcatheter aortic valve implantation revisited according to the Valve Academic Research Consortium definitions[J].Catheter Cardiovasc Interv,2011,78(3):457-467.
[25] Halliday BP,Dworakowski R,Brickham B,et al.Usefulness of periprocedural bleeding to predict outcome after transcatheter aortic valve implantation[J].Am J Cardiol,2012,109(5):724-728.
[26]Wenaweser P,Pilgrim T,Roth N,et al.Clinical outcome and predictors for adverse events after transcatheter aortic valve implantation with the use of different devices and access routes[J].Am Heart J,2011,161(6):1114-1124.
[27]de la Torre Hernandez JM,Gorria GM,de Prada JA,et al.Papillary muscle rupture:first report of this complication in a retrograde transfemoral aortic valve implantation[J].Catheter Cardiovasc Interv,2011,78(4):647-649.
[28]Vanezis AP,Baig MK,Mitchel IM,et al.Pseudoaneurysm of the left ventricle following apical approach TAVI[J].J Cardiovasc Magn Reson,2011,13:79.
[29]Bosmans JM,Kefer J,De Bruyne B,et al.Procedural,30-day and one year outcome following CoreValve or Edwards transcatheter aortic valve implantation:results of the Belgian national registry[J].Interact Cardiovasc Thorac Surg,2011,12(5):762-767.
[30]Thomas M,Schymik G,Walther T,et al.One-year outcomes of cohort 1 in the Edwards SAPIEN Aortic Bioprosthesis European Outcome (SOURCE)registry:the European registry of transcatheter aortic valve implantation using the Edwards SAPIEN valve[J].Circulation,2011,124(4):425-433.
[31]Ben-Dor I,Maluenda G,Iyasu GD,et al.Comparison of outcome of higher versus lower transvalvular gradients in patients with severe aortic stenosis and low(<40%)left ventricular ejection fraction[J].Am J Cardiol,2012,109(7):1031-1037.
[32] Wendt D,Eggebrecht H,Kahlert P,et al.Experience and learning curve with transapical aortic valve implantation[J].Herz,2009,34(5):388-397.
[33]Gurvitch R,Tay EL,Wijesinghe N,et al.Transcatheter aortic valve implantation:lessons from the learning curve of the first 270 high-risk patients[J].Catheter Cardiovasc Interv,2011,78(7):977-984.
[34]Kempfert J,Treede H,Rastan AJ,et al.Transapical aortic valve implantation using a new self-expandable bioprosthesis(ACURATE TA):6-month outcomes[J].Eur J Cardiothorac Surg,2012.[Epub ahead of print]
[35]Treede H,Mohr FW,Baldus S,et al.Transapical transcatheter aortic valve implantation using the JenaValve system:acute and 30-day results of the multicentre CE-mark study[J].Eur J Cardiothorac Surg,2012,41(6):e131-138.
[36]Naber CK,Ghanem A,Abizaid AA,et al.First-in-man use of a novel embolic protection device for patients undergoing transcatheter aortic valve implantation[J].EuroIntervention,2012,8(1):43-50.

