MIEX对水中溴离子的去除效能及其影响因素
陈 卫,曹 喆,刘 成,王 嫚
(河海大学a.浅水湖泊综合治理与资源开发教育部重点实验室;b.环境学院,南京210098)
臭氧作为一种强氧化剂,目前已被广泛应用于水处理工艺中。但含溴离子(Br-)的原水在臭氧化过程中会生成具有致癌和致突变性的溴酸盐,世界卫生组织对溴酸盐的暂行准则值为10μg/L[1],美国环保局饮用水标准中规定溴酸盐的最高允许浓度为10μg/L,期望值是不检出,欧盟规定为3μg/L[2]。影响溴酸盐生成的因素主要有水中溴离子浓度、臭氧投量、pH 值、碱度、温度、天然有机物(NOM)等[3]。现有的臭氧化过程中溴酸盐的控制方法多为加氨和控制pH值等[4],即在溴离子转化为溴酸盐的过程中对转化条件进行控制。此外,溴离子浓度是影响臭氧化过程中溴酸盐生成的重要因素,且存在一个临界浓度,低于此浓度时,溴酸盐的生成量低于仪器的检测限(2μg/L),而这个临界浓度随水质不同而变化;当要保证一定的剩余消毒臭氧量时,溴离子的临界浓度为0.18mg/L[5-6]。
磁性离子交换树脂(magnetic ion exchange resin,MIEX)是以聚丙烯为母体的季胺型阴离子交换树脂,形状为不透明的不规则球状物体,表面存在孔隙,粒径在180μm左右,氯离子(Cl-)作为树脂的可交换离子能与水中多种带负电的物质进行离子交换,其中包括溴离子[7-11]。本文采用去离子水加标的方法,研究MIEX对水中溴离子的去除效能及其影响因素。
1 材料与方法
1.1 试验材料与仪器
试验材料:MIEX(澳大利亚Orica公司),水中溴(Br)成分分析标准物质(上海市计量测试技术研究院),无水硫酸钠(国药集团化学试剂有限公司),氯化钠(南京宁试化学试剂有限公司),硝酸钾(南京宁试化学试剂有限公司),腐殖酸(上海巨枫化学科技有限公司嘉善巨枫化工厂),0.45μm微滤膜(上海市新亚净化器件厂)。
试验仪器:美国密利博超低有机物型超纯水器,深圳中润ZR4-6混凝试验搅拌机,HACH紫外分光光度扫描仪,德国耶拿analytikjenaAG MultiN/C2100TOC仪,美国戴安ICS-2000型离子色谱仪。
1.2 原水水质与试验方法
根据对水中溴离子含量调研结果和臭氧化过程中对溴离子含量的限值研究结果[12-15],确定溴离子加标初始浓度为1.0mg/L、0.5mg/L。考虑水中常见阴离子及有机物的情况,试验水样分为2大类:针对MIEX对溴离子去除效能的研究,采用去离子水加标配制成只含有溴离子的水样;针对影响因素的研究,向含相同浓度(0.5mg/L)的溴离子水样中投加不同浓度的硫酸盐、氯化物、硝酸盐以及腐殖酸,考察阴离子及有机物对MIEX去除溴离子效能的影响。
离子交换过程采用烧杯试验实现,搅拌速度为200r/min,在0~30min之间抽取水样,用0.45μm微滤膜过滤后测定各水质参数。
1.3 检测指标及方法
检测指标:波长254nm处的紫外吸光值(UV254)、溶解性有机碳(DOC)、pH 值、溴离子、硫酸根离子、氯离子、硝酸根离子。
UV254采用紫外分光光度计测定;DOC采用TOC仪测定;采用离子色谱仪测定各阴离子的浓度,分析柱为戴安IonPac AS11-HC(4mm×250 mm),淋洗液自动发生装置在线产生30mmol/L KOH等度淋洗,淋洗液流速为1.0mL/min,ASRS_4 mm阴离子抑制器,电流75mA,进样体积为100μL。
2 结果与分析
2.1 MIEX对溴离子的去除效能
分别采用3种不同 MIEX投加量(1、10、20 mL/L)处理2 种溴离子浓度的水样(488.444 2、991.053 3μg/L),试验结果见图1。
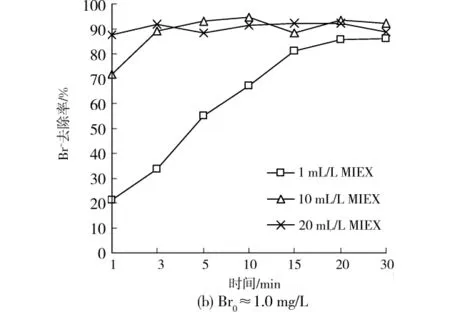
图1 不同MIEX投加量对纯水中溴离子的去除效果
如图1所示,随着反应时间的增加,溴离子的去除率也相应增加。3种投加量条件下MIEX对溴离子去除率均可达到90%以上,但达到平衡的时间存在一定的差别。投加量为1mL/L时,反应30min后溴离子的去除效果趋于稳定,而10、20mL/L时其对溴离子去除的平衡时间分别为5、3min。对于2种浓度的溴离子水样,MIEX对其去除的趋势基本一致,但相同MIEX投加量时,对低浓度的去除率略优于高浓度。原因在于相同剂量的MIEX对溴离子提供相同的交换位数量,虽然溴离子浓度上升会增加树脂边界水膜两侧离子的浓度梯度,使溴离子在水膜中扩散加快,从而增大离子交换速度,使离子交换平衡向正向移动,但由于采用烧杯试验,水中存在被置换下的氯离子,故逆向反应也会加剧直至达到新的平衡,此时树脂相上的溴离子占水样中总溴离子的比例则会有所下降,即溴离子的去除率降低。综上所述,10mL/L的MIEX投加量即可对溴离子的去除达到很好的效果,反应平衡时间为5min。
2.2 MIEX去除溴离子的影响因素
氯离子作为MIEX的可交换离子能与水中带负电的物质进行离子交换,水中存在的阴离子以及带负电的DOC分子均可与MIEX发生交换反应,进而影响MIEX对溴离子的去除效果。所以试验进一步考察了水中常见阴离子及有机物对MIEX去除溴离子效能的影响。
2.2.1 阴离子对溴离子去除效果的影响 不同含量的硫酸根离子(SO42-)对10mL/L的MIEX去除溴离子效果的影响见图2。如图所示,离子交换反应平衡时间同上文所述基本一致,在5min左右。硫酸根离子的存在显著降低了MIEX对溴离子的去除效果,且随着硫酸根离子含量的增加这种影响愈加明显。3种硫酸根含量(50、100、200mg/L)条件下,10mL/L的MIEX在5min时对溴离子的去除率分别为87%、76%、60%,均明显低于纯水中95%的去除率。这是因为离子交换树脂对各种离子具有选择性,它可以优先交换溶液中某种离子,一般化合价高的离子被优先交换,在同价离子中则优先交换原子序数大的离子[16]。MIEX对硫酸根离子的选择性强于溴离子,故在硫酸根离子与溴离子均存在时,硫酸根离子被优先去除,使单位溴离子所能接触的交换位数量减少,降低了MIEX对溴离子的去除率。此外,3种硫酸根离子含量条件下10mL/L的MIEX在5min时对硫酸根的去除率均高于对应溴离子的去除率(见图3),原因也在于MIEX对硫酸根离子的选择性强于溴离子,同时可能与硫酸根离子含量远高于溴离子含量有关。
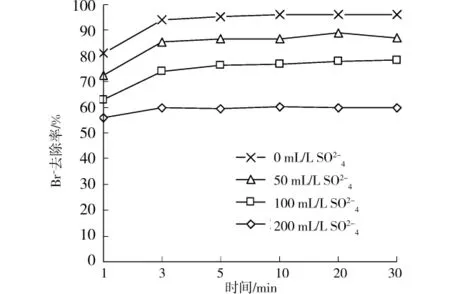
图2 不同硫酸根离子含量时对溴离子的去除效果
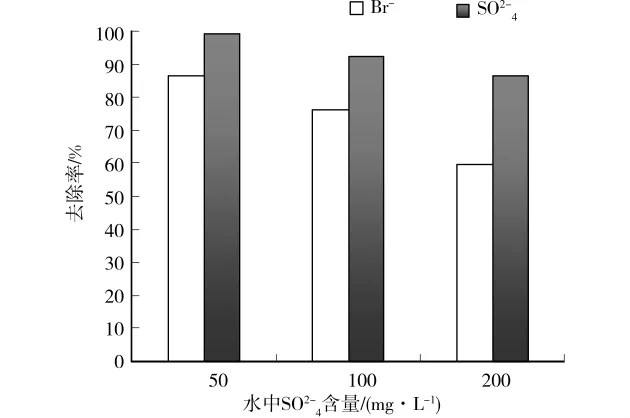
图3 不同硫酸根离子含量时对阴离子的去除效果
氯离子(Cl-)对MIEX去除溴离子效果的影响同硫酸根离子基本一致,如图4所示,10mL/L的MIEX对含有50、100、200mg/L氯离子的水样中溴离子的去除率分别为86%、81%、63%,树脂上的氯离子被置换到水中,增加了水中氯离子的含量,并且初始时水中氯离子的含量就远高于溴离子,根据化学平衡移动原理,当水中氯离子含量过高时,会抑制离子交换反应的正向进行,进而影响MIEX对溴离子的去除效能。
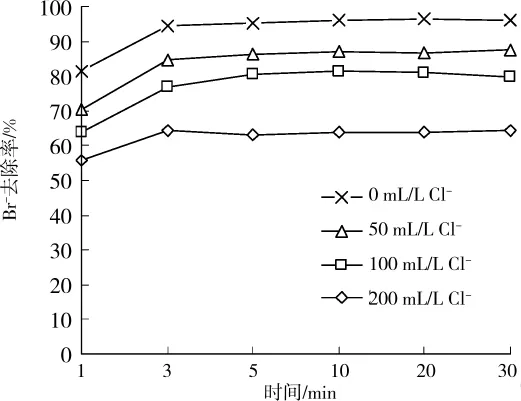
图4 不同氯离子含量时对溴离子的去除效果
由于水中硝酸根离子(NO3-)含量较少,故仅研究了10mg/L的硝酸根离子对MIEX去除溴离子的影响(见图5)。10mL/L的MIEX投加量时反应平衡时间同上文所述一致,在5min左右,对溴离子的去除率为95%,与纯水中溴离子的去除率基本一致,对硝酸根离子的去除率则达到了99%。硝酸根离子含量较低,在离子交换过程中只有少量阴离子与溴离子竞争MIEX交换位数量,故对溴离子去除几乎无影响,这说明水中阴离子含量是影响MIEX去除溴离子的主要因素之一。而MIEX对硝酸根离子的去除率略高于溴离子,这可能是因为MIEX对硝酸根离子的选择性强于溴离子,硝酸根离子被优先去除。

图5 硝酸根离子存在时对阴离子的去除效果
2.2.2 有机物对溴离子去除效果的影响 以腐殖酸为研究对象考察了有机物对MIEX去除溴离子的影响,结果见图6(图6所示水样中DOC为3.12 mg/L,UV254为0.208/cm)。
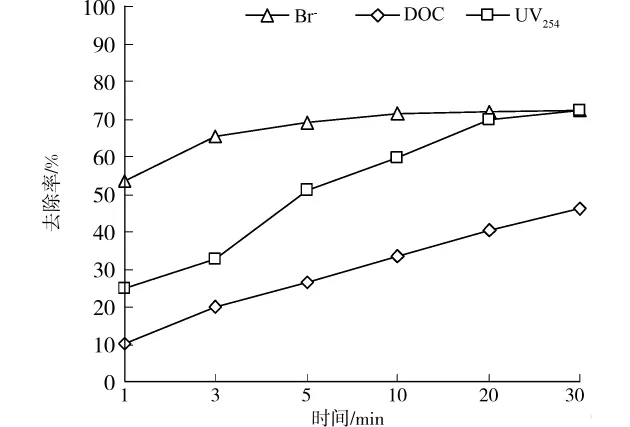
图6 有机物存在时对溴离子、DOC、UV254的去除效果
由图6可以看出,10mL/L的MIEX对溴离子的去除率在5min时为69%,明显低于纯水中95%的去除率,原因如前所述,但去除溴离子的反应平衡时间与前述基本一致,均在5min左右。与之相比,MEIX去除有机物的平衡时间则较长,其对2种表征有机物含量的指标(UV254、DOC)的去除稳定时间均在20min以上(对UV254的去除约在20min时稳定,而对DOC的去除则随时间呈上升趋势,直至反应30min时仍未达到平衡)。MIEX对3个指标的去除率顺序为溴离子>UV254>DOC,原因在于:同有机物分子量相比,溴离子原子量相对较小,容易并且迅速进入球状的MIEX与其表面和孔隙内的氯交换基进行离子交换,而分子量相对较大的有机物在水中及树脂孔隙内的扩散速度较慢,并且无法到达树脂内部孔隙较小的部分,故MIEX对溴离子的去除率及反应平衡时间均高于有机物;同时分子量相对较大的有机物分子会在一定程度上阻塞内部孔隙导致溴离子无法进入,并且在溴离子与有机物同时存在的位置有机物会同溴离子竞争MIEX交换位,从而使溴离子的去除效果降低。UV254表征水中不饱和键有机物,这些物质大部分为疏水性荷电物质,DOC则表征全部溶解性有机物,由于MIEX为阴离子离子交换树脂,故对UV254所表征的荷电物质去除率相对较高,这与国外研究[6-7,17]相符。MIEX 对有机物、阴离子去除过程的差异对于需要分别去除有机物和阴离子的特定用途时的工艺参数优化具有积极意义。
3 结 论
1)MIEX可以有效去除纯水中的溴离子,投加量为10mL/L和20mL/L时其对溴离子去除率均在90%以上,且达到交换平衡时间分别为5min和3min。
2)水中常见的其它带负电物质会在一定程度上影响MIEX对溴离子的去除效果,在常见的含量条件下10mL/L的MIEX对溴离子的去除率一般在50%以上。阴离子含量及MIEX的选择性是影响其对溴离子去除效果的主要因素。
3)有机物的存在使MIEX对溴离子的去除率明显下降,去除率在70%左右。MIEX对有机物、阴离子的去除过程存在差异:10mL/L的MIEX去除阴离子的反应平衡时间在5min左右,而去除有机物的平衡时间则较长,其对2种表征有机物含量的指标(UV254、DOC)的去除稳定时间均在20min以上,这对于需要分别去除有机物和阴离子的特定用途时的工艺参数优化具有积极意义。
[1]World Health Orgnization.Guidelines for drinking-water quality[M].3rd ed.Geneva:World Health Organization,2008.
[2]尹军,张小雨,刘志生,等.含溴矿泉水臭氧化过程中溴酸盐的生成及控制[J].供水技术,2008,2(6):1-4.YIN Jun,ZHANG Xiaoyu,LIU Zhisheng,et al.Formation and control of bromate in ozone disinfection of mineral water containing bromide [J].Water Technology,2008,2(6):1-4.
[3]陈伟鹏.催化臭氧氧化对溴酸盐生成影响研究[D].哈尔滨:哈尔滨工业大学,2007.
[4]吴清平,孟凡亚,张菊梅,等.臭氧消毒中溴酸盐的形成、检测与控制[J].中国给水排水,2006,22(16):12-15.WU Qingping,MENG Fanya,ZHANG Jumei,et al.Formation,detection and control of bromate in the ozone disinfection of drinking water[J].China Water& Wastewater,2006,22(16):12-15.
[5]Westerhoff P,Song R,Amy G,et al.NOM′s role in bromine and bromate formation during ozonation[J].American Water Works Association,1998,90(2):82-94.
[6]Gunten U,Hoigne J.Bromate formation during ozonization of bromide-containing waters:interaction of ozone and hydroxyl radical reactions[J].Environmental Science and Technology,1994,28(7):1234-1242.
[7]Boyer T H,Singer P C.Bench-scale testing of a magnetic ion exchange resin for removal of disinfection by-product precursors[J].Water Research,2005,39(7):1265-1276.
[8]Boyer T H,Singer P C.A pilot-scale evaluation of magnetic ion exchange treatment for removal of natural organic material and inorganic anions [J].Water Research,2006,40(15):2865-2876.
[9]Johnson C J,Singer P C.Impact of a magnetic ion exchange resin on ozone demand and bromate formation during drinking water treatment[J].Water Research,2004,38(17):3738-3750.
[10]Hsu S,Singer P C.Removal of bromide and natural organic matter by anion exchange[J].Water Research,2010,44(7):2133-2140.
[11]Humbert H,Gallard H,Suty H,et al.Performance of selected anion exchange resins for the treatment of a high DOC content surface water[J].Water Research,2005,39(9):1699-1708.
[12]王祖琴,李田含.含溴水臭氧化过程中溴酸盐的形成与控制[J].净水技术,2001,20(2):7-11.WANG Zuqin,LI Tianhan.Formation and control of bromate during ozonation of drinking water containing bromide[J].Water Purification Technology,2001,20(2):7-11.
[13]Siddiqui M S,Amy G L,Rice R G.Bromate ion formation in drinking water:a critical review [J].American Water Works Association,1995,87(10):58.
[14]Lefebvre E,Racaud P,Parpaillon T H,et al.Results of bromide and bromate monitoring at several water treatment plants[J].Ozone:Science & Engineering,1995,17(3):311-327.
[15]张奎山.饮用水臭氧化工艺研究与接触池流场模拟[D].天津:天津大学,2005.
[16]李圭白,张杰.水质工程学[M].北京:中国建筑工业出版社,2005.
[17]Kitis M,Harman B I,Yigit N O,et al.The removal of natural organic matter from selected Turkish source waters using magnetic ion exchange resin(MIEX®)[J].Water Research,2007,67(12):1495-1504.

