高乌甲素贴剂的体外释放度与经皮渗透研究
刘新国,李居怡,王雄,吴金虎
(武汉市第三医院,湖北武汉430061)
高乌甲素(Lappaconitine,又名拉巴乌头碱或刺乌头碱),是从毛莨科植物高乌头根中提取分离的生物碱,化学名称为(1α,14α,16β)-20乙基-1,14,16-三甲氧基-乌头烷-4,8,9-三醇-4-[2-(乙酰氨基)苯甲酸酯],分子式是C32H44N2O8,熔点为216℃[1]。作为我国首创一种以镇痛作用为主[2],同时具有局麻[3-4]、降温、解热和抗炎消肿[5]及抗心律失常[6]等作用的非成瘾性镇痛药,临床上已有氢溴酸高乌甲素片、氢溴酸高乌甲素注射液等制剂用于晚期癌症及术后镇痛治疗[7-8]。由于高乌甲素在极性溶媒中溶解度小,口服生物利用度较低,半衰期较短,将其制成经皮给药制剂可以避免口服给药发生的肝脏首过效应,避免其在胃肠道内的破坏,降低药物毒性和不良反应[9-11]。而聚异丁烯作为一种新型高分子热熔压敏胶材料,其长链大分子结构蜷曲形成独特的基质网状结构,对西药和中药均具有良好的包容性。聚异丁烯作为贴膏剂基质具有无过敏性、不粘毛,可反复撕贴的特点,因此对该贴剂的体外释药与经皮渗透行为进行研究,不仅有助于探讨聚异丁烯作为新型医药贴膏热熔压敏胶基质可行性,同时有利于镇痛药膜控释透皮吸收制剂的研究开发。
1 仪器、试药与动物
1.1 仪器TK—12B型透皮扩散试验仪,凯科技贸易有限公司,上海;Agilent 1200 Series四元泵高效液相色谱仪,美国;Mettler Toledo十万分之一分析天平,德国;HS6510D超声波清洗器,昆山市超声仪器有限公司;禹洋ZRS—8G智能溶出仪(符合《中国药典》标准)。
1.2 药品与试剂高乌甲素对照品,中国药品生物制品检定所,批号:100547-200401;高乌甲素贴剂,实验室自制,分子聚合度从小到大依次为药贴①<药贴②<药贴③;乙腈,色谱纯,天津四友试剂公司生产;水为纯净水,其他试剂均为分析纯。
1.3 实验动物健康成年雄性SD大鼠12只,广州中医药大学实验动物中心提供,合格证号:SCXK(粤)2009-0001。
2 高乌甲素定量测定方法
2.1 色谱条件[12]Diamonsil C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-水-三乙胺(200∶160∶0.5),用磷酸调pH为8.0;体积流量1.0 mL/min;检测波长252 nm;进样量10 μL;柱温30℃。
2.2 对照品贮备溶液制备精密称取高乌甲素对照品适量,用甲醇制成每1 mL含高乌甲素65.8 μg的溶液,摇匀,即得。
2.3 线性关系的考察精密吸取高乌甲素对照品贮备溶液100、200、1 000、2 000、4 000、8 000 μL,用甲醇稀释定容至10 mL,精密吸取10 μL注入液相色谱仪,按照上述色谱条件进行测定。以峰面积积分值为横坐标(X),高乌甲素进样量(ng)为纵坐标(Y),进行计算,得回归方程:Y=0.887 9X+0.378 1,r=0.999 9,表明高乌甲素在2.632~210.560 ng呈良好的线性关系。
2.4 精密度试验精密吸取同一供试品溶液10 μL,重复进样5次,测定指标峰峰面积,计算平均峰面积为240.907 7,RSD为1.80%,表明仪器精密度良好。
2.5 稳定性试验精密吸取同一供试品溶液10 μL,分别于0、2、6、12、24 h进样,测定高乌甲素色谱峰面积,计算平均质量浓度为2.63 μg/mL,RSD为1.18%,表明供试品溶液在24 h内稳定性良好。
2.6 回收率试验分别向已知量的渗透液样品中加入一定量高乌甲素对照品溶液,用流动相加至10 mL,混匀后,精密吸取10 μL注入液相色谱仪,测定指标峰峰面积,利用标准曲线计算高乌甲素含有量,并计算加样回收率。结果高乌甲素平均加样回收率为96.32%,RSD为0.86%,结果见表1。

表1 回收率试验结果(n=9)Tab.1 Recovery test results(n=9)
3 高乌甲素贴片体外释放度试验
体外释放度试验参照2010年《中国药典》二部附录XD第三法。以20%乙醇-生理盐水500 mL作为释放介质,预温至(32±0.5)℃,转速100 r/min,取贴片(释药面积34.63 cm2)固定于自制的两层碟片中间,释放面向上,搅拌桨相隔(25±2)mm。立即启动搅拌并计时,分别于1、2、4、6、8、10、12、14、16、20 h取样3 mL,并及时补充等体积的空白释放递质。释放液用0.45μm微孔滤膜过滤,弃去初滤液,收集续滤液,进行HPLC测定,测得高乌甲素的累积释药量Q[μg/(cm2)],结果见图1。

图1 贴剂中高乌甲素累积释药量的经时变化曲线Fig.1 The cumulative releasing curves of different lappaconitine patches
对累积释药量Q(μg/cm2)进行零级、一级和Higuchi动力学方程拟合,结果见表2。
由表2结果可知:3种高乌甲素贴剂释药行为均以Higuchi动力学方程拟合为优,药物从单位面积基质中的释放量与时间的平方根成正比,表明3种贴剂均属于骨架型释药系统。从3种药贴的释药速率常数J可以判断释药速率和完全程度药贴①>药贴②>药贴③。
4 3种高乌甲素贴剂经皮渗透试验
4.1 试验皮肤的制备取压倒性SD大鼠12只,8%BaS腹部脱毛,饲养24 h,脱颈椎处死后取下腹部皮肤,仔细剥离皮下脂肪组织,并用生理盐水冲洗至无浑浊为止,备用(皮肤用铝箔包裹,置于低温冰箱中保存,试验时取出,室温下自然解冻后使用)。
4.2 经皮渗透试验方法取预处理的鼠皮,将高乌甲素贴片紧贴于离体鼠皮角质层一侧,用改良的Franz扩散池(池口面积为2.8 cm2,高为6.5 mL)的两个半池将皮肤夹紧,角质层面向上,将多余的皮肤剪去,固定装置。将20%乙醇-生理盐水加入接收池,液面与皮肤内层接触,保证无气泡存在。开动电磁搅拌器恒速搅拌(200 r/min)和恒温水浴(32±1)℃。另取一套Franz扩散池装置,同法操作,将不含药物的贴剂空白基质紧贴于离体鼠皮角质层一侧,作为空白对照。分别于规定时间取样5 mL,再立即补充相同温度5 mL接收液。接收液用0.45 μm微孔滤膜滤过,取续滤液供HPLC测定。在测定的峰面积标准曲线上求出相应的药物浓度,计算累积渗透量[Q,μg/cm2],以Q~t作线性回归,直线的斜率即为透皮速率[J,μg/(cm2·h)],将稳态直线推至时间轴,得渗透时滞tlag(h)。

表2 3种贴剂释药行为的零级、一级和Higuchi方程拟合结果Tab.2 Simulation of pharmacokinetics equation of release for lappaconitine patches
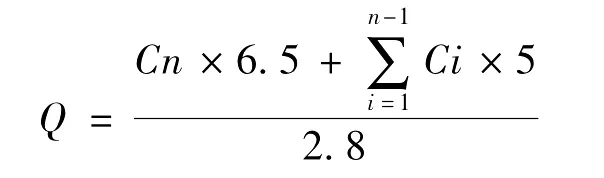
式中,Cn为第n个取样点测得的药物质量浓度(μg/mL);Ci为第i(i=n-1)个取样点测得的药物质量浓度(μg/mL);A为有效扩散面积。
4.3 3种高乌甲素药贴经皮渗透试验结果的比较研究按照4.2项下方法进行透皮实验,每种药物贴剂平行操作4次,并对接收液中高乌甲素进行测定,结果见图2。
对累积释药量Q(μg/cm2)进行零级、一级和Higuchi动力学方程拟合,结果见表3。
由表3可知,高乌甲素药贴①在20 h内累积透皮量显著大于其他两种类型贴剂(P<0.01),而药贴②与药贴③在考察时间内累积透皮量差异较小(P>0.05)。从3种贴剂释药速率与透皮速率差异的变化趋势可以看出,基质释药速率与皮肤实际透过能力差异越大,受皮肤的限速影响越强。

图2 贴剂中高乌甲素累积透皮量的经时变化曲线Fig.2 Cumulatively percutaneous penetration curves of different lappaconitine patches
5 讨论
3种高乌甲素贴剂在20 h内体外释放曲线和经皮渗透曲线均以Higuchi动力学方程拟合较好,判断该制剂应属于骨架型释药系统。其累积释药量与累积透皮量具有因聚异丁烯分子聚合度的增加而减小的趋势,药物从贴剂基质中的释放速率均大于渗透通过皮肤的速率。3种贴剂释药速率与透皮速率差异的变化趋势可以看出,基质释药速率与皮肤实际透过能力差异越大,受皮肤的限速影响越强。
除高分子基质材料的聚合度影响外,基质药物浓度、基质厚度、促渗剂种类与用量等同样会影响药物的释放与经皮渗透效果。对于这一类经皮给药制剂的研究,应根据考察指标的特点选择特异性方法进行考察,只有把主要影响因素研究清楚了才能开发出安全长效的膜控释经皮给药制剂。

表3 3种贴剂经皮渗透行为的零级、一级和Higuchi方程拟合结果Tab.3 Transdermal permeation parameters of lappaconitine patches
[1]蒋山好,朱元龙,朱任宏.中国乌头的研究[J].药学学报,1982,17(4):288-292.
[2]唐希灿.刺乌头碱氢溴酸的药理作用研究[J].药学通报,1983,18(8):579-584.
[3]周秋雯,徐建国,谢蔚影.氢溴酸高乌甲素对神经病理性疼痛大鼠的影响[J].临床麻醉学杂志,2006,22(11):847-849.
[4]林密迦,杨锡馨.高乌甲素对手术致痛大鼠的镇痛及局麻作用的研究[J].海峡药学,2011,23(4):29-31.
[5]刘铭佩,鞠洋,党月兰.高乌甲素的抗炎作用[J].中药药理与临床,2004,20(4):13-14.
[6]孔古娅,卿德华,楚延,等.氢溴酸高乌甲素的抗心律失常作用[J].四川生理科学杂志,2002,24(4):175-177.
[7]王俊莲,孙蒙蒙,谢志勇.高乌甲素复合芬太尼静脉自控镇痛对手术后应激反应的影响[J].山西医药杂志,2011,40(11):1135-1137.
[8]管玉珠,史彦斌,王荷.止痛药氢溴酸高乌甲素的研究进展[J].中国医学理论与实践,2005,15(12):1839-1840.
[9]辛蕊华,程富胜,胡振英,等.高乌甲素的研究概况[J].中兽医医药杂志,2009,2(2):74-75.
[10]许颖,倪京满,马子娇,等.氢溴酸高乌甲素大鼠在体胃肠的吸收动力学研究[J].中国新药杂志,2010,19(21):1995-1997.
[11]邱永锋,赵苗,沙先谊,等.氢溴酸高乌甲素经皮渗透特性研究[J].中国民族民间医药,2011,20(20):30-32.
[12]胡雪莲,余涛,邢茂,等.高效液相色谱法测定氢溴酸高乌甲素含量与有关物质[J].医药导报,2011,30(2):249-251.

