磁共振扩散成像肝脾ADC比值评价肝纤维化程度的研究
1.山西医科大学医学影像系2.山西医科大学第二医院CT室(山西 太原 030001)
张冬艳1 薛雁山2
肝纤维化是常见的肝脏弥漫性损害性疾病。临床对于肝脏受损程度的评估主要依靠Child-pugh分级,以临床症状、体征及实验室相关指标为依据。随着磁共振功能成像方面的突破,出现了目前唯一无创反映活体组织功能状态的影像学检查技术—磁共振扩散加权成像(diffusionweighted imaging,DWI)[1],其表观扩散系数(apparent diffusion coefficient,ADC)可以客观量化组织中水分子的受限程度,反映组织的病理变化。随着DWI在肝脏病变中的广泛研究和应用,慢性肝炎-肝纤维化方面也做出了一定的研究和评估[2,3]。本文拟采用1.5T磁共振DWI技术,以脾脏作为参考器官,研究肝脾ADC值比值与肝纤维化严重程度之间的关系。
材料与方法
1.1 研究对象
1.1.1 正常对照组 正常志愿者15例,男9例,女6例, 年龄31-68岁, 平均49.5岁, 临床检查均无肝炎及肝脏占位性病变,实验室检查肝功能指标及腹部影像学检查未见异常者。
1.1.2 病例组 选取我院2011年1月至8月的肝纤维化患者39例(病例组,均为病毒性肝炎患者), 其中男25例, 女14例, 年龄28-75岁, 平均51.5岁。慢性乙肝者32例,慢性丙肝者7例,除外其他原因肝损伤所致的肝纤维化病例。其中除5例经临床诊断为肝硬化外,34例患者均穿刺取病理组织活检证实。病例组中经手术病例确诊的3例于术前行MR检查,其余36例均与肝穿刺后两到三周时间区间行本MR检查。以上两组均告知实验的目的,并签署知情同意书。嘱受检者检查前晚饭以流质为主,检查前禁食、水至少4小时。对所有检查者进行闭气训练。采用Scheuer法[4]对所有入选者进行肝纤维化的程度分期(S0-S4期)。
1.2 仪器和扫描方法采用GE signal Excite HD1.5T超导型全身磁共振扫描系统,8通道体部相控阵线圈,并行采集空间敏感编码(ASSET) 技术,呼吸门控技术。常规行轴位T1WI、压脂T2WI、冠状位T1WI扫描,之后行DWI扫描,DWI扫描序列为SE-EPI-DWI。患者呈仰卧位,足先进,以肝门水平为中心,扫描野的上、下方各施加一个预饱和带,以消除肺部气体、胃肠道气体和蠕动及心脏搏动等因素对图像质量的影响。采用STIR技术消除化学位移伪影。选取b=200,400,600,800,1000s/mm2,扫描参数: TR 1800ms, TE 50ms, 弥散方向ALL,层厚8mm, 层间距1mm, FOV取值范围40cm×40cm~42cm×42cm,矩阵128×128, 激励次数2次, 于深吸气- 再深呼气- 呼气末闭气扫描模式, 均1次闭气完成扫描,扫描时间16s左右,得到DWI的原始图像(图1)。
1.3 ADC值测量和计算
1.3.1 肝右叶ADC值的测量经计算机处理后即可得出ADC图。在其上选取肝门中心层面及其上和其下两个层面的ADC图中直接测量ADC值,分别在肝右叶各选取三个感兴趣区(ROI),大小50-100mm2左右,避开DWI图像中肉眼可见的胆管和血管、伪影以及小的局灶性病灶(如小囊肿等),复制相同大小ROI,取其平均值,得到肝右叶平均ADC值(图2)。亦可用通用的ADC值的公式计算,在DWI原始图像上,取得ROI,利用公式ADC=In(SI0/SI1)/(b1-b0),b0=0s/mm2,b1分别为200,400,600,800,1000s/mm2,SI0 和SI1分别取相对应的DWI图像上的信号强度,In为自然对数计算而得。
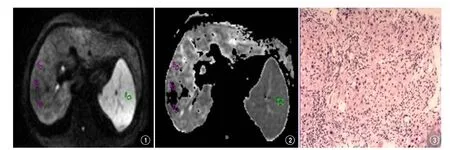
图1-2 为慢性乙肝S3期患者。图1为b=800s/mm2下DWI的原始图像。图2为该病人b=800s/mm2下的ADC图,用以测量相应层面的肝右叶ADC值及脾脏ADC值,其中粉色ROI为肝右叶ADC值,绿色为脾脏ADC值。图3为该病人的病理图片,显示肝小叶周围界板破坏,汇管区纤维组织增生(HE×100)。
1.3.2 脾脏ADC值的测量 以同样的方法测量连续三个不同层面的脾脏ADC值,取其平均值,尽量避免在脾门附近取值,得到脾脏的平均ADC值(图2)。
1.3.3 肝脾ADC值之比 对根据S分期的肝右叶平均ADC值与其相对应的脾脏平均ADC值取比值。
结 果
2.1 病理结果分析 15例正常对照组肝纤维化分期均为S0期。病例组中S0期2例,S1期4例,S2期7例,S3期8例(图3),S4期18例。
2.2 肝右叶及脾脏不同b值下ADC值的比较分析 随着肝纤维化程度的加重,相同b值下的肝右叶及脾脏的ADC值均是逐渐降低的,肝右叶的ADC值较脾脏下降的更快。肝脏各b值下的ADC值与纤维化分期组间两两比较,差别有统计学意义,p值均<0.05,b=800s/mm2时差异最大,相关性分析呈负相关,b=800s/mm2,与S期的相关性均优于其他组。脾脏各b值下的ADC值与纤维化分期组间两两比较,差别有统计学意义,但与S0、S1期无明显相关性,而与S2-S4期有明显相关性。见表1。

表1 肝纤维化不同分期在不同b值扫描下的ADC值(×10-3mm2/s)
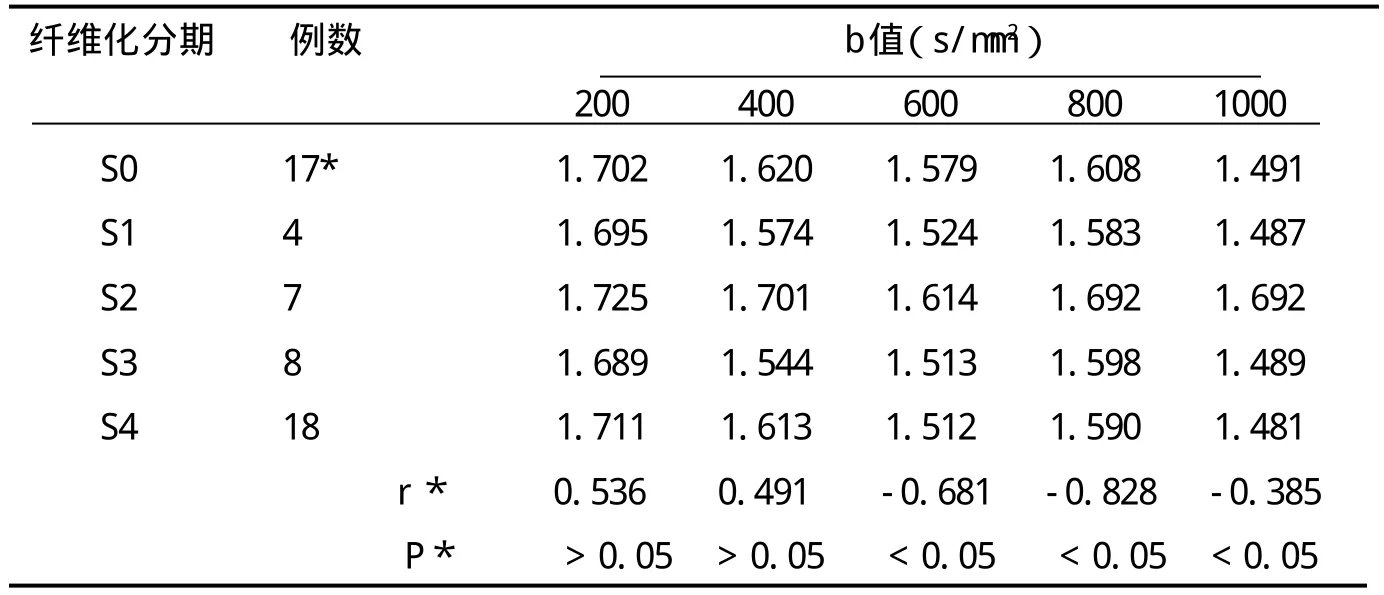
表2 不同b值下肝脾ADC比值与肝纤维化分期的相关性

表3 肝脾ADC比值与肝纤维化S2及S3的效能评价
2.3 肝脾ADC比值与肝纤维化分期的相关性分析 肝脾ADC比值在小b值(b=200和400 s/mm2)时与S分期无明显相关性,P值>0.05,而与S2期以上的肝纤维化呈负相关,且于b=800s/mm2时相关性最强。见表2。
2.4 肝脾ADC比值与肝纤维化分期效能评价 b=800s/mm2时,S2期以上的肝脾ADC比值评价肝纤维化的灵敏度和特异度分别为0.819和0.947;S3期以上肝脾ADC比值评价肝纤维化的灵敏度和特异度分别为0.857和1.000,均优于其他组。见表3。
讨 论
3.1 肝纤维化与肝脏DWIADC的关系 近来一些相关文献[5,6]报道了肝纤维化及肝硬化与ADC值的关系,但结果存在争议。Wang K等[7]利用DWI对肝纤维化和肝硬化病例的研究证实,ADC值与肝纤维化指标(实验室血清学指标及病理分级)和肝功能Child-pugh评分有显著相关性,利用ADC值可反映肝纤维化程度,这与本研究中肝纤维化组与肝纤维化S分期的相关性研究结果是基本一致的,推测导致其发生可能的原因:在发生肝纤维化时, 组织细胞内大量的纤维组织增生及大分子蛋白质的沉积,使原有正常肝小叶结构发生紊乱,细胞间隙和细胞内、外水分子的扩散活动受限, 导致肝脏ADC值下降,DWI信号高于正常肝脏[8]。杨正汉等[9,10]实验提出较重的肝纤维化组织的ADC值降低的另一可能因素是增生的纤维胶原破坏了肝细胞的微循环,造成肝实质的血流灌注的下降,并认为后者是肝纤维化ADC值下降的主要因素。肝纤维化时,除了伴随不同程度的炎症反应,还有脂肪浸润、铁质沉积等改变,亦成为肝纤维化ADC值下降的影响因素。
3.2 肝纤维化与脾脏DWIADC的关系 在进行对脾脏的ADC值探讨中发现,其与S2期以下(不包括S2期)的肝纤维化没有显著相关,而S2期以上(包括S2期)的肝纤维化却与脾脏ADC值存在相关性,笔者认为可能与S2期以上的肝纤维化时,脾脏已经出现相应的病理变化有关。肝纤维化时, 导致肝内门静脉受压和不规则狭窄, 肝血管床面积急剧减少, 门静脉灌注血流明显受阻, 从而引起更加严重的门静脉高压和脾肿大。出现门脉高压的患者脾脏的血管内皮细胞一氧化氮合酶(NOS)数量及活性明显增多,一氧化氮(NO)生成增加,造成血管扩张,门脉血流增多,脾静脉血流量亦增多。同时, 血流的高压状态及血液中的各种递质, 如NO、内皮素等, 均能刺激血管平滑肌细胞增殖[9],血管结构改建,造成了低速、高压、高血流的血流动力学状态,阻碍了水分子的扩散运动, 使脾脏ADC值下降。另外,门脉高压亦会导致纤维化脾结节的形成其中的铁元素而影响其磁共振信号[12]。
3.3 肝纤维化与肝脾ADC值比值的关系 以脾脏作为参考器官,利用磁共振扩散加权成像评价肝纤维化程度的相关性表明,b=800s/mm2对于S2期以上肝纤维化的评价优于其他各组,这与Do RK等[13]的以脾脏作为参考器官研究肝纤维化优于单纯测量肝脏ADC值的研究结果是相一致的。肝纤维化与肝脾ADC比值相关性,由正相关变为负相关,笔者认为主要原因有,第一,肝纤维化时,脾脏的改变,始终要晚于肝脏本身的变化,且程度也明显较肝脏变化轻,这也是能采用脾脏作为参考器官的原因之一;第二,由于ADC值受血液灌注影响较大,所以导致在小b值下测量的肝脏和脾脏的ADC值变异度较大,且不稳定,可能会对数据产生影响。
综上所述,本研究利用脾脏作为参考器官评价ADC值与肝纤维化分期的关系进行了分析,认为在b=800s/mm2对于评价S2期以上(中重度)的肝纤维化能力较强。但由于样本量等因素的制约,尚不能精确得出ADC的截点标准,仍需进一步探讨和研究。
1.Mürtz P, Krautmacher C, Traber F,et al. Diffusion-weighted whole body MR imaging with background body signal suppression: a feasibility study at 3.0 Tesla[J]. Eur Radiol,2007,17:3031-3037.
2.Girometti R, Furlan A, BazzocchiM,et al. Diffusion – weighted MR I in evaluating liver fibrosis∶ a feasibility study in cirrhotic patients[J]. Radiol ( Torino), 2007,112(3)∶394-408.
3.Lewin M, Poujol - Robert A, Bo? lle PY, et al. Diffusion -weighted magnetic resonance imaging for the assessment of fibrosis in chronic hepatitis C[J]. Hepatology,2007, 46(3)∶658-665.
4.Scheuer PJ.Classificationn of chronic viral hepatitis:a need for reassessment[J]. J Hepatol,1991,13:372-374.
5.Taouli B,Tolia AJ,Losada M,et a1.Diffusion-weighted MRI for quantification of liver fibrosis:preliminary experience[J].AJR,2007,189:799-806.
6.Girometti R,Furlan A,Esposito G,et a1.Relevance of b-values in evaluating liver fibrosis:a study in healthy and cirrhotic subjects using two single-shot spin-echo echoplanar diffusion-weighted sequences[J].J Magn Reson Imaging,2008,28:411-419.
7.Wang K, Wang PJ, Zhao ZH. FunctionalMR Iin chronic liver disease of hepatitis b patients[J]. Zhonghua Gan Bing Za Zhi,2006,14(8)∶590-596.
8.孙骏,施裕新,张志勇. MR扩散加权成像对肝纤维化诊断的初探[J].中国CT和MRI杂志,2008,6(6):35-38.
9.杨正汉,谢敬霞等.肝纤维化的磁共振扩散加权成像研究[J].中国医学影像技术,2002,18(9):907-909.
10.杨涛,王秀荣,杨广夫,等.磁共振扩散加权成像在肝脏疾病诊断中应用价值[J].中国CT和MRI杂志,2008,6(4):32-35.
11.Gibbons GH, Dzau V J. The emerging concept of vascular remodeling[J].N E ngl JM ed,1994,330(20):1431-1438.
12.Selcuk D, DemirelK. Gamna- Gandy bodies: A sign of portal hypertension[J]. Turk J Gastroenterol,2005,16(3):150-152.
13.Do RK,Chandarana H, Felker E,et al.Diagnosis of liver fibrosis and cirrhosis with diffusion-weighted imaging: value of normalized apparent diffusion coefficient using the spleen as reference organ[J].AJR,2010,195:671-676.

