2,3-丁二醇分离纯化中反应精馏的实验和模拟
刘佳娴,朱家文,吴艳阳,李琰君
(华东理工大学化学工程研究所,上海 200237)
2,3-丁二醇分离纯化中反应精馏的实验和模拟
刘佳娴,朱家文,吴艳阳,李琰君
(华东理工大学化学工程研究所,上海 200237)
对反应萃取-水解精馏法分离发酵液中2,3-丁二醇工艺中的水解精馏进行了实验和模拟研究。实验验证了4,5-二甲基-2-丙基-1,3-二氧戊环(DPD)水解精馏得到2,3-丁二醇的可行性。采用Aspen Plus建立反应精馏模型,以UNIFAC为热力学方程,RadFrac为反应精馏模块,对常压下DPD的水解精馏进行模拟,模拟结果与实验结果吻合较好。以2,3-丁二醇的收率为主要优化目标,考察最佳塔板数、进料位置、进料比、回流比和塔顶馏出比。模拟结果表明,在最佳操作条件下,塔釜2,3-丁二醇的收率为0.981,摩尔分率为0.150。
2,3-丁二醇 反应精馏 过程模拟 分离纯化
2,3-丁二醇(2,3-butanediol, 2,3-BD)是一种应用广泛的大宗化学品,所涉及的领域有化工、食品、航空航天等[1-3],其生产方法主要有化学合成法和微生物转化法。传统的化学合成法以石油制品为原料,工艺成本高、能耗大、污染重,不符合可持续发展原则[4]。随着石油资源的日益枯竭,微生物发酵法逐渐引起人们的关注。以糖质为原料,利用微生物的代谢将五碳糖或六碳糖转化为2,3-丁二醇,条件温和,污染少,更具竞争力和应用价值[5]。2,3-丁二醇对于微生物产生的毒性小于其他醇类[6],因此更加适合使用生物发酵法生产。但是2,3-丁二醇亲水性较强且沸点高,而发酵液中又含有多种表面活性物质和易结焦物质,成分复杂,使发酵生产2,3-丁二醇的下游分离困难,制约其大规模工业化生产。盐析分离法[7]利用无机盐对有机物的盐析作用,减少2,3-丁二醇在水中的溶解度,但是需要对发酵液进行预浓缩并且消耗大量无机盐;真空精馏法通过提高真空度降低2,3-丁二醇的沸点,但发酵液中的不溶物或固体颗粒浓缩成粘稠厚重的物质,阻碍了2,3-丁二醇的正常气化[8]。前期工作[9-12]在传统溶剂萃取法的基础上,分别选用正丁醇、乙酸丁酯和乙酸乙酯作为萃取剂,研究了水-2,3-丁二醇-萃取剂体系的液液相平衡和二元交互参数,提出采用溶剂萃取-共沸精馏工艺[13],通过共沸精馏以低能耗在脱除萃取剂的同时脱除产品中的水,简化了后续分离步骤,但该法仍需消耗大量有机溶剂,分离成本偏高。
二醇可以和醛类物质发生缩醛反应[14,15],通过可逆成环缩醛反应可以有效地将羟基暂时屏蔽,所得产物为环状的缩醛,很容易被有机溶剂萃取[16,17]。前期实验证明,采用反应与分离耦合的方法分离发酵液中的2,3-丁二醇,在pH值为1的盐酸催化下,以正丁醛为反应剂和萃取剂,与发酵液中的2,3-丁二醇进行反应生成4,5-二甲基-2-丙基-1,3-二氧戊环(4,5-dimethyl-2-propyl-1,3-dioxolane,以下简称DPD),DPD同时可被过量的正丁醇萃取。在室温、常压下就能得到较高的反应转化率和收率,反应见方程式(1)。
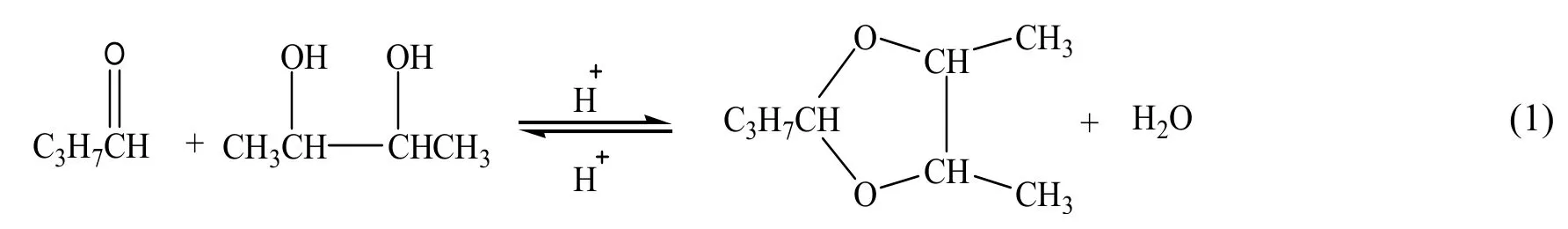
生成缩醛的反应很容易进行,因此作为逆反应的水解反应平衡转化率非常低,需要采用合适的反应条件或工艺流程,如水解精馏法。本工作对以反应分离耦合法纯化发酵液中2,3-丁二醇工艺中的水解精馏部分进行研究。通过实验证实反应精馏水解DPD生成2,3-丁二醇的可行性,在此基础上采用Aspen Plus软件建立模型,对DPD的水解精馏进行模拟分析,确定最佳塔板数、进料位置、进料比、回流比和塔顶馏出比,为整个工艺的工业化应用提供参考。
1 反应精馏实验
采用自行设计的小型填料塔进行水解精馏,塔径为0.028 m,填料高度为0.25 m,填料材质为拉西环状沸石,再沸器的功率为75 W,进料位置为填料高度1/2处,实验装置如图1所示。
采用乙醇-水体系对精馏塔的理论塔板数进行估算,得出全塔理论板数为 4,则进料板为第 2块板。以 2,3-丁二醇的收率为优化目标,在常压下对DPD的水解精馏进行考察,得出的较优操作条件为进料流量0.25 kg/h,塔身加热电压125 V,回流比为1.5,进料水油比(水与含90%DPD和10%正丁醛的油相的质量比)为1.2。

图1 精馏装置Fig.1 Rectification equipment
2 反应精馏模型的建立
Aspen数据库中没有收录DPD的相关物性,故使用Aspen的物性估算功能对其物性进行模拟,所用的估算方法均为基团贡献法。模拟所得DPD的主要物性参数如表1所示。
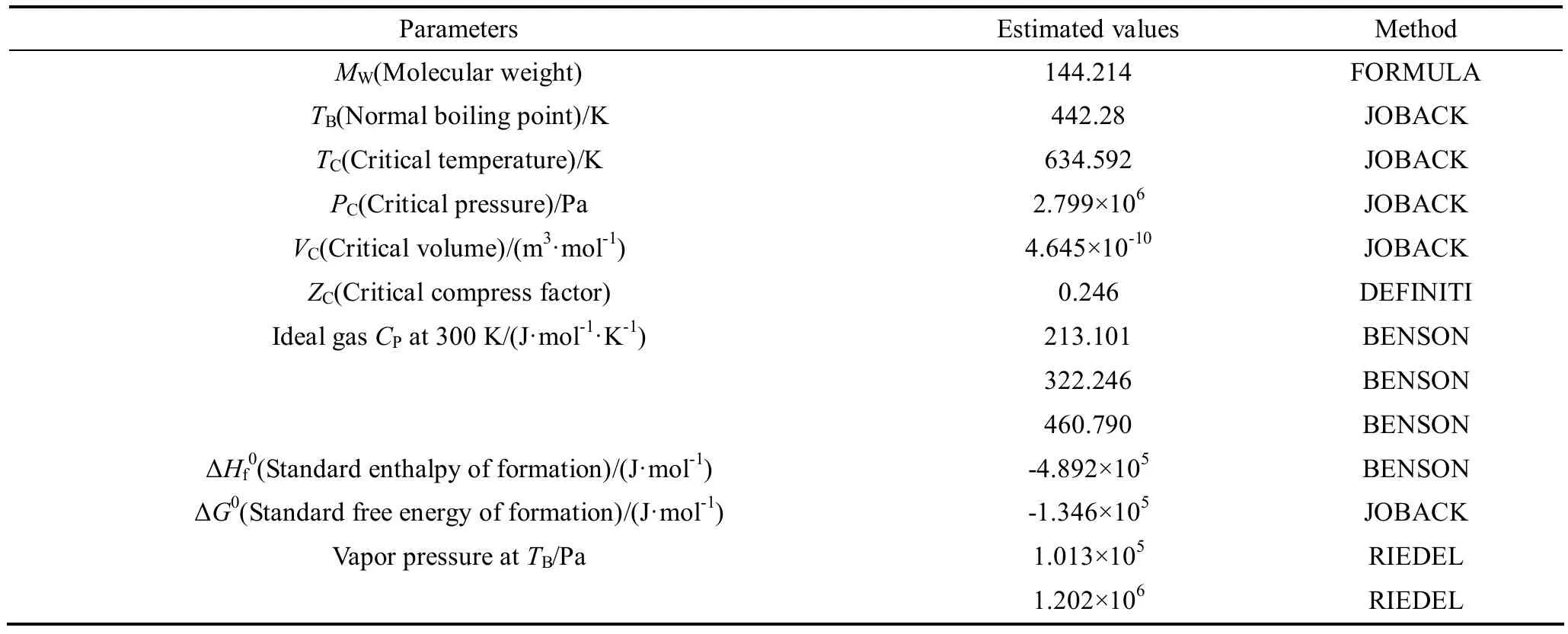
表1 DPD物性模拟结果Table1 Results of property estimation of DPD
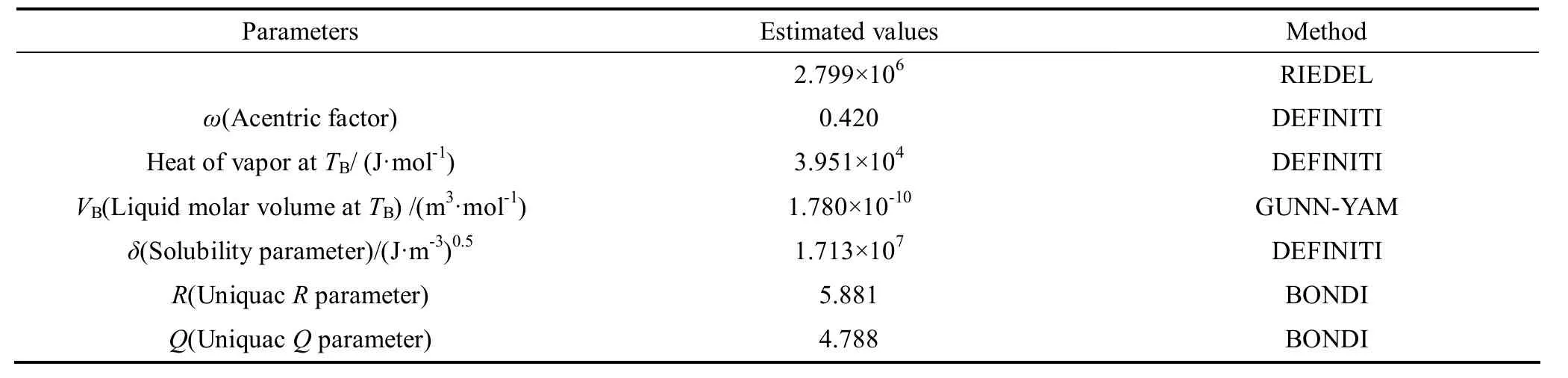
续表1
在缺乏二元交互参数的条件下,选用UNIFAC为热力学模型,得出水与DPD在369 K左右有最低共沸,水的共沸组成为0.95左右。以RadFrac模块对DPD的水解精馏进行模拟。
对较佳实验条件下的DPD水解精馏过程进行模拟,根据前期实验结果,缩醛反应动力学方程为:k1=1.93×1010exp(-64 540/(RT));水解反应动力学方程:k2=1.85×1012exp(-91 950/(RT))。在实际精馏过程中,由于各组分间的相互作用,催化剂盐酸的浓度在塔内分布并不是均一的,而是随着塔高变化。但在后续模拟的过程中,发现反应段只集中在进料位置附近的几块板上,因此为了简化模型,忽略塔内催化剂浓度变化对反应精馏的影响。由表2可以看出模拟所得的收率比实验值小。其原因有二:第一,在实际精馏过程中由于塔顶附近保温不理想,导致液相回流加大,实际回流比设定的回流比大,从而分离效果提高,使DPD在塔顶的损失小,产品收率上升;第二,实验时为了补偿塔身的温度损失,在塔身上加有外加热源,使得实际反应温度可能高于模拟值,导致水解反应更为迅速彻底,因此实验所得DPD在塔釜的含量比模拟值低,也会导致总收率上升。即便如此,模拟得出的其他参数仍然与实验值的拟合性较好,说明用该模型对DPD的水解精馏做出设计型计算是比较可靠的。
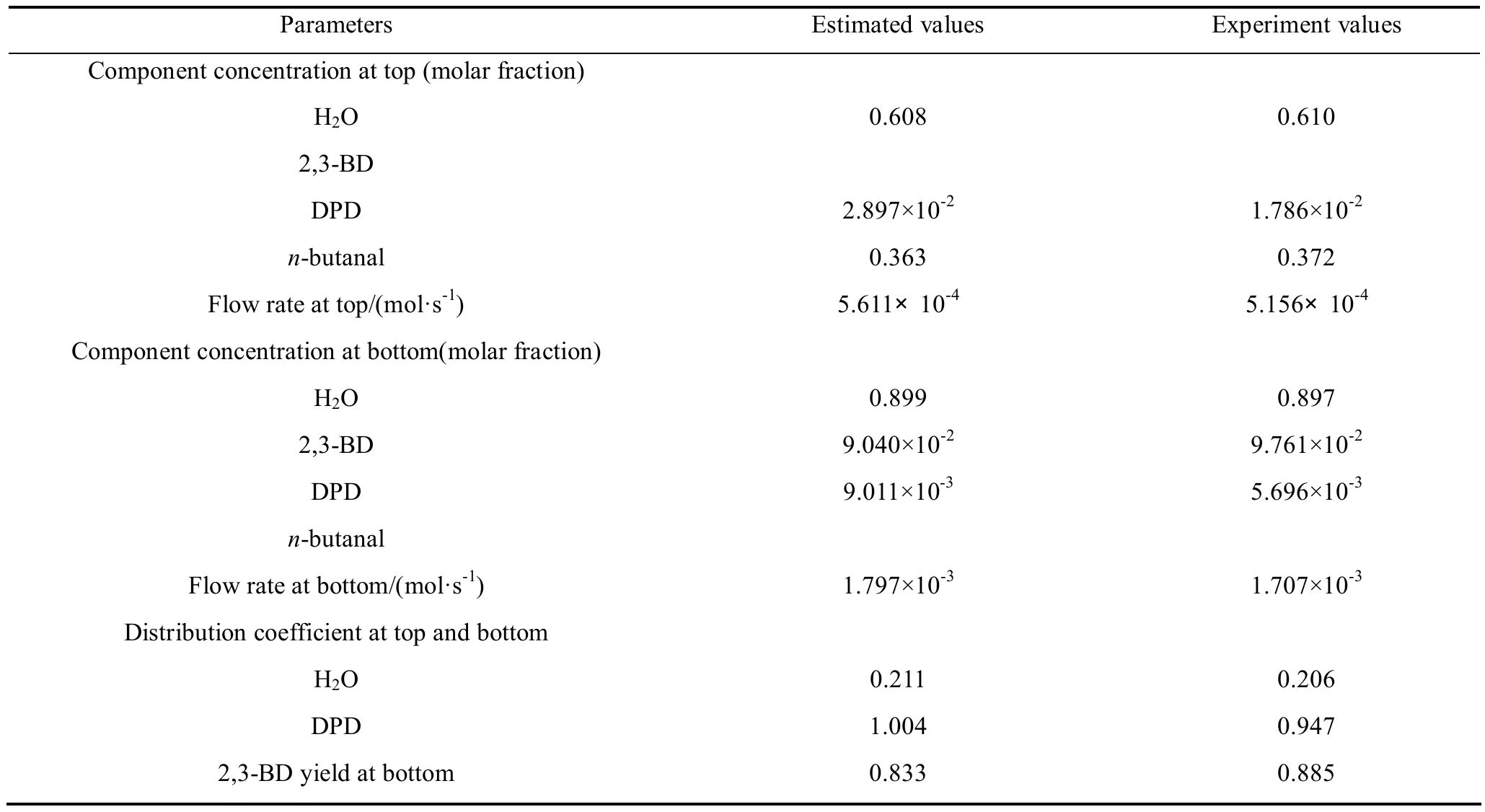
表2 水解精馏的实验结果与模拟值比较Table 2 Comparison of experimental and simulation results of reactive distillation
3 反应精馏过程设计型计算
3.1 塔板数确定
要得到较高的反应转化率,使反应产物得到有效分离,必须有足够的理论板数,然而过多的理论板数会加大精馏塔的建造投资和再沸器能耗,因此必须在满足反应分离的基础上考察合理的理论板数。设定进料水油比为 1.2,回流比为 1.5,塔顶馏出比为0.3,塔顶压力为0.1 MPa。在RadFrac模型中,只有再沸器功率随进料流量呈等比例变化,其他参数不受进料流量影响,因此为方便起见,将进料流量设为1 kg/h。分别考察在不同塔板数下液相中2,3-丁二醇的浓度在不同塔板位置的分布,进料位置均为塔板数的1/2处,模拟结果如图2所示。
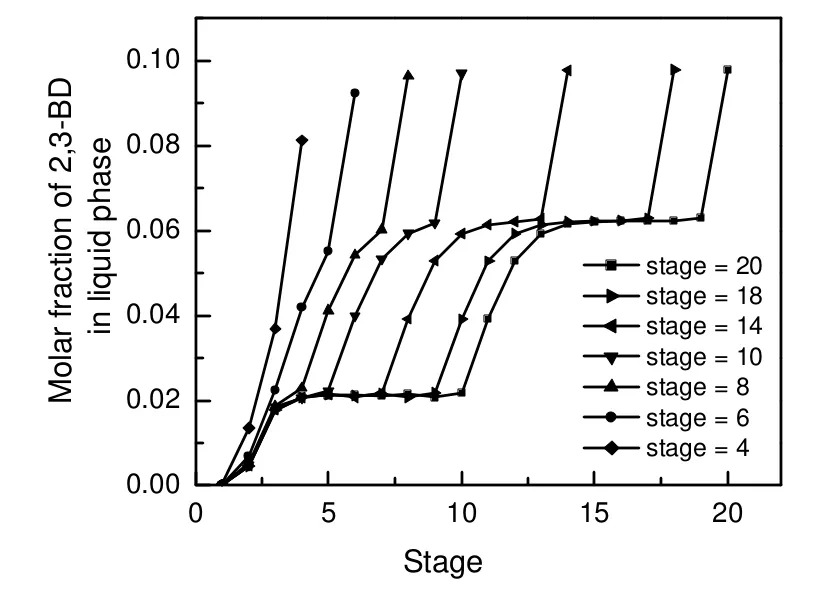
图2 不同板数时塔内2,3-丁二醇的液相浓度分布Fig.2 Distribution of 2,3-BD liquid concentration in different column with different stages
仅在塔板数少于8的情况下塔釜产品浓度随塔板数的减小有相对明显的变化,2,3-丁二醇浓度变化最大处在进料板附近的几块板之间,在低于进料板处5块理论板之下,2,3-丁二醇浓度基本不随塔高变化,仅在塔釜才突然增高。这表明在该水解精馏中,反应是影响该过程的主导因素,在保证必要的反应板数的情况下,想要通过增加塔板数的方法增加塔釜产品的浓度和收率是不可行的。对反应分离效果起关键作用的是进料板附近的几块板。考虑到再沸器功率会随着塔高的增加而上升,将塔板数设为10。
3.2 进料位置设定
在塔板数为10的情况下,分别模拟不同进料位置对反应分离效果的影响,结果如图3所示。由图3可知,总体上2,3-丁二醇的塔釜收率和浓度均随着进料位置的下降而减小,但是两条曲线都在进料板为第3块理论板处有小的波动。这是因为当进料板为第3块板时,第4块板的温度十分接近水与DPD的共沸点,因此更多的DPD以水的最低共沸物形式被蒸出塔顶,导致可参与反应的DPD减少。考虑到在实际操作中进料板为2时,精馏段较短,物系可能得不到有效分离,故将进料设在第4块理论板的位置上。
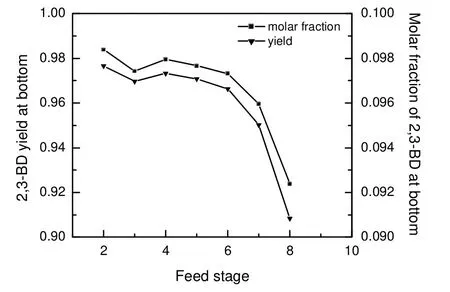
图3 塔釜2,3-丁二醇收率和浓度随进料位置的变化Fig.3 Variation of yield and concentration of 2,3-butanediol at bottom and feed stage
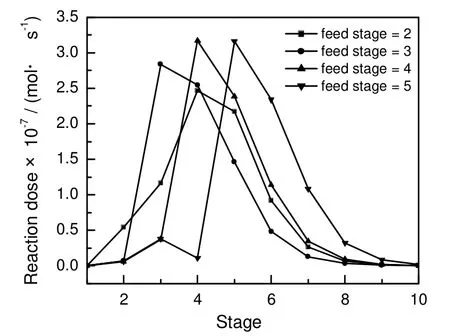
图4 在不同板进料时塔内的反应量分布Fig.4 Distribution of reaction dose in column with different feed stage
图4为进料位置变化对反应量分布的影响。由于第2块板接近冷凝器,温度不够高,而DPD的水解是吸热反应,故在该板处的反应量不大。当进料板为第2块板时,料液在重力作用下向塔下部移动,到第3块板才有较为明显的反应。这是因为从第3块板开始,塔板温度才达到DPD水解所需要的温度。当进料板为第3块板时,由于进料是液相,进料板上反应物浓度最大,反应量也最大,导致反应产物2,3-丁二醇在该处附近的浓度较高。由于此处距塔顶较近,一部分2,3-丁二醇由于分离不完全经塔顶馏出,造成损失,塔釜收率下降。当进料板为第4块板时,进料口到塔顶间的板数增多,对2,3-丁二醇的分离效果更好,使2,3-丁二醇在塔顶的馏出量减小,塔釜收率上升。当进料板继续下移,主要反应段也随之下移,DPD作为第二重组分在塔釜的滞留量增加,水解不完全引起收率下降。在进料位置低于第3块板时,第3块板上的反应均量略有上升,是因为塔顶液相回流中的DPD继续参与了水解反应。
当进料在第2块板和第4块板时,塔釜的产品收率和浓度都较进料在第3块板高。但进料板为2时,反应段较长,在实际操作中物系可能得不到有效分离,故将进料设在第4块理论板的位置上。
3.3 回流比、进料比和馏出比确定
传统的分离过程中,回流比越大分离效果越好。但是在反应精馏中,回流比过大会使塔顶附近某一组分的浓度上升,从而影响整个塔的浓度分布,可能导致水解平衡逆向移动。理论上来说,进料中水油比越大,水解越完全,塔釜2,3-丁二醇的收率越高。但是当水过量较多时,水解产生的正丁醛浓度减小,而塔顶馏出比保持不变,此时作为沸点第二低的组分,水会被蒸出塔顶,同时带走与其共沸的 DPD,引起产品收率降低。馏出比对水解精馏的影响存在正反两方面:一方面是增大馏出比可以使水解产物正丁醛尽快被分离出反应体系,从而使反应平衡正向移动,收率升高;另一方面是增大馏出比使塔顶水含量增加,从而使塔顶DPD也增加,总收率降低。回流比、进料比和馏出比之间是相互影响的,在确定最佳操作因素时,需将三者共同考虑。
图5为回流比、进料比和馏出比共同变化时塔釜2,3-丁二醇收率、浓度和再沸器功率变化的模拟结果,其中塔釜收率是首要的生产指标,需要在保证其值较高的情况下再考虑另外两个因素。
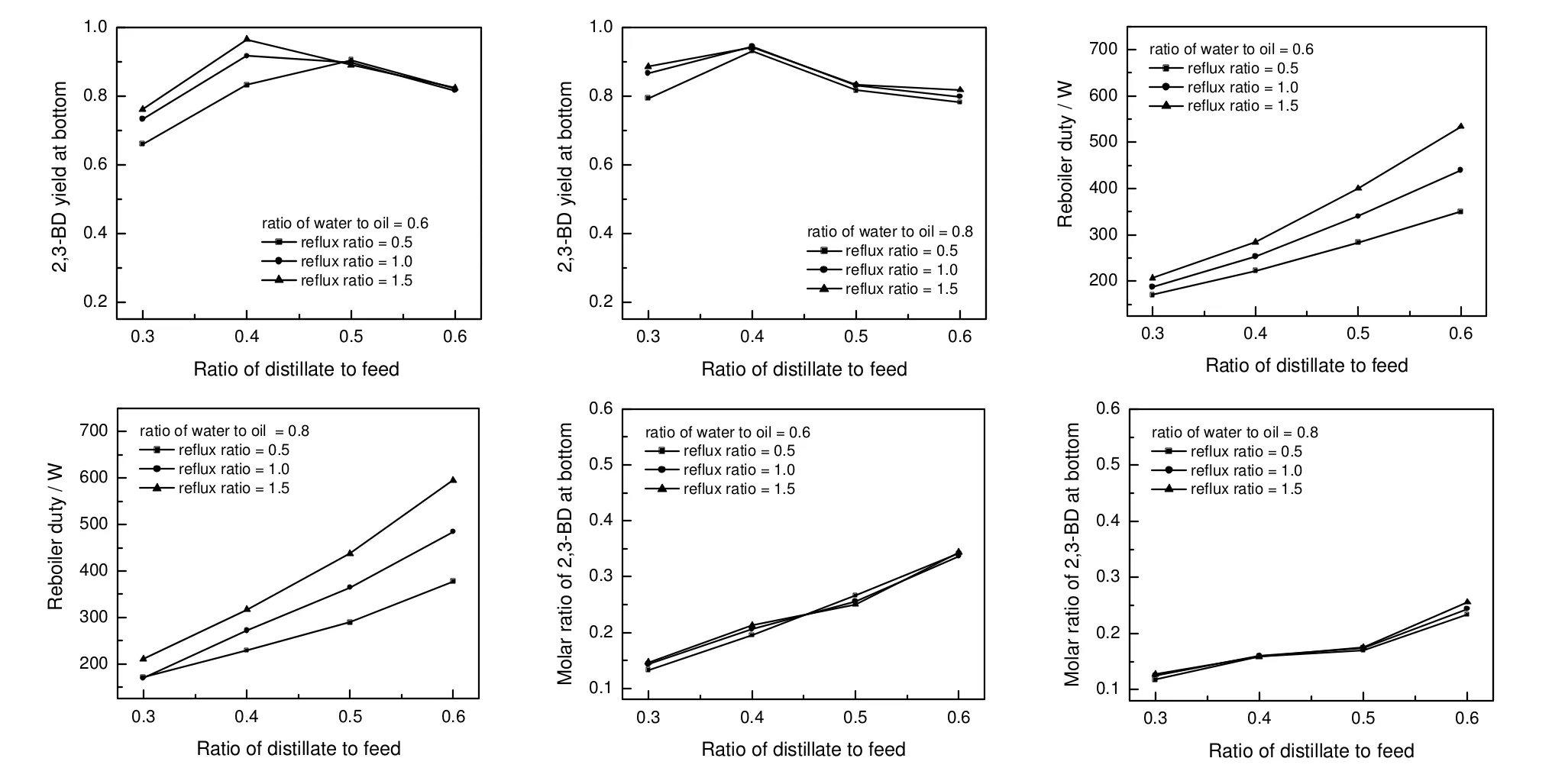
图5 不同回流比下塔釜2,3-丁二醇收率、浓度和再沸器功率随馏出比和进料水油比的变化Fig.5 Variation of 2,3-BD yield, concentration and reboiler power at bottom with ratio of distillate to feed and ratio of water to oil in feed at different reflux ratio
图5显示水油比为0.6和0.8时,在馏出比为0.4附近可以获得较高的收率。为了进一步提高收率,在这两点附近进行再次优化,得出结果见表3。由表3可知,想要提高产品浓度,需要以提高能耗或者降低产品收率为代价,具体操作可以根据生产时的不同需求来决定。

表3 水解精馏模拟优化结果Table 3 Optimal results of simulation of hydrolysis distillation
3.4 灵敏板确定
图6和图7分别为回流比为1.5时塔内各组分液相浓度分布和回流比分别为1.0,1.5和2.0时塔内温度分布的模拟结果。可以看出在第3块理论板处,水和DPD的浓度和液相总体流率的变化都最为剧烈,且该板处的温度较其他位置有较为明显的突变,因此在实际操作中可将第3块板视为灵敏板,通过控制灵敏板的温度来调节塔顶组分含量。在实验操作中正是因为第3块塔板处的温度比模拟值低,才造成塔顶DPD的含量比模拟值低,从而总收率比模拟值高。
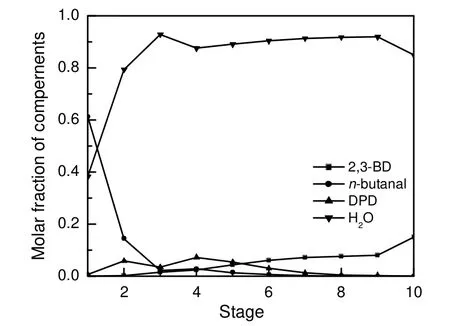
图6 塔中各板处液相浓度分布Fig.6 Distribution of concentration in liquid phase at different stage
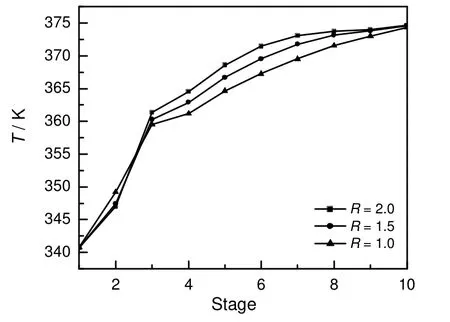
图7 不同回流比下塔中温度分布Fig.7 Distribution of temperature in column at different reflux ratio
4 结 论
以盐酸为催化剂,对正丁醛与发酵液中的2,3-丁二醇反应萃取所得产物DPD在反应精馏塔中进行水解,水相pH为1。在实验的基础上使用Aspen Plus软件建立水解精馏塔模型,以UNIFAC为热力学模型,以RadFrac模型作为反应精馏模块,采用基团贡献法模拟DPD的物性参数,模拟结果与实验结果拟合程度较好。用该模型对DPD的水解精馏进行设计型模拟,以塔釜2,3-丁二醇的收率为主要生产指标,同时优化再沸器功率和塔釜2,3-丁二醇的浓度。通过模拟得出最佳塔板数为10,最佳进料位置为第4块理论板,较优进料水油比、回流比和塔顶对进料的馏出比分别为0.8,1.5和0.35,塔釜2,3-丁二醇的收率可达0.981,摩尔分率可达0.150,同时再沸器功率较低。在实际应用中,为了进一步提高收率,可以采用控制灵敏板温度的方法,影响塔顶附近DPD与水的共沸,从而使DPD的塔顶含量减小,提高水解转化率。
[1]Faveri P, Torre F, Molinari P, et al. Carbon material balances and bioenergetics of 2,3-butanediol bio-oxidation by acetobacter hansenii[J].Enzyme Microb Technol, 2003, 33: 708-719.
[2]van Haveren J, Scott E L, Sanders J. Bulk chemicals from biomass[J]. Biofuels Bioprod Bioref, 2008, 2: 41-57.
[3]蒋丽群, 郭 峰, 方 真, 等. 微生物发酵法生产2,3-丁二醇的研究[J]. 化学与生物工程, 2011, 28(6): 25-28.Jiang Liqun, Guo Feng, Fang Zhen, et al. Production of 2,3-butanediol by microorganism fermentation[J]. Chemistry & Bioengineering, 2011,28(6): 25-28.
[4]吴艳阳, 朱家文, 陈 葵, 等. 生物基化学品2,3-丁二醇分离纯化的研究[D]. 上海: 华东理工大学化工学院, 2008.
[5]Jia Xiaojun, Huang He, Ouyang Pingkai. Microbial 2,3-butanediol production: A state-of-the-art review[J]. Biotechnology Advances, 2011,29(3): 351-364.
[6]Converti A, Perego P. Use of carbon and energy balances in the study of the anaerobic metabolism ofEnterobacter aerogenesat variable starting glucose concentrations[J]. Appl Microbiol Biotechnol, 2002, 59: 303-309.
[7]Afschar A S, Vaz Rossell C E, Jonas R, et al. Microbial production and downstream process of 2,3-butanediol[J]. Journal of Biotechnology,1993, 27(3): 317-329.
[8]Garg S K, Jain A. Fermentative production of 2,3-butanediol: a review[J]. Bioresource Technology, 1995, 51(2): 103-109.
[9]Wu Yanyang, Zhu Jiawen, Chen Kui, et al. Liquid-liquid equilibria of water+2,3-butanediol+1-butanol atT=298.15 K,T=308.15 K andT=318.15 K[J]. Fluid Phase Equilibria, 2008, 265(1/2): 1-6.
[10]Wu Yanyang, Zhu Jiawen, Chen Kui, et al. Liquid-liquid equilibiria of water+2,3-butanediol+butyl acetate atT=298.15 K,T=308.15 K andT=318.1 K[J]. J Chem Eng Data, 2008, 53(2): 559-563.
[11]Wu Yanyang, Zhu Jiawen, Chen Kui, et al. Liquid-liquid equilibria of water+2,3-butanediol+ethyl acetate at several temperatures[J]. Fluid Phase Equilibria, 2008, 266(1/2): 42-46.
[12]Wu Yanyang, Zhu Jiawen, Chen Kui, et al. Vapor-liquid equilibria for the binary mixtures of 2,3-butanediol withn-butanol,n-butyl acetate and ethyl acetate at 101.3 KPa[J]. Fluid Phase Equilibria, 2007, 262: 169-173.
[13]吴艳阳,朱家文,陈 葵,等. 2,3-丁二醇萃取-精馏耦合工艺开发研究[J]. 化学工程, 2011, 39(8): 90-94,102.Wu Yanyang, Zhu Jiawen, Chen Kui, et al. Development and study on extraction coupled distillation technology for 2,3-butanediol separation[J]. Chemical Engineering (China), 2011, 39(8): 90-94,102.
[14]Flory P J. Statistical mechanics of reversible reactions of neighboring pairs of substituents in linear polymers[J]. J Am Chem Soc, 1950, 72(11):5052-5055.
[15]Broekhuis R R, Lynn S, King C J. Recovery of propylene glycol from dilute aqueous solutions via reversible reaction with aldehydes[J]. Ind Eng Chem Res, 1994, 33: 3230-3237.
[16]向波涛, 陈书锋, 刘德华. 发酵液中1,3-丙二醇的萃取分离[J]. 清华大学学报自然科学版, 2001, 41(12): 53-55.Xiang Botao, Chen Shufeng, Liu Dehua. Extraction of 1,3-propanediol in dilute fermentation broth[J]. J Tsinghua Univ (Sci & Tech), 2001,41(12): 53-55.
[17]张慧敏, 李 彦, 钱 倩. 反应萃取耦合法分离1,3-丙二醇中缩醛反应的研究[J]. 化学反应工程与工艺, 2005, 21(6): 551-555.Zhang Huimin, Li Yan, Qian Qian. Acetal reaction in separation of 1,3-propanediol by coupling method of reaction-extraction[J]. Chemical Reaction Engineering and Technology, 2005, 21(6): 551-555.
Experiment and Simulation of Reactive Distillation for 2,3-butanediol Separation from Fermentation Broth
Liu Jiaxian, Zhu Jiawen, Wu Yanyang, Li Yanjun
(Chemical Engineering Research Centre, East China University of Science and Technology, Shanghai 200237, China)
The hydrolysis distillation for separation of 2,3-butanediol from fermentation broth by reactive extraction-hydrolysis distillation method was studied by experiment and simulation. The feasibility of 4,5-dimethyl-2-propyl-1,3-dioxolane(DPD) hydrolysis in reactive distillation column was investigated by experiment and the model of reactive distillation was established by Aspen Plus. UNIFAC equation was used as thermodynamics method and RadFrac module was applied. The results of simulation were fitted with experiment which implied that the model was reliable. Hydrolysis distillation column was designed on the basis of the established model. Appropriate stage number, feed stage, ratio of water to oil in feed, reflux ratio and ratio of distillate to feed were determined. Under the optimum operate conditions, 0.981 of 2,3-butanediol yield at bottom and 0.15 of 2,3-butanediol molar fraction at bottom could be obtained while the reboiler duty was low.
2,3-butanediol; reactive distillation; process simulation; separation
TQ028;TQ031.5;TQ413.25 文献标识码:A
1001—7631 ( 2012 ) 02—0104—07
2011-12-31;
2012-03-19
刘佳娴(1985-),女,硕士研究生;吴艳阳(1979-),女,讲师,通讯联系人。E-mail: wyywitty@ecust.edu.cn
国家自然科学基金项目(21106039)

