溶胶-凝胶-水热晶化法制备锐钛矿TiO2纳米膜的耐蚀性能
云 虹 林昌健 杜荣归
(1厦门大学化学化工学院化学系,固体表面物理化学国家重点实验室,福建厦门361005;
2上海高校电力腐蚀控制与应用电化学重点实验室,上海电力学院能源与环境工程学院,上海200090)
溶胶-凝胶-水热晶化法制备锐钛矿TiO2纳米膜的耐蚀性能
云 虹1,2林昌健1,*杜荣归1
(1厦门大学化学化工学院化学系,固体表面物理化学国家重点实验室,福建厦门361005;
2上海高校电力腐蚀控制与应用电化学重点实验室,上海电力学院能源与环境工程学院,上海200090)
以钛酸正丁酯为前驱体,采用溶胶-凝胶-水热晶化法在不锈钢(SS)表面制备TiO2纳米膜.利用X射线衍射(XRD)、Raman光谱、场发射扫描电子显微镜(SEM)、原子力显微镜(AFM)和俄歇电子能谱(AES)表征了TiO2纳米膜的晶型、表面形貌和表面化学组成.通过极化曲线和电化学阻抗谱(EIS)研究了TiO2纳米膜的耐蚀性能. 170°C下水热晶化制备的锐钛矿TiO2与450°C焙烧制备的锐钛矿TiO2的结晶度类似,但两种TiO2薄膜的表面结构存在明显差异,水热晶化法制备的TiO2纳米膜在3.5%(w)NaCl溶液中的耐蚀性能优于焙烧法制备的.
水热晶化;锐钛矿TiO2;腐蚀与防护
1 引言
TiO2因稳定性好、抗高温氧化和价廉无毒,在金属保护方面受到特别的关注.1-3采用溶胶-凝胶法在金属基体表面涂覆TiO2薄膜可有效提高金属基体的耐蚀性.4-6TiO2在自然界有三种结晶态:锐钛矿型、金红石型和板钛矿型.鉴于锐钛矿型TiO2的性能好而应用广泛,这方面的研究多数采用锐钛矿型TiO2.为了制备锐钛矿型TiO2,通常采用高温焙烧的方法.焙烧一般在400°C以上进行,高温一方面促进了TiO2由非晶态向锐钛矿晶体的转变,另一方面可能向也导致周围气氛排放CO2(来源于溶胶中的有机溶剂和钛醇盐)等污染环境的副产物.7,8因此,有必要采用一种环境友好的可在温和条件下制备锐钛矿型TiO2的方法.水热反应是在密闭容器中、在温度低于250°C下进行,属于一种环境友好、成本低廉且操作简便的合成方法.利用水热反应促使一些非晶化合物脱水结晶而得到晶型化合物的方法,称为水热晶化法.近来,通过水热晶化法制备具有一定晶型的TiO2材料颇受人们的关注,9-17在光催化降解污染物领域已有广泛的应用.研究表明,采用此法得到的锐钛矿型TiO2在光催化降解污染物领域表现出优越的光催化性能.18-24对相同的目标降解物,最佳水热晶化条件制备的锐钛矿型TiO2的光催化活性明显高于商品化的Degussa P25(锐钛矿型和金红石型混合的TiO2).25-28此外,水热晶化法制备的锐钛矿型TiO2在太阳能电池、29-31锂离子电池32和生物医用材料33等领域也有一定的应用.然而,关于水热晶化法制备锐钛矿型TiO2应用于钢铁防腐蚀的研究鲜有报道.
本工作采用溶胶-凝胶-水热晶化法在不锈钢表面构筑锐钛矿型TiO2纳米膜,运用腐蚀电化学方法考察TiO2纳米膜在3.5%(w)NaCl溶液中的耐蚀性能,并与高温焙烧制备的锐钛矿型TiO2纳米膜的性能进行比较分析,以期揭示TiO2增强不锈钢基体防腐蚀性能的机制.
2 实验部分
2.1 锐钛矿型TiO2纳米膜的制备
以钛酸正丁酯为前驱体,无水乙醇为溶剂,乙酰乙酸乙酯为螯合剂,制备稳定的黄色透明TiO2溶胶.6以316L SS(1 cm×3 cm×0.1 cm)不锈钢为金属基体材料,分别用400#-1500#水磨砂纸和1.0µm的Al2O3抛光粉机械打磨表面成镜面,再依次用丙酮、无水乙醇、去离子水超声清洗.采用浸渍-提拉法在316L SS表面构筑TiO2薄膜.过程如下:自制提拉机以0.5-1 mm·s-1的速率匀速提拉,在金属基体表面构筑一层均匀的薄膜,自然干燥,在100°C下干燥10 min,重复操作4次得到一定厚度的TiO2薄膜.将得到的TiO2/316L SS置入聚四氟乙烯反应釡内,以去离子水为反应介质,体积填充度为80%,在170°C下反应4 h,取出清洗干燥即可.采用水热晶化法制备的结晶态TiO2样品标记为H-TiO2.为了对比,另一组采用相同溶胶-凝胶过程得到的TiO2/316L SS样品在空气中450°C下焙烧2 h制备结晶态TiO2,对应的标记为C-TiO2.
2.2 TiO2纳米膜的表征
采用日本HITACHI公司LEO-1530场发射高倍电子扫描电镜(SEM)观察纳米膜的形貌.采用德国SIS公司的ULRA Objective扫描探针仪进行AFM实验,在非接触模式下表征样品的表面形貌和表面粗糙度.分别采用XRD和Raman光谱表征TiO2的晶型.XRD测试采用荷兰Philips公司的panalytical X′pert转靶X射线粉末衍射仪.Raman光谱使用Renishaw UV-Vis Raman System 1000R,Ar+激光的强绿线作光源,激光波长514.5 nm,功率100 mW.俄歇电子能谱(AES)分析在PHI 660 SAM上进行,电子束压为5.0 kV,束流为100 nA,分析室真空度优于1.3×10-7Pa,Ar+离子溅射速率为10 nm·min-1.
2.3 电化学测试
电化学测试采用荷兰Autolab PGSTAT30电化学工作站.电解池为三电极体系,工作电极为TiO2/ 316L SS膜电极,辅助电极为Pt电极,参比电极为饱和甘汞电极(SCE),电解液为3.5%(w)NaCl溶液.极化曲线测试电位范围在自然腐蚀电位附近±250 mV,扫描速度为0.167 mV·s-1.EIS测试在开路电位下进行,扰动电压10 mV,频率范围为105-10-3Hz.测试均在室温下,在Faraday屏蔽箱中进行,以避免外界电磁干扰.

图1 316LSS表面不同TiO2薄膜的Raman光谱Fig.1 Raman spectra of different TiO2films on the surface of 316LSS(a)TiO2/316L SS via sol-gel and hydrothermal reaction at 170°C for 4 h(H-TiO2/316L SS),(b)TiO2/316L SS via sol-gel and calcination at450°C for 2 h(C-TiO2/316L SS),(c)TiO2/316L SS via sol-gel
3 结果与讨论
3.1 TiO2薄膜的晶型
图1是316L SS表面不同TiO2薄膜的Raman图谱.从图中可见,位于147、198、398、517和639 cm-1的Raman峰,与锐钛矿型TiO2的晶格振动模式一一对应,表明两种方法制备的TiO2均为锐钛矿型,图中未发现其他TiO2结晶态的Raman峰,表明样品为单一锐钛矿型,纯度高.Raman散射峰强度与TiO2薄膜的结晶程度相对应.比较可见,经170°C水热晶化4 h得到的TiO2的结晶度与450°C下焙烧2 h得到的相近.图1c为采用溶胶-凝胶法在316L SS表面未经任何处理的TiO2薄膜的Raman谱,没有明显的Raman散射峰,表明其为无定形TiO2.Raman光谱是一种有效表征氧化物结晶形态的分析技术,也适合于分析基体表面的氧化物薄膜.与XRD分析相比,可避免某些基体材料对薄膜的影响.在XRD分析中,经450°C焙烧2 h制备的TiO2的XRD谱图(文中未给出)上仅出现较弱的锐钛矿型TiO2(101)面的衍射峰,这并不意味着TiO2的晶型较差,是由于316L SS基体材料信号的干扰和薄膜较薄.水热晶化法得到的TiO2样品的XRD测试也得到类似的结果.可见,运用Raman光谱表征制备TiO2薄膜的晶型较合适.
3.2 TiO2薄膜在3.5%(w)NaCl溶液中的耐蚀性能

图2 316LSS和TiO2/316LSS电极在3.5%(w)NaCl溶液中的极化曲线Fig.2 Polarization curves for 316LSS and TiO2/316LSS electrodes in 3.5%(w)NaCl solution(a)H-TiO2/316L SS,(b)C-TiO2/316L SS,(c)316L SS
图2为316L SS、H-TiO2/316L SS和C-TiO2/ 316L SS膜电极在3.5%(w)NaCl溶液中的极化曲线.可以看到,两种TiO2薄膜电极表现出相似的阳极极化和阴极极化行为.与316L SS相比,H-TiO2/ 316L SS和C-TiO2/316L SS膜电极的阳极极化曲线趋于平缓,具有较低的阳极极化电流,自然腐蚀电位都正移,表明H-TiO2/316L SS和C-TiO2/316L SS膜电极在溶液中处于钝化状态,涂覆TiO2薄膜的316L SS的防腐性能得到提高.比较之下,H-TiO2/ 316L SS膜电极的电位正移数值更大.一般认为,较正的腐蚀电位,意味着涂层具有较好的热力学阻挡层作用.这表明水热晶化法制备的TiO2薄膜在3.5%(w)NaCl溶液中具有更好的耐蚀性能.
图3为316L SS、H-TiO2/316L SS和C-TiO2/ 316L SS膜电极在3.5%(w)NaCl溶液中的电化学阻抗谱.两种TiO2薄膜电极的Nyquist图上都只出现一个圆弧,相比之下,水热晶化法得到的样品的圆弧半径较大,即阻抗较大,耐蚀性更好.在相同情况下,两个样品的Bode图存在明显差别.经焙烧得到的TiO2薄膜电极的Bode图上出现至少两个时间常数.水热晶化法得到样品的Bode图上低频容抗弧的半径显著增大,致使高频容抗弧难以分辨,表现为一个大的时间常数.通常,基体表面的薄膜对应的高频时间常数越小,在高频处的容抗弧半径也越小,表明薄膜与基体的结合性能更好,薄膜更致密.采用图4a所示的等效电路来拟合316L SS电极和水热晶化法制备的膜电极体系,采用图4b所示的等效电路拟合焙烧处理得到的膜电极体系.在等效电路中,Rs代表溶液电阻,Rt代表腐蚀反应的传递电阻,其数值的大小反映金属防腐蚀性能的强弱,Rc反映膜电阻的大小,Qc和Qdl分别代表膜电容和空间电荷层电容.经拟合计算,316L SS的传递电阻Rt为7.6× 105Ω·cm2,焙烧制备的TiO2薄膜的Rt为1.04×107Ω· cm2,而水热晶化法制备的TiO2薄膜的Rt为2.84×107Ω·cm2.经TiO2薄膜修饰后316L SS的耐蚀性能均有提高,水热晶化法制备的TiO2薄膜提高的幅度更显著.这与前面极化曲线分析得到的结果是一致的.
3.3 TiO2薄膜的表面结构
3.3.1 SEM表征
图5为316L SS表面不同TiO2薄膜的SEM图.在450°C焙烧处理2 h后,在TiO2薄膜表面出现密实的晶粒,晶粒呈规整的球形,平均颗粒直径约为25 nm(图5a).采用水热晶化法在170°C下处理4 h后得到的TiO2薄膜形貌发生了明显的变化.TiO2薄膜中TiO2为纳米立方形颗粒,在表面均匀分布且排列紧凑,尺寸范围为30-40 nm(图5b).
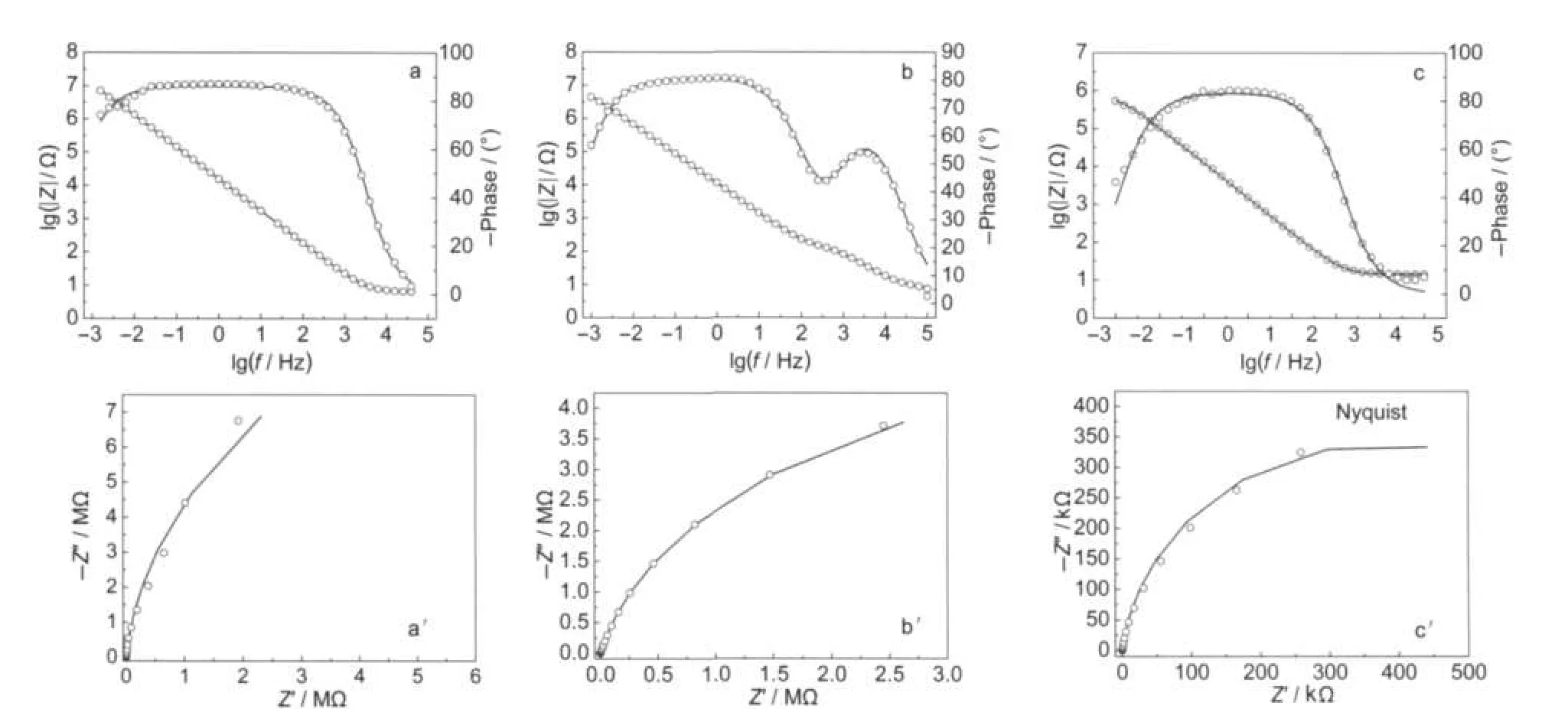
图3 316LSS和TiO2/316LSS电极在3.5%(w)NaCl溶液中的电化学阻抗谱Fig.3 EIS spectra for 316LSS and TiO2/316LSS electrodes in 3.5%(w)NaCl solution(a,a′)H-TiO2/316L SS,(b,b′)C-TiO2/316L SS,(c,c′)316L SS

图4 316LSS和TiO2/316LSS电极在3.5%(w)NaCl溶液中电化学阻抗谱的模拟电路Fig.4 Equivalent circuits for 316LSS and TiO2/316LSS electrodes in 3.5%(w)NaCl solution (a)H-TiO2/316L SS and 316L SS,(b)C-TiO2/316L SS

图5 316LSS表面不同TiO2纳米膜的SEM图Fig.5 SEM images of the nano TiO2films on the surface of 316LSS (a)C-TiO2/316L SS,(b)H-TiO2/316L SS
3.3.2 AFM表征
图6为不同TiO2薄膜的AFM三维图(高度模式).两种TiO2薄膜的表面形貌呈现明显的差别.采用水热晶化法制备的锐钛矿型TiO2表面由圆顶的连续岛形粒子构成,分布均匀(图6a).而采用焙烧法制备的TiO2表面由笋状突起排列而成,表面突起尺寸较大,膜层中有孔洞存在(图6b).利用AFM工作站的附带程序对两种TiO2薄膜的表面粗糙度进行分析,以轮廓最大高度Rymax和Rz及轮廓算术平均偏差Ra这三个参数来评定纳米级表面粗糙度.水热晶化法制备的TiO2薄膜的Rymax、Rz及Ra分别为4.26、3.06和0.618 nm,而焙烧方法制备的对应的数值分别为11.00、8.65和1.530 nm.水热晶化法制备的TiO2薄膜的表面粗糙度评定参数Rymax、Rz及Ra都明显小于焙烧方法制备的,这是其颗粒分布均匀且镶嵌密实的结果.

图6 不同TiO2纳米膜的AFM图Fig.6 AFM images of the different TiO2nano films (a)H-TiO2film,(b)C-TiO2film

图7 不同TiO2/316 LSS样品的AES深度剖析图Fig.7 AES depth profiles of the different TiO2/316LSS samples (a)H-TiO2/316L SS,(b)C-TiO2/316L SS
3.4 AES分析
为了解不同TiO2纳米膜的表面化学组成及薄膜的微结构,运用AES分析了两种方法制备的TiO2纳米膜.图7分别为316L SS表面采用水热晶化法和焙烧法制备的锐钛矿型TiO2纳米膜的AES深度剖析谱.可以看出,316L SS表面由氧化层和扩散层组成,氧化层主要是Ti和O,其中存在一定的C污染. C的来源可能有两个,一是真空度的限制,另一个可能是有机物未完全分解的残余.在氧化层中氧和钛的组成比例随着深度的增加基本保持不变,说明氧化层的组成分布均匀.比较之下,在氧化层中,水热晶化法得到样品中氧与钛的原子数比值大于焙烧法得到样品中氧与钛的原子数比值,其偏高的氧主要来自于表面羟基化作用.从图7a可见,在水热过程中,以少许Ti和O元素向基体的迁移扩散为主.从图7b可见,在焙烧条件下,主要是基体Fe元素向TiO2纳米膜的扩散.一般热处理的温度越高,时间越长,扩散现象越严重.焙烧法制备的样品中薄膜与基体间扩散层较宽,表明产生了较为严重的界面扩散,这一现象是高温处理导致的负面影响.34-36严重的界面扩散致使焙烧法制备的样品中氧化层的厚度相对减少,这可能是焙烧法制备的TiO2薄膜的耐蚀性弱于水热晶化法制备的一个因素.另一方面,热处理形成较宽的铁氧化物界面层和Fe元素大幅度向TiO2纳米膜扩散,必然影响TiO2纳米膜层的化学组成和界面结构,进而影响TiO2纳米膜在3.5% (w)NaCl溶液中的耐蚀性能.
4 结论
采用溶胶-凝胶-水热晶化法在316L SS表面制备了锐钛矿TiO2薄膜.水热晶化处理得到的TiO2薄膜表面结构、化学组成和界面结构不同于热处理制备的.170°C下水热晶化法制备的TiO2薄膜表面结构更致密,避免了高温焙烧时基体材料与TiO2薄膜严重的界面扩散反应,增强了TiO2薄膜在3.5%(w) NaCl溶液中对基体材料的保护性能.结果表明,水热晶化法是一种切实可行的制备结构完美锐钛矿TiO2膜层的方法,在金属防腐蚀等领域具有广阔应用前景.
(1)Atik,M.;Delima Neto,M.J.Appl.Electrochem.1995,25,142.
(2) Deki,S.;Aoi,Y.J.Mater.Res.1998,13,883.
(3) Huang,X.Q.;Li,N.J.Alloy.Compd.2008,465(1-2),317.
(4) Shen,G.X.;Chen,Y.C.;Lin,L.;Lin,C.J.;Scantlebury,D. Electrochim.Acta 2005,50,5083.
(5) Szalkowska,E.;Gluszek,J.;Masalski,J.;Tylus,W.J.Mater. Sci.Lett.2001,20(6),495.
(6) Yun,H.;Li,J.;Chen,H.B.;Lin,C.J.Electrochim.Acta 2007, 52,6679.
(7)Yu,H.G.;Yu,J.G.;Cheng,B.;Zhou,M.H.J.Solid State Chem.2006,179,349.
(8)Kim,D.S.;Kwak,S.Y.Appl.Cata.A:Gen.2007,323,110.
(9) Dai,S.X.;Wu,Y.Q.;Sakai,T.;Du,Z.L.;Sakai,H.;Abe,M. Nanoscale Res.Lett.2010,5(11),1829.
(10) Shao,S.F.;Dimitrov,M.;Guan,N.J.;Kohn,R.Nanoscale 2010,2(10),2054.
(11)Yuan,J.J.;Li,H.D.;Gao,S.Y.;Sang,D.D.;Li,L.A.;Lu,D. Mater.Lett.2010,64(18),2012.
(12)Arita,T.;Moriya,K.;Minami,K.;Naka,T.;Adschiri,T.Chem. Lett.2010,39(9),961.
(13)Wang,X.N.;Huang,B.B.;Wang,Z.Y.;Qin,X.Y.;Zhang,X. Y.;Dai,Y.;Whangbo,M.H.Chem.Eur.J.2010,16(24),7106.
(14)Xu,Y.M.;Fang,X.M.;Xiong,J.A.;Zhang,Z.G.Mater.Res. Bull.2010,45(7),799.
(15) Li,J.;Yu,H.P.;Sun,Q.F.;Liu,Y.X.;Cui,Y.Z.;Lu,Y.Appl. Surf.Sci.2010,256(16),5046.
(16) Liu,S.J.;Gong,J.Y.;Hu,B.;Yu,S.H.Cryst.Growth Des. 2009,9(1),203.
(17)Yamamoto,K.;Tomita,K.;Fujita,K.;Kobayashi,M.;Petrykin, V.;Kakihana,M.J.Cryst.Growth 2009,311(3),619.
(18) Yasui,K.;Isobe,T.;Nakajima,A.Mater.Lett.2010,64(19), 2036.
(19)Shen,X.;Wang,Y.X.;Lu,L.Q.;Chen,Y.L.;Xia,Y.;Li,Y.H. J.Sol-Gel Sci.Technol.2010,54(3),340.
(20)Shen,L.M.;Bao,N.Z.;Zheng,Y.Q.;Gupta,A.;An,T.C.; Yanagisawa,K.J.Phys.Chem.C 2008,112(24),8809.
(21) Zhang,X.;Zhao,Y.;Zhang,C.B.;Meng,H.Acta Phys.-Chim. Sin.2007,23(6),856.[张 霞,赵 岩,张彩碚,孟 皓.物理化学学报,2007,23(6),856.]
(22)Zhao,H.J.;Shen,Y.M.;Zhang,S.Q.;Zhang,H.M.Langmuir 2009,25(18),11032.
(23)Atsunori,M.;Tatsuo,M.;Toshihiro,K.;Kiyoharu,T.;Tsutomu, M.;Masahiro,T.Chem.Mater.2005,17,749.
(24) Hosono,E.;Fujihara,S.;Kakiuchi,K.;Imai,H.J.Am.Chem. Soc.2004,126,7790.
(25) Pavasupree,S.;Jitputti,J.;Ngamsinlapasathian,S.;Yoshikawa, S.Mater.Res.Bull.2008,43(1),149.
(26) Tomita,K.;Kobayashi,M.;Petrykin,V.;Yin,S.;Sato,T.; Yoshimura,M.;Kakihana,M.J.Mater.Sci.2008,43(7),2217.
(27)Yu,J.G.;Wang,G.H.;Cheng,B.;Zhou,M.H.Appl.Catal. B-Environ.2007,69,171.
(28) Liu,Z.Y.;Sun,D.D.;Guo,P.;Leckie,J.O.Chem.Eur.J.2007, 13,1851.
(29) Hsiao,P.T.;Lu,M.D.;Tung,Y.L.;Teng,H.S.J.Phys.Chem. C 2010,114(37),15625.
(30) Jung,H.G.;Kang,Y.S.;Sun,Y.K.Electrochim.Acta 2010,55
(15),4637.
(31)An′amt,M.N.;Radiman,S.;Huang,N.M.;Yarmo,M.A.; Ariyanto,N.P.;Lim,H.N.;Muhamad,M.R.Ceram.Int.2010, 36(7),2215.
(32)Shim,H.W.;Lee,D.K.;Cho,I.S.;Hong,K.S.;Kim,D.W. Nanotechnology 2010,21(25),255706.
(33)Chiu,K.Y.;Wong,M.H.;Cheng,F.T.;Man,H.C.Appl.Surf. Sci.2007,253,6762.
(34) Zhao,X.;Liu,M.H.;Zhu,Y.F.Thin Solid Films,2007,515, 7127.
(35)Wu,Y.;Yao,W.Q.;Zhu,Y.F.Acta Phys.-Chim.Sin.2007,23
(5),625.[伍 彦,姚文清,朱永法.物理化学学报,2007,23
(5),625.]
(36)Zhu,Y.F.;Zhang,L.;Wang,L.;Fu,Y.;Cao,L.L.Acta Chim. Sin.2000,58(4),467.[朱永法,张 利,王 莉,付 艳,曹立礼.化学学报,2000,58(4),467.]
December 7,2010;Revised:February 11,2011;Published on Web:March 17,2011.
Anticorrosion Properties of Nano Anatase TiO2Films Derived from Sol-Gel and Hydrothermal Crystallization
YUN Hong1,2LIN Chang-Jian1,*DU Rong-Gui1
(1State Key Laboratory for Physical Chemistry of Solid Surfaces,Department of Chemistry,College of Chemistry and
Chemical Engineering,Xiamen University,Xiamen 361005,Fujian Province,P.R.China;2Key Laboratory of Shanghai Colleges and Universities for Electric Power Corrosion Control and Applied Electrochemistry,Department of Energy Source and Environment Engineering,Shanghai University of Electric Power,Shanghai 200090,P.R.China)
Nano TiO2films were applied to the surface of stainless steel(SS)by sol-gel and hydrothermal crystallization using Ti(O(CH2)3CH3)4as a precursor.The properties of the TiO2films were determined by X-ray diffraction(XRD),Raman spectroscopy,scanning electron microscopy(SEM),atomic force microscopy(AFM),and Auger electron spectroscopy(AES).The corrosion performance of the TiO2films was evaluated by electrochemical impedance spectroscopy(EIS)and polarization measurements.Anatase TiO2films prepared by hydrothermal crystallization at 170°C showed similar crystallization to those prepared by conventional calcination at 450°C.The TiO2prepared by the two methods were,however, obviously different from the surface structure and the material prepared by hydrothermal crystallization showed better anticorrosion performance in 3.5%(w)NaCl solution compared with the material prepared by calcination.
Hydrothermal crystallization;Anatase TiO2;Corrosion and protection
O646
∗Corresponding author.Email:cjlin@xmu.edu.cn;Tel:+86-592-2189354.
The project was supported by the National Natural Science Foundation of China(50571085,20773100,21003089)and National High Technology Research and Development Program of China(2009AA03Z327).
国家自然科学基金(50571085,20773100,21003089)和国家高技术研究发展专项(2009AA03Z327)资助项目

