微波法合成1,ω-二(2,2-二氨基-1,3,4-噻二唑-5-)烷烃类化合物*
单 栋, 寿妙萍, 赵金枝, 徐文龙, 申立全, 何冰晶
(台州学院 医药化工学院,浙江 临海 317000)
杂环化合物尤其是含氮杂环化合物在当今农药的研究与开发中占据重要地位。1,3,4-噻二唑衍生物因其具有良好的杀虫、杀菌、除草、植物生长调节、药物活性等多种功效而倍受关注[1~6];因其可作为药物中间体,在新药开发过程中具有较大的应用潜力和价值[7~9];作为一种重要的液晶材料的结构单元而成为近年来的研究热点[10,11]。
双氨基双噻二唑化合物结构中具有双噻二唑环,有望得到比单边噻二唑更高的生物活性;结构中所含的两个氨基可作为聚合反应的单体,合成高分子链上具有环结构的刚性聚合物,有望得到耐高温性能较好的聚合物;也可与一些单体合成具有适当比例的刚性段与柔性段的高分子,并控制刚性段的长径比,有望得到高分子液晶。以往文献报道多以含单噻二唑环结构的化合物为主,而双氨基双噻二唑化合物的合成却鲜有报道。
Scheme1
本文以浓硫酸为催化剂,氨基硫脲(1)与二元羧酸(2a~2d)在微波辐射下经环合反应合成了四种新型的1,ω-二(2,2-二氨基-1,3,4-噻二唑-5-)烷烃类化合物(3a~3d, Scheme 1),其结构经1H NMR和IR表征。采用单因素优选法对最佳反应条件进行了优选。
1 实验部分
1.1 仪器与试剂
WR-52型数字熔点仪;Varian Mercury-Vx 200型核磁共振仪(DMSO-d6为溶剂,TMS为内标);岛津FT-IR-8400型红外光谱仪(KBr压片)。所用试剂均为分析纯。
1.2 3的合成通法
在研钵中加入1 20 mmol, 2 10 mmol和浓硫酸2.2 mL(12 mmol),研磨使其成糊状浆体后转入烧杯中,用保鲜膜覆盖,并在保鲜膜上刺6个~8个小孔,放入微波炉中,将微波炉功率调节至中低火,反应5 min。加入蒸馏水200 mL,调至pH 1~2;抽滤,滤液用40%NaOH溶液调至pH 7~8,析出大量沉淀,抽滤,滤饼用去离子水洗涤多次后干燥得3。
3a: 浅黄色晶体,产率56.3%, m.p.295.2 ℃~297.1 ℃(溶于DMSO,微溶于DMF,不溶于水、乙醇、丙酮和乙醚);1H NMRδ: 7.0(s, 4H, NH2), 3.25(s, 2H, CH2); IRν: 3 366~3 100(NH2), 1 636, 1 611(C=N), 1 511~1 481(CH2) cm-1。
3b: 灰白色晶体,产率65.7%, m.p.302.6 ℃~304.3 ℃(溶于DMSO,微溶于DMF,不溶于水、乙醇、丙酮和乙醚);1H NMRδ: 7.0(s, 4H, NH2), 3.21(s, 4H, CH2CH2); IRν: 3 393~3 200(NH2), 1 670, 1 639(C=N), 1 524~1 606(CH2) cm-1。
3c: 土黄色粉末,产率71.54%, m.p.320.8 ℃~323.7 ℃;1H NMRδ: 1.98(s, 2H, CH2), 2.95(s, 4H, CH2), 7.00(s, 4H, NH2); IRν: 3 393~3 089(NH2), 1 670, 1 639(C=N), 1 524~1 606(CH2) cm-1。
3d: 土黄色粉末,产率70.16%, m.p.328.6 ℃~329.9 ℃;1H NMRδ: 1.64(s, 4H, CH2), 2.80(s, 4H, CH2), 7.00(s, 4H, NH2); IRν: 3 027~3 089(NH2), 1 624(C=N), 1 455~1 496(CH2) cm-1。
2 结果与讨论
以1,3-二(2,2-二氨基-1,3,4-噻二唑-5-)丙烷(3c)的合成为模板,考察诸反应条件对其产率的影响,寻找最佳反应条件。
2.1 微波炉功率对3c产率的影响
1 20 mmol,2c20 mmol,浓硫酸2.2 mL,微波辐射5 min,其余反应条件同1.2,考察微波功率对3c产率的影响,结果见表1。由表1可以看出,低火条件下,反应不够完全,产率较低;中、中高火条件下,由于微波所提供的能量过高,使部分反应分解,产率反而下降。最佳功率是中低火。

表 1 微波炉功率对3c产率的影响*
*1 20 mmol,2c20 mmol,浓硫酸2.2 mL,微波辐射5 min,其余反应条件同1.2

表 2 r对3c产率的影响*
*中低火,其余反应条件同表1;r=n(1)∶n(2)
2.2 原料配比[r=n(1)∶n(2)]对3c产率的影响
中低火,其余反应条件同2.1,考察r对3c产率的影响,结果见表2。由表2可以看出,随着r的增加,产率增加;当r=2.0∶1.8时,反应逐渐趋于完全。最佳r=2.0∶1.8。
2.3 浓硫酸用量对3c产率的影响
中低火,r=2.0∶1.8,其余反应条件同2.1,考察浓硫酸用量对3c产率的影响,结果见表3。由表3可以看出,随着浓硫酸用量的增加,产率增加;当其用量为2.6 mL时,产率稳定在77%左右。浓硫酸最佳用量为2.6 mL。

表 3 浓硫酸用量对3c产率的影响*
*中低火,r=2.0∶1.8,其余反应条件同表1
2.4 辐射时间对3c产率的影响
中低火,r=2.0∶1.8,浓硫酸2.6 mL,其余反应条件同2.1,考察辐射时间对3c产率的影响,结果见表4。由表4可见,随着时间的增加,反应趋于完全,产率增加;当辐射时间为6 min时,产率最高;时间再增加,微波的巨大能量使部分产物分解,产率反而有所下降。最佳辐射时间为6 min。
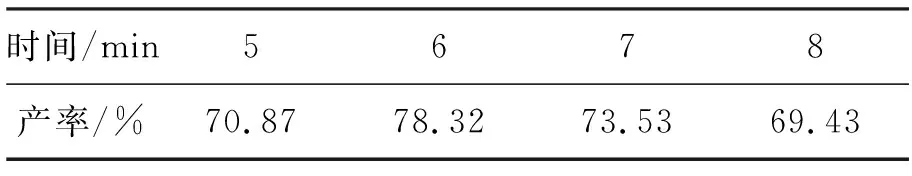
表 4 辐射时间对3c产率的影响*
*中低火,r=2.0∶1.8,浓硫酸2.6 mL,其余反应条件同表1

表 5 优化反应条件下的平行实验结果*
*1 20 mmol,n(1)∶n(2) =2.0∶1.8,中低火微波辐射6 min
综上所述,合成3c的最佳反应条件为:1 20 mmol,n(1)∶n(2)=2.0∶1.8,浓硫酸2.6 mL,中低火微波辐射6 min。在最佳反应条件下做平行实验,结果见表5。由表5可见,平均收率为77.46%,且重现性较好。
3 结论
用微波法合成了四种新型的1,ω-二(2,2-二氨基-1,3,4-噻二唑-5-)烷烃类化合物。微波合成具有反应时间短、污染小、产率高、纯度高等特点,充分体现了微波合成法绿色、高效、快捷的巨大优势。
[1] Chen L, Wang Q M, Huang R Q,etal. Synthesis and insecticidal evaluation of propesticides of benzoylphenylureas[J].J Agric Focd Chem,2005,53(1):38-41.
[2] Zou X J, Lai L H, Jin G Y,etal. Syntheses fungicidal activety and 3D-QSAR of pyridazinone-substituted 1,3,4-oxadiazoles and 1,3,4-thiadiazoles[J].J Agric Focd Chem,2002,50:3757-3760.
[3] 乐长高,饶火瑜,谢宗波. 1-(5-乙基-1,3,4-噻二唑基)-3-苯基硫脲的合成及生物活性[J].化学世界,2003,44(7):367-369.
[4] 金桂玉,侯震,赵国锋. 1-芳酰基-4-取代吡唑甲酰基氨基硫脲和环化产物的合成及生物活性[J].高等学校化学学报,1997,18(3):409-412.
[5] 谭小红,宋新建.N-(2-氯苯甲酰基)-Nc-[5-(3-吡啶基)-1,3,4-噻二唑-2-基]硫脲的相转移催化法合成[J].湖北民族学院学报(自然科学版),2005,23(3):243-245.
[6] Foroumadi A, Soltani F, Moshfi M H,etal. Syntheses and in vitro antibacterial activity of someN-(5-aryl-1,3,4-thiadiazole-2-yl)piperazinylquinolne derivatives[J].J Farmaco,2003,58(10):1023-1028.
[7] 宋新建,王子云,汪焱钢,等. 2-氨基-5-(4-吡啶基)-1,3,4-噻二唑碱的合成及其生物活性[J].应用化学,2005,22(3):334-336.
[8] 宋新建,冯桂荣,陈传兵,等.N-[5-(4-吡啶基)-1,3,4-噻二唑-2-基]-Nc-芳酰基脲的合成及其生物活性[J].有机化学,2005,25(12):1587-1590.
[9] Prasad A R, Ramalingam T, Bhaskar Pao A,etal. Syntheses and biological activity of 2-aryloxyl/aryl-5-(3,4-methylenedioxyphenyl)-triazolo[3.4-b]-1,3,4-thiadiazoles[J].Indian J Chem,1986,25B:566-568.
[10] 李茂国,商永嘉,陆婉芳,等. 新型含酰胺键的噻二唑类液晶的合成[J].高等学校化学学报,2002,23(4):576-580.
[11] 刘思印,许闽,申小清,等. 含液晶基元的1,3,4-噻二唑衍生物的合成与表征[J].东华大学学报(自然科学版),2008,34(2):137-140.

