一种新型螯合剂的合成及对钴(Ⅱ)离子螯合性能的研究
彭青林,周随安,湛雪辉,曹 芬
(长沙理工大学化学与环境工程学院,湖南 长沙 410076)
随着手机、笔记本等数码产品的增加,废旧锂离子电池的处理问题引起了全社会的关注[1].而废旧锂离子电池中的钴、镍既是匮乏的资源,又对生物系统有巨大的危害.重金属离子是生物所不能降解的,常规处理方法有化学沉降法、有机溶剂萃取、浮选[2-4]等方法.但这些方法处理成本高,繁琐,且对环境产生二次污染.
利用螯合剂回收过渡金属离子、进行水处理,因其效果显著、环保、易处理等诸多优点,引起了众多研究者的兴趣[5].螯合剂主要利用O、S、N、P原子的孤对电子与过渡金属离子形成配位键,将其从水溶液中螯合出来,达到分离、提纯的效果[6-9].目前,众多的研究者都以羟基、羧基、氨基作为螯合配体,将其应用于冶金、水处理、医药等方面,而以S元素作为配体的研究较少[10-12].本文作者根据巯基对重金属离子具有良好的配位和沉淀效果,使用混酸与对甲苯硫酚反应,合成了一种新型螯合剂,并研究了其对钴离子的螯合性能.
1 材料与方法
1.1 试剂和仪器
主要仪器为:原子吸收光谱(岛津AA-6800,日本);红外光谱仪(傅里叶红外光谱仪WQF-410,美国);对甲苯硫酚购于苏州亚科化学试剂有限公司,浓硝酸(66%),浓硫酸(98%),乙醇和二氯甲烷购于长沙化玻有限公司,均为分析纯.实验使用的水均为二次蒸馏水.
1.2 实验步骤

图1 对甲基苯硫酚硝化反应原理
1.2.1 4-甲基-2-硝基硫酚的合成 将0.62 g对甲基苯硫酚(0.005 mol)溶于15 mL二氯甲烷、10 mL乙醇混合溶剂,控制温度为15 ℃左右,在1 h内滴加浓硫酸和浓硝酸组成的混酸并保持温度为15 ℃左右,反应原理如图1所示.滴加完毕,继续反应3 h.反应完毕,将反应液倒入冰水中,分液,得到下层黄绿色溶液.除去溶剂,用乙醇与水的混合溶液重结晶2次,得到产物4-甲基-2-硝基硫酚,为黄色晶体.使用新制的亚硝酸检测滤液中的巯基[13],确认产物的纯度.
1.2.2 4-甲基-2-硝基硫酚对钴离子螯合研究 按照文献方法[14],回收废旧锂离子电池中的钴酸锂,得到黑色固体.使用3 mol/L的硫酸与2.4 mol/L的双氧水浸出黑色固体中的钴离子,过滤,稀释至100 mL,经原子吸收光谱检测钴离子浓度为1 681 mg/L,备用.
称取一定量的 4-甲基-2-硝基硫酚溶于乙醇中,然后称取一定量氢氧化钠(氢氧化钠与4-甲基-2-硝基硫酚摩尔比为3∶1)溶于乙醇,在50 ℃减压蒸馏除去乙醇,得到黄色固体.量取5 mL蒸馏水溶解黄色固体,用30%的硫酸溶液调节pH值至6,得到4-甲基-2-硝基硫酚钠溶液.
分别量取5 mL浓度为1 681 mg/L的钴离子溶液,加入到4-甲基-2-硝基硫酚钠溶液中,磁力搅拌1 h,螯合原理如图2所示.

图2 4-甲基-2-硝基硫酚螯合原理
过滤,将所得到的滤液取少部分置于西林瓶,用原子吸收光谱检测滤液中钴离子浓度.螯合率使用如下公式进行计算:
式中:A为螯合率;C1、C2为吸附前后水溶液中钴离子浓度;V1、V2为吸附前后溶液的体积.
1.2.3 4-甲基-2-硝基硫酚与钴离子的螯合物解吸附研究 将所得到的滤渣置于25 mL 8 mol/L的HCl溶液中,磁力搅拌4 h后过滤,将所得到滤液取少量于西林瓶中,供测试钴离子浓度,解吸附原理如图3所示[15].
解吸附率使用如下公式进行计算:
式中:D为解吸附率,C3为解吸附后溶液中钴离子浓度,V3为解吸附后的溶液体积.
2 结果与分析
2.1 产物的IR表征
图4为4-甲基-2-硝基硫酚的红外光谱图.从图4中可以看出,1 302 cm-1上存在的吸收峰为硝基的特征峰,表明硝化反应已成功将硝基连接在苯环上[16].
2.2 反应物比例的影响
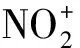

图4 4-甲基-2-硝基硫酚红外谱图

图5 硝酸用量对于产率的影响
2.3 温度的影响
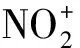
2.4 反应时间的影响
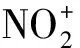

图6 温度对产率的影响

图7 反应时间对产率的影响
2.5 螯合剂用量对吸附性能的影响
选择5 mL浓度为1 681 mg/L的钴离子溶液进行螯合实验,考察不同质量的螯合剂对钴离子的螯合性能,结果如表1所示.随着螯合剂的增加,螯合率增加,因此溶液中残留的钴离子含量逐渐降低,当螯合剂质量为0.30 g时,吸附已经趋于平衡,继续增加螯合剂的质量,螯合率增加不大.由表1可知,使用25 mL 8mol/L的盐酸对沉淀进行解吸附,室温下搅拌4 h,最大解吸附率达到83.6%.由此可知,由于螯合剂与钴离子弱的键合作用,使用盐酸能够达到较好的解吸率,达到回收钴离子的最佳效果.

表1 螯合及解吸率数据
3 结论
(1)在二氯甲烷与乙醇的混合溶液中,使用混酸对对甲基苯硫酚进行硝化反应.当反应物中浓硝酸、对甲基苯硫酚的物质的量之比为4∶1,反应温度为15 ℃,反应时间为3 h时达到的最大产率为48.5%.
(2)在乙醇溶液中将4-甲基-2-硝基硫酚制成钠盐,然后进行与钴离子的螯合实验.4-甲基-2-硝基硫酚用量为0.3 g时,对5 mL钴离子浓度为1 681 mg/L溶液达到的最大螯合率为98.7%.
(3)使用8 mol/L的盐酸溶液对螯合物进行解吸附,最大解吸率达到83.6%.
参考文献:
[1] XU J Q,THOMAS H R,FRANCIS W,etal.A review of processes and technologies for the recycling of lithium-ion secondary batteries[J].J Power Sources,2008,177:512-527.
[2] PAULINO J F,BUSNARDO N G,AFONSO J C.Recovery of valuable elements from spent Li-batteries[J].J Hazard Mater,2008,150:843-849.
[3] LUO L,WEI J H,WU G Y,etal.Extraction studies of cobalt and nickel from chloride solution using PC88A[J].Trans Nonferrous Met Soc China,2006,16:687-692.
[4] 姜述芹,周保学,于秀娟,等.氢氧化镁处理含镉废水的研究[J].环境化学,2003,22(6):601-604.
[5] SAMAL S,ACHARYA S,DEY R K,etal.Synthesis and metal ion uptake studies of chelating resins derived from formaldehyde-furfuraldehyde condensed phenolic Schiff bases of 4,4′-diaminodiphenylether and o-hydroxyacetophenone[J].Talanta,2002,57:1075-1083.
[6] ALEXANDRATOS S D,SUBRAMANIAN NATESAN.Ion-selective polymer-supported reagents:the principle of bifunctionality[J].Eur Polym J,1999,35:431-436.
[7] TOKALIOGLU S,YILMAZ V,KARTAL S,etal.Synthesis of a novel chelating resin and its use of selective separation and preconcentration of some trace metals in water samples[J].J Hazard Mater,2009,169:593-598.
[8] LLOSA TANCO M A,PACHECO TANAK D A,FLORES V C,etal.Preparation of porous chelating resin containing linear polymer ligand and the adsorption characteristics for harmful metal ions[J].React Funct Polym,2002,53:91-101.
[9] ATIA A A,DONIA A M,ABOU-EL-ENEIN S A,etal.Studies on uptake behavior of copper and lead by amine chelating resins with different textural properties[J].Sep Purif Technol,2003,33:295-301.
[10] XU Y M,LI J X,DAI X H,etal.Preparation of thiol-functionalized mesoporous molecular sieve and removal of Pb2+,Hg2+and Cd2+in water[J].Chin Appl Chem,2002,19(10):941-945.
[11] 王 刚,常 青.两性高分子重金属絮凝剂PEX等电点与絮凝性能的研究[J].环境化学,2007,26(2):180-183.
[12] 李健生,苗小郁,易 睿,等.巯基功能化介孔氧化硅的合成及其对Pb(Ⅱ)的吸附[J].功能材料,2007,38(8):1386-1388.
[13] 陈耀祖.有机分析[M].北京:高等教育出版社,1983:416.
[14] 童东革,赖琼钰,吉晓洋.废旧锂离子电池正极材料钴酸锂的回收[J].化工学报,2005,56(10):1967-1970.
[15] CHEN C Y,CHIANG C L,CHEN C R.Removal of heavy metal ions by a chelating resin containing glycine as chelating groups[J].Sep Purif Technol,2007,54:396-403.
[16] ERNO P,PHILIPPE B,MARTIN B.Structure determination of organic compounds[M].Berlin:Springer,2009:295.

