Cu-OMS-2催化甲醇氧化羰基化合成碳酸二甲酯
周 烜,陈启明,杨小俊
(武汉工程大学 绿色化工过程教育部重点实验室,湖北 武汉 430073)
Cu-OMS-2催化甲醇氧化羰基化合成碳酸二甲酯
周 烜,陈启明,杨小俊
(武汉工程大学 绿色化工过程教育部重点实验室,湖北 武汉 430073)
采用固态离子交换法制备了Cu-OMS-2催化剂,并通过XRD,SEM,XPS对催化剂进行了表征,将其用于甲醇氧化羰基化合成碳酸二甲酯(DMC)反应,分析了催化剂的物相和形貌对其催化活性的影响。实验结果表明,Cu-OMS-2催化剂对合成DMC有较好的催化性能,其原因是:(1)CuCl以薄片形式均匀堆积排列分布在载体表面,有利于反应物的吸附;(2)催化剂中Cu2+和Cu+以合适的比例存在时有利于DMC的合成。采用CuCl负载量(质量分数)为25%、500℃下焙烧5 h制备的Cu-OMS-2催化剂,在优化的反应条件下,DMC的收率达84.6%。
碳酸二甲酯;甲醇;氧化羰基化;锰氧八面体分子筛;铜催化剂
碳酸二甲酯(DMC)是一种环境友好、具有多种官能团的化工中间体[1-4]。它可代替光气进行羰基化等反应生成多种重要化工产品[5];以DMC为原料可制备多种高附加值的精细专用化学品,在医药、农药等领域具有广泛应用[6-8];同时由于 DMC氧含量高、相溶性好,还广泛用于低毒溶剂和燃油添加剂[9]。因此,DMC的发展和应用将对煤化工、甲醇化工和碳一化工起到巨大的推动作用[10]。在DMC的合成方法中,甲醇氧化羰基化法因原料价廉易得、原子利用率高而被认为是最有工业应用前景的工艺路线,其核心是催化体系的选择[11-14]。在甲醇氧化羰基化合成DMC的催化体系中,铜系催化剂,尤其是以CuCl为主活性组分的催化剂具有很好的工业应用前景[15]。选择合适的载体和助剂进一步提高催化剂的活性和选择性已成为该领域重要的研究方向。
分子筛均匀分布的孔道结构对反应物分子具有高度几何选择性,经离子交换负载到分子筛上的活性金属在表面经还原后有极高的分散度,能提高活性组分的利用率并增强其抗毒性[16],因而分子筛被广泛应用于甲醇氧化羰基化合成DMC的研究。King[17]用高温固体离子交换技术,将Cu+负载在Y型分子筛上,用于甲醇氧化羰基化合成DMC,甲醇的单程转化率达11%,DMC的选择性为80%。Li等[18]合成了中孔分子筛 MCM -41,并将其与CuCl粉末高温处理制备出CuCl/MCM-41催化剂,用于甲醇氧化羰基化合成DMC,甲醇的转化率为5%~10%,DMC的选择性达100%。锰氧八面体分子筛(OMS-2)是一种类似于沸石型分子筛隧道结构的新型材料[19],具有温和的表面酸碱性、优异的离子交换性能和良好的氧化还原性[20]。OMS-2对甲醇具有较好的吸附性能,有利于反应物中甲氧基的生成[21]。通过离子交换法制备的Cu-OMS-2催化剂在异丙醇分解、有机物氧化脱氢等反应中表现出优良的催化性能。
本工作采用回流法制备了K-OMS-2载体,并采用固态离子交换法制备了Cu-OMS-2催化剂,通过对催化剂的结构表征及其催化性能的评价,为甲醇液相氧化羰基化合成DMC催化体系的研究开发奠定基础。
1 实验部分
1.1 载体及催化剂的制备
在100 mL三颈瓶中,将15 mL 1.75 mol/L的MnSO4溶液加入到50 mL 0.4 mol/L的 KMnO4溶液中,保持n(MnO4-) ∶n(Mn2+)≈0.76,在磁力搅拌下缓慢滴加6.8 mL浓硝酸至pH=2~3,100℃下回流24 h,抽滤,用去离子水洗涤至中性,120℃下干燥8 h,得到黑色的K -OMS-2载体[22]。
按一定比例称取K-OMS-2载体和CuC1,放入玛瑙碾钵中,充分研磨使两者混合均匀,置于管式炉中在N2气氛下焙烧得到负载CuC1的Cu-OMS-2催化剂。
1.2 催化剂的表征
采用日本电子公司JEOL JSM 5510LV型扫描电子显微镜观察催化剂的表面形貌。采用VG公司MULT1LAB2000型X射线光电子能谱仪对催化剂表面存在的离子价态、氧物种类型及其相对含量进行分析,光源为MgKα靶(结合能为1 253.6 eV),功率为300 W,工作条件12 kV、20 mA,分析室真空度低于0.2 μPa,以 C 1s结合能 285.0 eV 为能量校正标准。采用帕纳科公司X'Pert PRO型X射线衍射仪进行物相分析,采用CuKα靶、粉末法测定,工作条件40 mA、40 kV,范围扫描2θ=10 ~90°。
1.3 催化剂的活性评价
将50 mL甲醇和3 g催化剂加入250 mL高压反应釜中。通入 O2至0.2 MPa,然后通入 CO至4.0 MPa,在搅拌转速600 r/min下充分混合,加热至120℃反应4 h。反应完成后降温至40℃,过滤得DMC与甲醇的混合液。所得产物用岛津公司GC-2014型气相色谱仪进行分析。分析条件:柱温80℃,进样温度200℃,检测温度200℃,载气流量1.2 mL/min。由于在反应过程中O2的量不足、CO过量,因此DMC的收率以O2为基准计算。
2 结果与讨论
2.1 焙烧温度对催化剂活性的影响
制备了一系列CuCl负载量不同的Cu-OMS-2催化剂。文献报道CuCl的熔点为430℃[23],故在300~700℃内考察了催化剂的焙烧温度对甲醇氧化羰基化合成DMC反应的影响。不同焙烧温度下,CuCl负载量(质量分数)为5%和10%的催化剂上DMC的收率见图1。
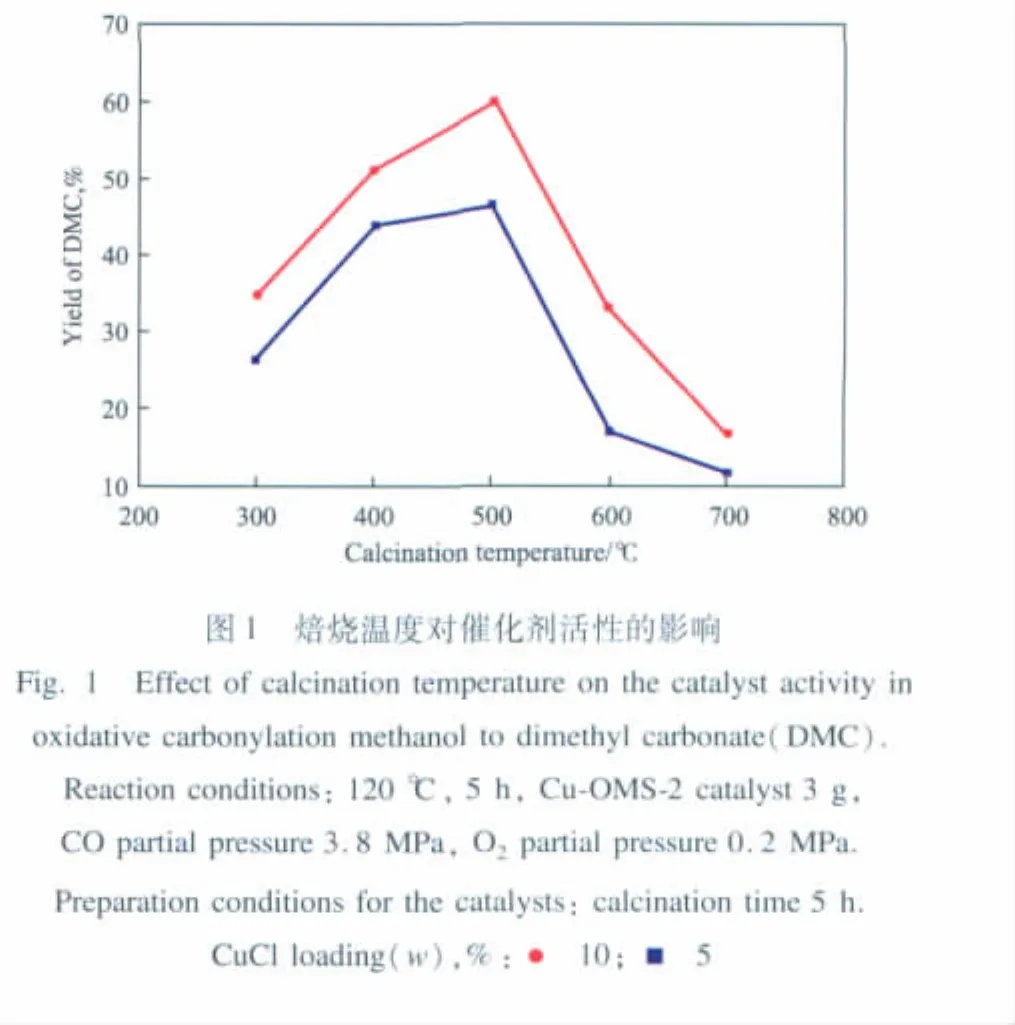
从图1可看出,CuCl负载量为5%和10%的催化剂的活性均随焙烧温度的升高先提高后下降,到500℃时催化活性最高,DMC的收率达到最大值。
不同焙烧温度下制备的Cu-OMS-2催化剂的XRD谱图见图2。由图2可看出,催化剂经400 ℃焙烧后在2θ=28.5,47.4,56.9°处出现了明显的CuC1衍射峰。当焙烧温度达到500℃时,CuC1 衍射峰强度减弱,在 2θ=28.3,41.3,58.3°处出现了KCl的衍射峰。可能是此时CuC1与载体孔道内的K+部分发生离子交换,部分Cu+以键合态的形式存在,有效增加了表面活性物种的数量,有利于提高催化剂的活性[24]。经600℃焙烧的催化剂中基本看不到CuC1的衍射峰。其原因是在较高温度下焙烧时,CuC1除了在载体表面发生自发分散及离子交换外,高温还加剧了CuC1的升华,导致CuC1从催化剂中脱除[25]。同时,当焙烧温度高于500 ℃时,在2θ=23.1,32.9,55.1°处出现了 Mn2O3的衍射主峰,并随焙烧温度的继续升高Mn2O3的衍射峰强度增强。这是由于K-OMS-2分子筛的热稳定温度为500℃,高于500℃时会生成新晶相Mn2O3。
不同焙烧温度下制备的Cu-OMS-2催化剂的SEM图像见图3。由图3可看出,当焙烧温度为400℃时,主要看到纤维状的K-OMS-2分子筛,而CuCl以颗粒状不均匀地分布在载体表面;当焙烧温度达到500℃时,颗粒状的CuCl变为片状的,并均匀堆积排列分布在载体表面;当焙烧温度达到600℃时,CuCl由片状变为块状,并在载体表面发生烧结。催化剂的表面形貌及活性金属的分布等对表面催化反应的活性具有重要的影响。一般而言,疏松多孔的表面更有利于表面反应的进行,而活性金属分布得越均匀,活性也越高。因此,500℃焙烧时得到的催化剂具有最高的催化活性。
2.2 焙烧时间对催化剂活性的影响
焙烧时间对催化剂活性的影响见图4。


图3 不同焙烧温度下制备的Cu-OMS-2催化剂的SEM图像Fig.3 SEM images of Cu - OMS -2 catalysts calcinated at different temperatures.Preparation conditions for the catalysts:CuCl loading(w)25%,calcination time 5 h.
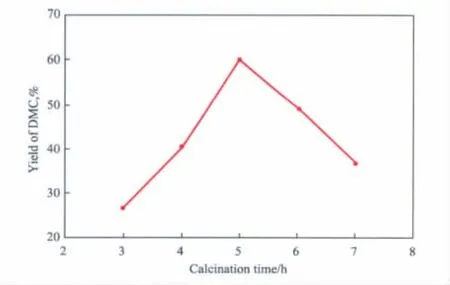
图4 焙烧时间对催化剂活性的影响Fig.4 Effect of calcination time on the catalytic activity.Reaction conditions referred to Fig.1.Preparation conditions for the catalysts:CuCl loading(w)10%,calcination temperature 500℃.
由图4可看出,DMC的收率随焙烧时间的延长先升高后降低,当焙烧时间达到5 h时,DMC收率达到最大值(59.9%)。
图5为不同焙烧时间下制备的Cu-OMS-2催化剂的XRD谱图。从图5可看出,焙烧时间为3 h和5 h时都出现了KCl的衍射峰,且随焙烧时间的延长KCl衍射峰的强度增强。这是因为焙烧时间延长,更有利于Cu+与K+发生离子交换。但当焙烧时间延长至8 h时KCl的衍射峰消失,这是因为在高温下长时间焙烧,K-OMS-2分子筛的骨架和内部孔结构完全塌陷,无法进行离子交换。另外,当焙烧时间大于5 h时,有少量的MnO2发生分解转变为Mn2O3。

不同焙烧时间下制备的Cu-OMS-2催化剂的SEM图像见图6。由图6可看出,在500℃下焙烧3 h时CuCl只有部分形成片状,而大部分还是以颗粒状存在;当焙烧时间延长至5 h时,颗粒状的CuCl全部转变成片状的,并均匀分布在载体表面,孔隙变大,有利于反应物的吸附,使催化反应易于进行;当焙烧时间延长至8 h时,催化剂部分烧结团聚,导致催化活性降低。因此,500℃下焙烧5 h的催化剂活性最好。
2.3 CuCl负载量对催化剂活性的影响
CuCl负载量对催化剂活性的影响见图7。由图7可看出,对于焙烧温度为500,600℃的催化剂,DMC的收率均随CuCl负载量的增加逐渐升高,当CuCl负载量为25%时,DMC收率达到最大值;当CuCl负载量超过25%时DMC收率随CuCl负载量的增加而降低。
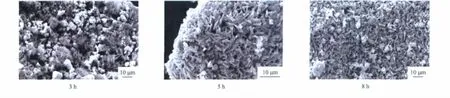
图6 不同焙烧时间下制备的Cu-OMS-2催化剂的SEM图像Fig.6 SEM images of Cu - OMS -2 catalysts prepared in different calcination times.Preparation conditions for the catalysts:CuCl loading(w)25%,calcination temperature 500℃.

图7 CuCl负载量对催化剂活性的影响Fig.7 Effect of CuCl loading on the catalytic activity.Reaction conditions referred to Fig.1.Preparation conditions for the catalysts:a 500℃,5 h; b 600℃,5 h
不同CuCl负载量的Cu-OMS-2催化剂的XRD谱图见图8。从图8a可看出,焙烧温度为300℃时,随CuCl负载量的增加,CuC1衍射峰的强度逐渐增强,且峰形更加尖锐;同时K-OMS-2分子筛的特征衍射峰(2θ=37.7°)强度随 CuCl负载量的增加而逐渐增强。从图8b可看出,焙烧温度为500℃时,随CuCl负载量的增加,CuC1衍射峰的强度逐渐减弱,而Cu4O3的衍射峰强度逐渐增强。分析认为,部分CuCl经过离子交换转变为KCl;同时,在该温度下随CuCl负载量的增加,过量的CuCl逐渐转变为Cu4O3。
不同CuCl负载量的Cu-OMS-2催化剂的SEM图像见图9。由图9可看出,随CuCl负载量的增加,片状CuCl逐渐长大、增多。当CuCl负载量为10%时,仅看到纤维状的K-OMS-2分子筛,在载体表面看不到CuCl,表明Cu+进入到分子筛孔道中,此时催化剂具有活性,DMC收率为59.9%(见图7)。这说明交换到K-OMS-2分子筛骨架中的Cu+是催化剂的活性相之一。当CuCl负载量为15%时,CuCl以较薄的片状不均匀地分布在载体表面;当CuCl负载量增加到25%时,片状的CuCl逐渐形成,孔隙变大,且均匀地分布在载体表面。CuCl负载量为15%和25%的催化剂活性提高,DMC收率分别为63.3%和84.6%(见图7)。这说明载体表面的片状CuCl也是活性相,且催化剂活性与CuCl分布的均匀程度相关。当CuCl负载量增加到30%时,CuCl由片状变为块状,且在载体表面出现了部分聚集,导致催化剂活性降低。

结合XRD和SEM分析结果认为,当CuCl负载量较小时,单位质量催化剂表面的CuCl量较少,即活性中心较少。随CuCl负载量的增加,单位质量催化剂表面的CuCl量逐渐增多,载体表面的活性吸附位被利用,因此催化剂活性提高。当CuCl负载量达到25%时,载体表面的活性吸附位被完全利用,所以此时催化剂活性最高。当CuCl负载量大于25%时,催化剂表面的CuCl呈过饱和状态,导致催化剂活性下降。因此,CuCl负载量为25%最佳。
2.4 催化剂中Cu的价态分析
在XPS表征中,Cu2+的2p3/2在结合能相距9.8 eV时有伴峰,即通常所称的斜上峰,但 Cu0和Cu+没有斜上峰。因此,是否出现斜上峰可以表征试样中是否含有 Cu2+[26]。
不同条件下制备的 Cu-OMS-2催化剂的XPS谱图见图10。由图10可看出,试样b的斜上峰出现在结合能941.6 eV处,说明在931.7 eV处应该为Cu2+;同样,试样a在结合能为940.8 eV处也出现了斜上峰,表明在930.5 eV处为Cu2+。但试样a和b的Cu2+结合能远低于Cu2+的结合能标准值(933.6 eV),反而接近于Cu+的结合能标准值(932.4 eV)。这可能是因为该催化剂中既有Cu2+又有Cu+存在的缘故。结合XRD表征(图8b)可看出,高温有利于化学位移向高位能方向移动,即试样b中Cu2+增多;低温有利于化学位移向低位能方向移动,即试样a中Cu+增多。
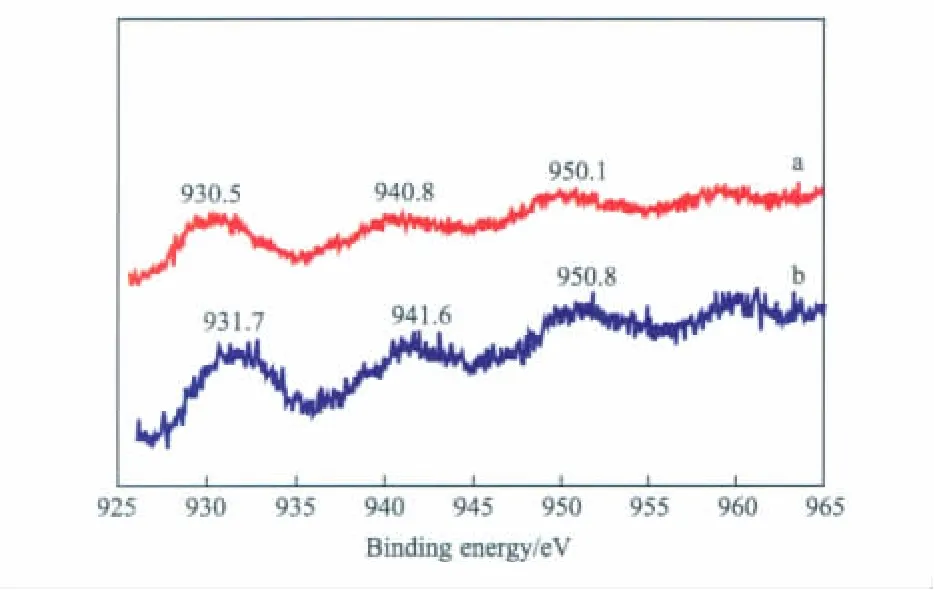
图10 Cu-OMS-2催化剂的XPS谱图Fig.10 XPS spectra of Cu - OMS -2 catalysts.Preparation conditions for the catalysts:
根据CuCl催化甲醇液相氧化羰基化合成DMC的反应机理[27]认为,Cu2+与甲醇反应生成Cu(OCH3)Cl,Cu+与 CO 反应生成 Cu(CO)Cl,然后Cu(OCH3)Cl与Cu(CO)Cl再反应生成一个混合价的中间体Cu(OCH3)Cl·Cu(CO)Cl,该中间体进一步反应生成 Cu(COOCH3)Cl,最后Cu(COOCH3)Cl与Cu(OCH3)Cl反应得到DMC。由此说明,催化剂中Cu2+和Cu+的比例合适有利于DMC的合成。这一结果与Lee等[28]在研究甲醇液相氧化羰基化合成DMC反应中,用CuCl2与NaX分子筛离子交换制备的催化剂活性组分是Cu2OCl2和CuCl相似。
3 结论
(1)Cu-OMS-2催化剂的最佳制备条件为:CuCl的负载量为25%,500℃下焙烧5 h。采用该条件下制备的催化剂,在优化的反应条件下,DMC的收率达84.6%。
(2)催化剂的表征结果显示,CuCl以薄片形式均匀排列堆积在载体表面,使催化剂疏松多孔,有利于反应物的吸附。Cu-OMS-2催化剂中Cu2+和Cu+的比例合适有利于DMC的合成。
[1]Delledonne D,Rivetti F,Romano U.Developments in the Production and Appliction of Dimethylcarbonate[J].Appl Catal,A,2001,221(1 -2):241 -251.
[2]Rivetti F.Dimethylcarbonate:An Answer to the Need for Safe Chemicals[M]//Tundo P,Anastas P,eds.Green Chemistry:Challenging Perspectives.New York:Oxford University Press,USA,2000:201-219.
[3]Ono Y.Dimethyl Carbonate for Environmentally Benign Reactions[J].Catal Today,1997,35(1 -2):15 -25.
[4]Ono Y.Dimethyl Carbonate for Environmentally Benign Reactions[J].Pure Appl Chem,1996,68(2):367 -375.
[5]Hirofumi Itoh,Yoshiyuki Watanabe,Kenji Mori.Synthesis of Dimethyl Carbonate by Vapor Phase Oxidative Carbonylation of Methanol[J].Green Chem,2003,5(5):558 -562.
[6]王登峰,张学兰,高阳艳,等.离子液体催化氨基甲酸甲酯和甲醇合成碳酸二甲酯[J].石油化工,2010,39(4):387-390.
[7]Tundo P,Selva M.The Chemistry of Dimethyl Carbonate[J].Acc Chem Res,2002,35(9):706 -716.
[8]Ono Y.Catalysis in the Production and Reactions of Dimethyl Carbonate,an Environmentally Benign Building Block[J].Appl Catal,A,1997,155(2):133-166.
[9]Pacheco M A,Marshall C L.Review of Dimethyl Carbonate(DMC)Manufacture and Its Characteristics as a Fuel Additive[J].Energy Fuels,1997,11(1):2 -29.
[10]刘永新,田庆来.碳酸二甲酯的市场需求和生产技术进展[J].精细石油化工,2002,24(4):41-45.
[11]马新宾,黄守莹,王胜平,等.氧化羰基化法合成有机碳酸酯的研究进展[J].石油化工,2010,39(7):697-705.
[12]Mo Wanling,Xiong Hui,Li Tao,et al.Catalytic Performance and Corrosion Inhibition of CuCl/Schiff Base System in Homogeneous Oxidative Carbonylation of Methanol[J].J Mol Catal A,2006,247(1-2):227-232.
[13]Sato Y,Kagotani M,Souma Y.A New Type of Support‘Bipyridine Containing Aromatic Polyamide’to CuCl2for Synthesis of Dimethyl Carbonate(DMC)by Oxidative Carbonylation of Methanol[J].J Mol Catal A,2000,151(1 -2):79 -85.
[14]Sato Y,Kagotani M,Yamamoto T,et al.Novel Effective Poly(2,2'-Bipyridine-5,5'- Diyl) - CuCl2Catalyst for Synthese of Dimethyl Carbonate(DMC)by Oxidative Carbonylation of Methanol[J].Appl Catal,A,1999,185(2):219 -226.
[15]杨洋,刘晓勤,刘定华,等.羰基化合成碳酸二甲酯用铜系催化剂的研究[J].精细石油化工进展,2006,7(5):21-25.
[16]赵骧编.催化剂[M].北京:中国物资出版社,2001:633-640.
[17]King S T.Reaction Mechanism of Oxidative Carbonylation of Methanol to Dimethyl Carbonate in Cu - Y Zeolite[J].JCatal,1996,161(2):530 -538.
[18]Li Zhong,Xie Kechang,Slade R C T.High Selective Catalyst CuCl/MCM-41 for Oxidative Carbonylation of Dimethyl Carbonate[J].Appl Catal,A,2001,205(1 -2):85 -92.
[19]Shen Yanfei,Zerger R P,De Guzman R N,et a1.Manganese Oxide Octahedral Molecular Sieves:Preparation,Characterization and Application[J].Science,1993,260(4):511 -515.
[20]Peluso M A,Gambaro L A,Pronsato E,et a1.Synthesis and Catalytic Activity of Manganese Dioxide(Type OMS-2)for the Abatement of Oxygenated VOCs[J].Catal Today,2008,133-135:487-492.
[21]马新宾,李振花,王保伟,等.甲醇氧化羰基化合成碳酸二甲酯原位红外研究[J].天津大学学报,2002,35(4):460-462.
[22]Abecassis-Wolfovich M,Jothiramalingam R,Landau M V,et al.Cerium Incorporated Ordered Manganese Oxide OMS -2 Materials:Improved Catalysts for Wet Oxidation of Phenol Compounds[J].Appl Catal,B,2005,59(1):91 -98.
[23]李飞阔.负载CuCl催化剂催化甲醇液相氧化羰基化合成碳酸二甲酯的研究[D].武汉:武汉工程大学化工与制药学院,2009.
[24]李忠,孟凡会,任军,等.CuCl/SiO2-Al2O3催化剂的表面结构及甲醇氧化羰基化催化性能[J].催化学报,2008,29(7):646-647.
[25]Xie Y C,Tang Y Q.Advances in the Studies of Spontaneous Monolayer Dispersion of Oxides and Salts on Supports[J].Adv Catal,1990,37(12):1 -13.
[26]陈兴权,薛冰,赵春香,等.甲醇气相氧化羰基化合成碳酸二甲酯[J].石油化工,2005,34(11):1041-1045.
[27]殷元骐主编.羰基合成化学[M].北京:化学工业出版社,1996:238 -260.
[28]Lee M Y,Park D C.Alkyl Carbonate Synthesis by New Catalytic System[J].Stud Surf Sci Catal,1991,66(2):631 -640.
Oxidative Carbonylation of Methanol to Dimethyl Carbonate over Cu-OMS-2 Catalyst
Zhou Xuan,Chen Qiming,Yang Xiaojun
(Key Laboratory for Green Chemical Process of Ministry of Education,Wuhan Institute of Technology,Wuhan Hubei 430073,China)
Cu-OMS-2 catalysts were prepared by solid-state ion-exchange method and used in oxidative carbonylation of methanol to dimethyl carbonate.The catalysts were characterized by means of XRD,SEM and XPS.The effects of the crystalline phase and structure on the catalyst activity in the oxidative carbonylation were investigated.The results showed that the good catalytic performance of Cu-OMS-2 catalyst could be attributed to the appropriate proportion between Cu2+and Cu+in the catalyst.CuCl existed in thin slice form and dispersed well on the catalyst surface,which was beneficial to adsorption of the reactants.Among the used catalysts,the Cu-OMS-2 catalyst with 25%(w)CuCl loading and calcinated at 500℃ for 5 h showed the highest catalytic activity.The yield of dimethylcarbonate could reach 84.6%at the optimal reaction conditions.
dimethyl carbonate;methanol;oxidative carbonylation;manganese-oxygen octahedral molecular sieve;copper catalyst
1000-8144(2011)04-0369-07
TQ 225.52
A
2010-10-12;[修改稿日期]2011-01-17。
周烜(1985—),女,湖北省武汉市人,硕士生,电邮406268599@qq.com。联系人:陈启明,电话 13476830452,电邮qiming_yuanxin@hotmail.com。
国家自然科学基金重点项目(20936003);湖北省自然科学基金项目(2008CDA009)。
(编辑 安 静)

