pH对氟罗沙星与BSA之间结合常数的影响
徐艳霞,夏小环,刘世旺
(黄冈师范学院化学与生命科学学院,湖北黄州438000)
pH对氟罗沙星与BSA之间结合常数的影响
徐艳霞,夏小环,刘世旺
(黄冈师范学院化学与生命科学学院,湖北黄州438000)
采用毛细管区带电泳法,通过测定在不同pH值、不同牛血清白蛋白浓度的缓冲溶液条件下药物迁移时间的变化,计算出了pH分别为6.8、7.4和8.0时氟罗沙星与牛血清白蛋白相互作用的结合常数,其值分别为11.807 ×104、5.682 ×104、7.472 ×104mol/L。结果显示:当 pH=6.8 时结合常数值最大,当 pH 增大为7.4时,结合常数值显著下降。探讨pH对结合常数的影响规律,对于进一步阐明药物作用机理具有较强的理论意义。
氟罗沙星;牛血清白蛋白;毛细管区带电泳;结合常数;pH
氟罗沙星(fleroxacin,FLRX)是1987年人工合成的第3代氟喹诺酮类抗菌素。由于其副作用小、口服吸收迅速完全、体内分布范围广、药物持续时间长、血药浓度高、对大多数需氧G-杆菌、葡萄球菌以及衣原体、支原体等均具有良好的抗菌活性,故其在临床上使用广泛,是一种常见的人兽共用抗炎药[1-3]。血清白蛋白是血浆中含量最丰富的载体蛋白,它能与许多内源及外源性化合物结合,起到存储与转运的作用。研究氟罗沙星与血清白蛋白之间的作用,有助于了解药物分子在体内的运输和分布情况,对于阐明氟喹诺酮类药物的作用机理、药代动力学等都有非常重要的意义[4-6]。
结合常数(Kb)是研究分子之间非共价相互作用的最重要参数之一,在生物化学及药物学研究中,测定相关物质之间的Kb、研究各种环境因素等对Kb的影响是一项很重要的工作。毛细管电泳(CE)是上世纪八十年代初发展起来的一种新型分离技术,广泛应用于包括蛋白质-蛋白质、蛋白质-核酸、蛋白质-药物、酶-底物、抗原-抗体等各种亲和体系的分离和分析[7]。与传统方法相比,CE法用于分子间相互作用的研究具有分析速度快,分离效率高,样品用量少(nmol级),对受体的纯度要求不高,在溶液中进行,可以保持生物分子相互作用所需要的生理条件等优点[8]。本文首次采用毛细管区带电泳法,通过测定在不同pH值、不同牛血清白蛋白(BSA)浓度的缓冲溶液条件下药物迁移时间的变化,计算出了不同pH值条件下氟罗沙星与BSA相互作用的结合常数,同时通过比较分析,探讨了pH值影响结合常数的规律和内在机理,这些对于进一步阐明氟喹诺酮类药物的作用机理并迅速开发出更高效的人兽两用广谱抗菌药物具有较强的理论和现实意义。
1 实验部分
1.1 试剂与仪器
氟罗沙星样品购自中国药品生物制品检定所,BSA(MW=66000) 购自 Sigma(St.Louis,MO,USA),磷酸氢钠、磷酸二氢钠、氢氧化钠、盐酸、丙酮等均为市售分析纯试剂,水为二次去离子水。P/ACE 5000毛细管电泳仪(Beckman,USA),紫外检测器;未涂渍石英毛细管 50 μm i.d.×57 cm(有效长度50 cm,河北永年光纤厂)。Varian CARY 1E紫外-可见光分光光度计(Australia)。
1.2 实验条件及操作步骤
电泳条件:温度为20.0℃,冷冻液控温;操作电压为18 kV;检测波长为280 nm;压力进样,进样时间为10 s;两次测定之间,将毛细管先用0.2 mol/L NaOH溶液冲洗6 min,再用去离子水冲洗2 min,随后用运行缓冲溶液冲洗3 min,然后进样。每份样品均平行测定三次。
以不同pH值、50 mmol/L磷酸盐缓冲溶液为运行缓冲溶液,使用前经0.22 μm微孔滤膜过滤。氟罗沙星样品先用浓盐酸溶解,再加等体积pH=7.4的中性磷酸盐缓冲溶液(PBS,100 mmol/L)稀释,作为储备液4℃冰箱冷藏备用。实验前用运行缓冲溶液稀释储备液,使得氟罗沙星的浓度约为0.50 mmol/L;采用丙酮作为中性标记物,样品中丙酮的浓度约为0.2%(v/v);将BSA溶于运行缓冲溶液中,分别配制成0.003、0.006、0.009、0.012、0.015、0.018 mmol/L 等系列浓度。
2 结果与讨论
2.1 电泳条件的优化
为研究氟罗沙星在生理条件下(pH 6.0~8.0)与BSA的相互作用,同时综合考虑到电渗流、电荷和离子强度等因素的影响,实验选择了浓度为 50 mmol/L、pH 值分别为 6.8、7.4、8.0 的磷酸盐缓冲体系。通过考察不同电压下氟罗沙星电泳分离情况,并综合考虑迁移时间和热效应等因素的影响后,我们选择操作电压为18 kV。将氟罗沙星稀释至0.020 mmol/L左右后,在紫外-可见光分光光度计上扫描得到氟罗沙星的紫外吸收光谱(见图1)。根据紫外吸收光谱和毛细管电泳仪性能指标要求,我们选择电泳检测波长为280 nm。
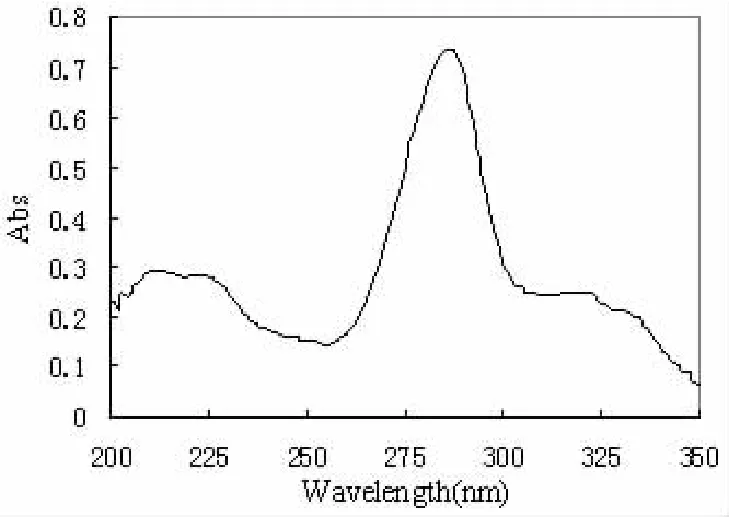
图1 氟罗沙星紫外吸收光谱Fig.1 UV -Vis spectra of Fleroxacin
2.2 氟罗沙星与BSA间Kb测定
2.2.1 测定模型 为了简化计算,我们建立了一种简单模型,并假设药物分子与蛋白质的结合比为1∶1。将蛋白质加入缓冲溶液中,药物样品进样后在毛细管区带中与蛋白质发生相互作用,快速达到如下平衡:
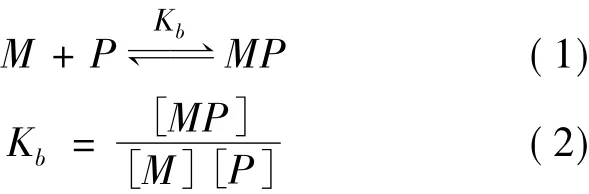
其中Kb为药物分子与蛋白质之间的结合常数,[M]和[P]分别为平衡体系中游离药物和游离蛋白质的浓度,[MP]为药物与蛋白质结合而成的复合物的浓度。
Yang等[9]依据色谱原理,推导出以下线性方程:

其中k'为容量因子,Φ为相比(Vs/Vm),s和m分别代表固相和液相。
k'可以根据方程(4)通过实验数据计算得到:

其中t为药物的保留时间,t0为中性标记物的保留时间。根据方程(3)作k'~[P]图,直线的斜率为a,截距为b,结合常数Kb可通过方程(5)计算得到:

2.2.2 测定结果 本实验以丙酮为中性标记物,测定了在不同pH值、不同BSA浓度缓冲溶液条件下氟罗沙星的迁移时间,相对标准偏差(RSD)在0.02% ~1.1%之间,重现性很好,说明该方法准确、可靠。根据模型中的方程(3)和(4)进行数据处理,作k'~[BSA]图,分别得到不同pH值条件下氟罗沙星与BSA相互作用的线性关系(见图2)。应用模型中的方程(5)计算出相应的结合常数如表1。
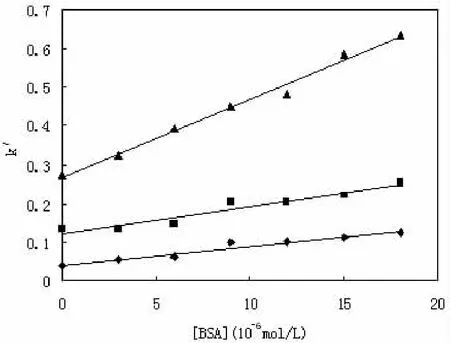
图2 不同pH条件下,k`和BSA浓度之间的线性关系图Fig.2 The Linear relationship of k'and the concentration of BSA

表1 不同pH条件下,氟罗沙星与BSA相互作用的结合常数Table 1 The binding constants of the interactions between Fleroxacin and BSA
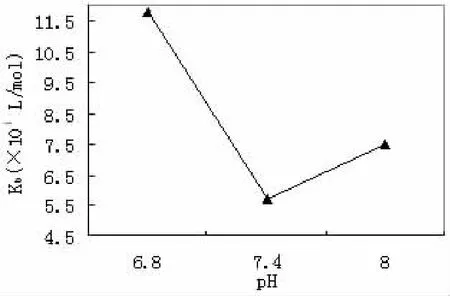
图3 氟罗沙星与BSA相互作用的Kb和pH之间的关系图Fig.3 Relationship between the binding constants and pH
氟罗沙星与BSA之间的结合常数随pH值变化的趋势情况如图3。由图3可见,在所研究的pH值范围内,氟罗沙星Kb的最大值出现在pH值为6.8时,当pH值增大为7.4时,Kb值显著下降,降幅超过50%,当pH值再增大至8.0时,Kb值则略有增加,变化曲线整体上呈U形。2.2.3 讨论 实验结果表明,氟罗沙星分子在不同pH条件下均能与BSA发生较强烈的相互作用,药物与BSA之间的Kb均在104-105L/mol数量级。不同pH条件下氟罗沙星与BSA相互作用的线性相关系数r>0.96,说明氟罗沙星分子与BSA之间结合比为1∶1以及药物分子的保留行为与色谱过程中相似的假设是合理的,即氟罗沙星分子以1∶1的比例与BSA相互作用,分子结构上存在单一确定的中心作用位点。
本小组对培氟沙星、左氧氟沙星、氧氟沙星、环丙沙星等做过类似研究[10]。根据Kb值随pH变化的情况推测,这四种药物分子与BSA之间的结合力,在中性或偏碱性(pH7.4~8.4)时以范德华力为主,在微偏酸(pH=6.8)时以电荷作用力为主。本实验结果显示,氟罗沙星与BSA之间的Kb值随pH变化的规律与上述四种药物分子非常相似,即pH=6.8时 Kb值最大,pH 增至7.4时Kb值显著减小。由此推测,在不同pH时氟罗沙星和BSA之间相互作用力的类型与上述四种分子相同,即在微偏酸时以电荷作用力为主,在中性或偏碱性时以范德华力为主。
氟罗沙星与培氟沙星等同属氟喹诺酮类分子。在不同pH条件下,氟罗沙星和BSA之间相互作用的特点与其它四种药物相似,这是它们分子骨架相同的结果(如图4)。在一定pH条件下,氟罗沙星、培氟沙星等分子结构中可能成为带电荷的基团主要有:羧基、酮基、氟原子及哌嗪基中的亚氨基。其中羧基和酮基在中性和偏酸性条件下易形成氢键,氢键的形成会使羧基和酮基的电荷量大大减少,基团作用力也会相应减弱,但实际测知氟罗沙星等的Kb值在微偏酸(pH=6.8)时均最大,由此可以推测,在中性和微偏酸环境中氟罗沙星与BSA作用的主要基团不是羧基和酮基,而哌嗪基中的亚氨基则很可能处在作用位点的中心位置上。氟罗沙星与培氟沙星在分子结构上的差异主要表现在氟原子个数上,而两者Kb随pH发生相似变化的规律表明:在药物与BSA相互作用时,氟原子可能不在作用位点的中心。
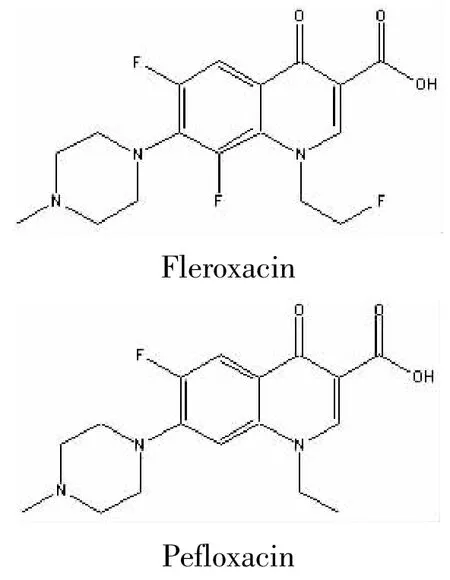
图4 氟罗沙星与培氟沙星的分子结构Fig.4 Structure of Fleroxacin and Pefloxacin
3 结论
本文利用毛细管区带电泳,通过测定氟罗沙星的迁移时间,计算得到了pH分别为6.8,7.4和8.0时氟罗沙星与BSA之间的结合常数,其值分别为11.807 ×104、5.682 ×104、7.472 ×104L/mol。环境pH对氟罗沙星与BSA之间的相互作用有强烈影响,当 pH处在6.8-7.4之间时,结合常数对pH尤为敏感。同时,根据实验结果分析推测:氟罗沙星分子是以1∶1的比例与BSA相互作用的,分子结构上存在单一确定的中心作用位点;在pH6.8-7.4范围内,氟罗沙星与BSA之间的相互作用以电荷作用力为主,而在pH 7.4~8.0范围内,氟罗沙星与BSA之间的相互作用以范德华力为主。在药物与BSA相互作用时,氟原子可能不在作用位点的中心。
[1]聂丽华,赵慧春,王学斌,等.荧光法研究氟罗沙星与牛血清白蛋白的相互作用[J].北京师范大学学报(自然科学版),2001,37(1):87 -91.
[2]何建鹏,李日生,刘厚凡,等.喹诺酮类药物的发展概况[J].江西化工,2007,(3):17-18.
[3]陈超森,曾卓,熊淑群.喹诺酮类药物的研究进展[J].精细化工中间体,2005,35(5):1 -5.
[4]谭非,张胜建.氟罗沙星与人血清白蛋白相互作用研究[J].化学研究与应用,2009,21(2):184-188.
[5]刘炜,毕和平,张连华,等.洛美沙星与 DNA相互作用的光谱研究[J].海南师范大学学报(自然科学版),2008,21(3):282 -286.
[6]易平贵,俞庆森,商志才,等.氧氟沙星与牛血清白蛋白相互作用机制[J].药学学报,2000,35(10):774-777.
[7]Tanaka Y,Terabe S.,Estimation of binding constants by capillary electrophoresis[J].J Chromatogr B,2002,768:81-92.
[8]J.Otergaard,C.Schou,C.Larsen,N.H.H.Heegaard,Effect of Dextran as a Run Buffer Additive in Drug-Protein Binding Studies Using Capillary Electrophoresis Frontal Analysis[J]. Anal. Chem.,2003,75:207-214.
[9]Yang Y,Liu XX,Zhang X X,Korenaga T.Study on the Dynamic Complexation Between Protein and PAHs by Capillary Electrophoresis[J].Anal Sci,2001,17:i1345-i1348.
[10]刘世旺,徐艳霞,夏小环.pH对氟喹诺酮药物与BSA之间相互作用影响的研究[J].分析科学学报,2009,25(5):542 -546.
Influence of pH value on the interactions between fleroxacin and bovine serum albumin
XU Yan-xia,XIA Xiao-huan,LIU Shi-wang
(Chemistry and Life Science College,Huanggang Normal University,Huangzhou 438000,Hubei,China)
The interactions between fleroxacin(FLRX)and bovine serum albumin(BSA)were studied with capillary zone electrophoresis.The migration behaviors of FLRX were investigated in a series of running buffers containing different concentrations of BSA.The binding constants(Kb)of FLRX and BSA were calculated.As pH values of the running buffer were 6.8,7.4 and 8.0 respectively,Kbwas 11.807 ×104,5.682 ×104,and 7.472 ×104L/mol correspondingly.The results shows that pH value had a great influence upon the interactions between FLRX and BSA,and when pH value was equal to 6.8,Kbof FLRX and BSA had its maximum.Kbdecreased gradually when the pH value was 7.4.The binding type and site between FLRX and BSA were investigated in detail.Studying on the influence of pH value on the binding constants would be very helpful to explore the pharmacokinetic mechanism of the drug and develop its new derivatives.
fleroxacin;bovine serum albumin;capillary zone electrophoresis;binding constants;pH value
O657.8
A
1003-8078(2011)06-0061-04
2011-09-14 doi10.3969/j.issn.1003 -8078.2011.06.17
徐艳霞,女,湖北武汉人,高级实验师,主要从事生理学的教学和科研工作。
刘世旺,男,湖北武汉人,教授,主要从事生物化学的教学科研工作。E-mail:swlsw@hgnu.edu.cn
湖北省自然科学基金项目(2008CDZ040);湖北省教育厅科学研究重点项目(D20092706);湖北省产学研结合重点项目(C2010061)。
(李鑫)

