依帕司他联合甲钴胺治疗糖尿病周围神经病变的临床观察
李新慧
新疆维吾尔自治区克拉玛依市克拉玛依区银河卫生服务中心,新疆克拉玛依 834000
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)是糖尿病在神经系统发生的多种病变的总称,是糖尿病三大并发症之一,比糖尿病视网膜病变、糖尿病肾病发病率高,症状出现早。研究证实约半数以上的糖尿病患者都伴发不同程度的周围神经病变,临床症状主要表现为对称性疼痛及感觉异常,下肢症状较上肢多见,感觉异常包括麻木、蚁走、虫爬、触电样感觉等,严重者可表现出现感觉减退甚至消失[1]。糖尿病神经病变晚期可出现肢体坏疽,被人称为不死的癌症,足见其对患者健康的危害。糖尿病神经病变的原因复杂,发病机制尚未完全阐明,因此,该病还未有根本的治疗方法。本临床实验研究发现,应用依帕司他联合甲钴胺治疗DPN取得了良好疗效,现报道如下:
1 资料与方法
1.1 一般资料
选择2009年5月1日~2010年5月8日我院就诊的2型糖尿病合并DPN患者80例,随机分为治疗组和对照组,每组各40例。其中,对照组,男20例,女20例;平均年龄为(50.23±4.68)岁;糖尿病病程为(9.23±3.12)年,DPN 病程为(3.54±1.35)年;空腹血糖值为(11.45±3.56)mmol/L,糖化血红蛋白(HbA1c)水平为(9.34±2.9)%;采用肌内注射维生素 B1和维生素B12治疗。治疗组男22例,女18例;平均年龄为(52.02±5.68)岁;糖尿病病程为(9.75±3.25)年,DPN 病程为(3.68±1.56)年;空腹血糖值为(11.98±4.21)mmol/L,HbA1c水平为(9.87±3.3)% ;采用依帕司他与甲钴胺联合治疗。两组患者在年龄、性别、基本病情等方面差异均无统计学意义(P>0.05),具有可比性。
1.2 入选标准
入选患者需满足以下条件:①符合1999年WHO糖尿病的诊断标准[2]。②身体有感觉异常或者运动神经受累的临床表现,如蚁走、虫爬、发热、触电样感觉,刺痛、灼痛、钻凿痛、肢体麻木;跟腱反射、膝腱反射减弱或消失;震动觉减弱或消失;位置觉减弱或消失,尤以深感觉减退为明显。③应用肌电图进行检测神经传导具有明显下降。④除外其他疾病可引发的神经病变。
1.3 方法
治疗组应用甲钴胺片联合依帕司他片治疗,剂量分别为500 mg和50 mg,口服,3次/d;对照组肌内注射维生素B1和维生素 B12,剂量分别为 100 mg 和 500 μg,1 次/d;两组治疗疗程均为2周。
1.4 疗效评价
根据《疾病临床诊断和疗效标准》,对疗效进行分级[3-4],显效:临床上症状显著好转或者症状者完全消失,感觉异常、跟腱反射、膝腱反射等方面显著好转或恢复正常且神经传导速度(NCV)增加量>5 m/s或恢复正常;有效:临床症状有所好转,感觉异常、跟腱反射、膝腱反射有所改善,NCV增加<5 m/s;无效:临床上症状无好转,跟腱反射、膝腱反射、感觉异常较前无变化,NCV无改变。
1.5 统计学方法
应用SPSS 13.0统计学软件进行数据分析,计量资料数据用均数±标准差(±s)表示,多组数据间的比较采用单因素方差分析,分析前进行方差齐性检验,若总体方差齐,采用SNK法进行两两比较;若总体方差不齐,则采用秩和检验;计数资料用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗效果比较
治疗组有效率高于对照组,差异有统计学意义(P<0.05)。见表1。

表1 两组治疗效果比较(例)
2.2 两组治疗前后神经传导速度变化
对照组治疗前后各项神经传导速度均无明显改变,差异无统计学意义(P>0.05);治疗组治疗前后正中神经与腓总神经的运动神经传导速度(MCV)和感觉神经传导速度(SCV)比较,差异均有统计学意义 (均P<0.05)。见表2。
表2 两组治疗前后神经传导速度变化(±s,m/s)
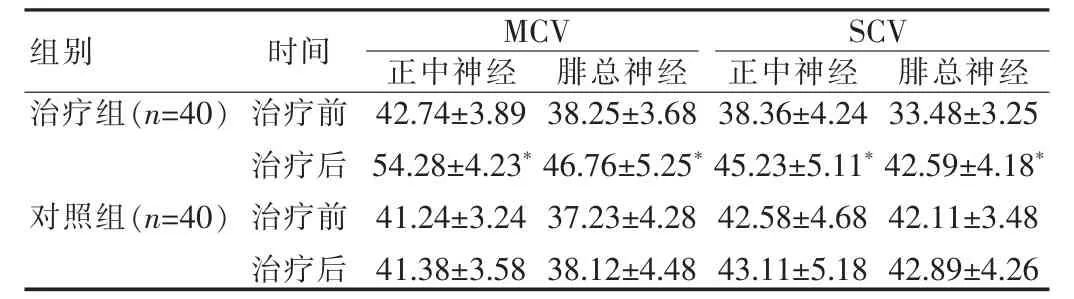
表2 两组治疗前后神经传导速度变化(±s,m/s)
注:与同组治疗前比较,*P<0.05
组别 时间治疗前治疗后治疗前治疗后MCV正中神经 腓总神经SCV正中神经 腓总神经治疗组(n=40)对照组(n=40)42.74±3.8954.28±4.23*41.24±3.2441.38±3.5838.25±3.6846.76±5.25*37.23±4.2838.12±4.4838.36±4.2445.23±5.11*42.58±4.6843.11±5.1833.48±3.2542.59±4.18*42.11±3.4842.89±4.26
3 讨论
糖尿病患者的治疗方法主要是控制血糖,但能否有效预防并发症的发生也是决定糖尿病患者预后的关键。DPN是糖尿病最常见的并发症,其发病与患者血糖高低和糖尿病病程长短有关,患者的血糖越高、病程越长,其DPN的发生几率也越高。因此,能否有效治疗DPN是糖尿病患者将来是否有高质量生活的关键因素[5]。
DPN的发病原因复杂,发病机制尚未完全明晰。纵观国内外相关研究,人们普遍将糖代谢紊乱基础上的多因素作用作为其发病的主要机制,而其中包括的亚因子也较为复杂,主要有多元醇旁路的激活、局部血流微循环障碍、非酶促糖基化产物的积聚、脂代谢紊乱及神经营养等因子的缺乏[6]。相关的临床实验亦证实,多种不同作用机制的药物联合治疗对于DPN的治疗能够起到很好的疗效[7]。 DPN的主要病理变化是神经轴突萎缩变性甚至消失,髓鞘节段性或弥散性皱缩或脱髓鞘,导致神经细胞的结构和功能发生障碍。目前,我国对该病的治疗多以甲钴铵为主,甲钴铵的分子结构与维生素B12相似,中央钴分子上结合了1个甲基基团,使其更易进入神经细胞内。甲钴胺的作用机制主要是参与体内甲基的转移及核酸、卵磷脂、蛋白质的合成,进而促进髓鞘合成与轴突再生,修复损伤的神经,可以有效改善DPN的临床症状,并加快神经的传导速度[8]。过多的葡萄糖被醛糖还原酶催化产生山梨醇是发生糖尿病神经病变的重要原因,山梨醇在山梨醇脱氢酶作用下生成果糖,然而由于神经组织中缺乏果糖激酶,无法代谢果糖,故山梨醇和果糖大量沉积于周围神经,导致周围神经发生水肿、脱髓鞘和坏死等后果[9]。依帕司他作为一种醛糖还原酶非竞争性抑制剂,能够选择性抑制醛糖还原酶的活性,防止山梨醇在神经组织蓄积,进而改善运动神经的传导速度[10]。
综上所述,本研究采用甲钴胺联合依帕司他治疗糖尿病神经病变临床效果显著,可以明显改善患者的临床症状,加快神经传导的恢复,且患者的耐受性好,值得临床推广使用。
[1]李雪霞,李平,雷龙涛.2型糖尿病周围神经病变的危险因素探讨[J].中国医学创新,2011,8(14):192-194.
[2]叶任高,陆再英.内科学[M].6版.北京:人民卫生出版社,2004:797.
[3]李剑波,陈家伟.糖尿病外周神经病变的发病机理研究进展[J].国外医学:内分泌学分册,2004,3(2):82-83.
[4]李家邦,陈泽奇,张翔,等.清肝利湿汤治疗肝湿热证的临床研究[J].湖南中医学院学报,1996,16(2):27-28.
[5]胡绍文,郭瑞林,童光焕.实用糖尿病学[M].2版.北京:人民军医出版社,2003:389.
[6]蔡洁,董继宏,汪昕.糖尿病周围神经病变发病机制的研究进展[J].中国临床医学,2007,14(3):302-305.
[7]Simmons Z,Feldman EL.Update on diabetic neuropat hy[J].Curr Opin Neurol,2002,15(5):595-603.
[8]常乐军.灯盏细辛联合用钴胺治疗糖尿病周围神经病变[J].中国实用神经疾病杂志,2007,10(9):120-122.
[9]E KE,Ruiz F,Darmanin C,et al.Aldose reductasest ructures:implications for mechanism and inhibition[J].Cell Mol Life Sci,2004,61(7/8):750-762.
[10]Ikeda T,Iwata K,Tanaka Y.Long term effect of epalrestat on cardiac autonomic neuropathy in subjects with noninsulin dependent diabetes mellitus[J].Diabetes Res Clin Pract,1999,43(3):193-198.

