氢溴酸高乌甲素分散片的溶出度考察
胡雪莲,余涛,邢茂,雷健,陈琳,张恩娟
(第三军医大学新桥医院药剂科,重庆 400037)
氢溴酸高乌甲素是从高乌头中提取总碱,经化学分离获得的二萜类单体—刺乌头碱的氢溴酸盐[1],为国内首创的非依赖性镇痛药,是卫生部《癌症患者三阶梯镇痛疗法指导原则》中规定的中度镇痛药。临床广泛用于癌症镇痛、术后镇痛等[2-8]。目前已批准使用的剂型仅有注射剂、片剂和贴片,注射剂起效快,但携带及使用不方便,普通片剂和贴片起效慢,不能达到迅速镇痛的要求。因此,笔者研制携带、使用方便,又能迅速起效的氢溴酸高乌甲素分散片,采用高效液相色谱(HPLC)法对其溶出行为进行研究。因本品规格较小(5 mg),故采用小杯法进行研究。
1 仪器与试药
Waters 600高效液相色谱仪(美国Waters公司)、Waters 2487紫外检测器;ZRS-8智能药物溶出仪(天津大学无线电厂制造);氢溴酸高乌甲素对照品(中国药品生物制品检定所,批号:100289-200902),氢溴酸高乌甲素分散片(自制,规格:每片 5 mg,批号:090601,090602,090603),氢溴酸高乌甲素片(福州海王福药制药有限公司,规格:每片 5 mg,批号:0812280),甲醇(色谱纯,Scharlau Chemie S.A.),水为纯化水,其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:Diamonsil C18柱(250mm×4.6mm,5 μm);流动相:0.05 mol·L-1磷酸二氢钠-甲醇(28∶72);柱温:25℃;检测波长:252 nm;流速:1.0mL·min-1;进样体积:20 μL。
2.2 检测波长的选择 精密称取氢溴酸高乌甲素对照品适量,用流动相制成每毫升约含20 μg的溶液,以流动相为空白于200~400 nm波长扫描。结果对照品在221,252,309 nm处有吸收峰。考虑到221 nm靠近末端吸收,309 nm波长处峰值较低,因此选择波长252 nm为检测波长。
2.3 色谱条件的选择及系统适用性 参考氢溴酸高乌甲素含量和有关物质研究[9-10]的色谱条件进行实验,选 用18柱 (250mm ×4.6mm,5 μm),以0.05 mol·L-1磷酸二氢钠溶液-甲醇(28∶72)为流动相,结果主峰峰形对称,理论板数>1 500,主峰与邻近峰的分离度>1.5。故选择此色谱条件。
2.4 溶出转速的选择 采用小杯法,以100mL水为溶剂,考察转速分别为100,50 r·min-1时的溶出情况,结果50 r·min-1,10 min时溶出即>80%,说明氢溴酸高乌甲素分散片溶出较快,故选择50 r·min-1较合适。
2.5 溶出介质的选择 照溶出度测定法(《中华人民共和国药典》2010年版二部附录X C第三法),转速为50 r·min-1,分别选择水、0.1 mol·L-1盐酸、磷酸盐缓冲液(pH6.8)3种溶出介质进行考察,结果在3种溶出介质中的溶出行为相似,无明显差别。因此选择水为氢溴酸高乌甲素分散片的溶出介质。
2.6 滤膜吸附的考察 分别采用滤膜(孔径0.45 μm)过滤和离心(3 000 r·min-1)两种方式处理溶出液,结果两种方式处理的峰面积十分相近,说明采用滤膜(孔径0.45 μm)过滤不会对主药产生吸附,而滤膜过滤较离心法简单易行,因此采用滤膜过滤法处理样品。
2.7 溶出度方法验证
2.7.1 系统适用性考察 称取氢溴酸高乌甲素分散片细粉适量,用水配制成每毫升约含氢溴酸高乌甲素50 μg的溶液,取 20 μL注入液相色谱仪,记录色谱图。结果主峰峰形对称,理论板数>1 500;与邻近峰分离度>1.5,已完全分离。
另取氢溴酸高乌甲素对照品溶液,连续进样5次,每次20 μL,记录色谱图,计算各峰面积的RSD,考察本色谱系统的重复性。结果连续进样5次的峰面积RSD 为0.65%(<1.0%),说明本色谱系统重复性很好。
2.7.2 专属性考察 分别称取氢溴酸高乌甲素对照品、氢溴酸高乌甲素分散片细粉、空白辅料适量,用水配制成每毫升约含氢溴酸高乌甲素50 μg的溶液,取20 μL注入液相色谱仪,记录色谱图(图1)。结果空白辅料约在3.1 min出现较小的辅料峰,但与主峰相距甚远,对溶出度测定无干扰。说明所选择的溶出度测定方法专属性较好。
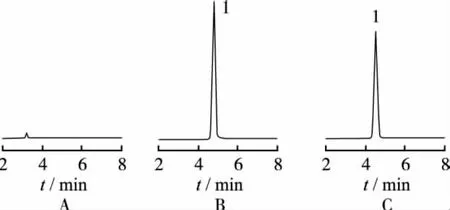
图1 氢溴酸高乌甲素HPLC图A.空白对照;B.氢溴酸高乌甲素对照品;C.氢溴酸高乌甲素分散片;1.氢溴酸高乌甲素Fig.1 HPLC chromatogram of lappaconitine hydrobromideA.blank control;B.the reference of lappaconitine hydrobromide;C.lappaconitine hydrobromide dispersible tablets;1.lappaconitine hydrobromide
2.7.3 溶出液稳定性考察 取专属性项下的样品溶液,分别于室温下放置 0,2,4,6,12,24 h 后,取 20 μL注入液相色谱仪,记录色谱图,结果各时间点的峰面积RSD 为1.35%(<2.0%),说明本品溶出液的稳定性较好,至少在24 h内稳定。
2.7.4 线性关系考察 精密称取氢溴酸高乌甲素对照品12.2 mg,置25mL量瓶中,加水溶解并稀释至刻度,摇匀,作为贮备溶液。分别精密量取贮备溶液0.2,0.5,0.8,1.0,1.2,1.5mL 置 10mL 量瓶中,用水稀释至刻度,配制成浓度分别为9.76,24.40,39.04,48.80,58.56,73.20 μg·mL-1的溶液。分别取上述溶液20 μL,注入液相色谱仪,记录色谱图。以浓度为横坐标,主峰面积为纵坐标进行线性回归,得回归方程为Y=19 583X-14 259(r=0.999 7)。氢溴酸高乌甲素在9.76 ~73.20 μg·mL-1浓度范围内峰面积与浓度呈良好的线性关系。
2.7.5 溶出度回收实验 按氢溴酸高乌甲素分散片溶出度测定浓度的50%,80%,100%进行回收实验。分别精密称取氢溴酸高乌甲素对照品约6.25,10.00,12.50 mg各3份,置250mL量瓶中,再分别加入空白辅料约0.14 g,加水溶解并稀释至刻度,滤过,取续滤液作为供试品溶液。另精密称取氢溴酸高乌甲素对照品约10 mg,置25mL量瓶中,加流动相溶解并稀释至刻度,摇匀。再精密量取该溶液1mL,置10mL量瓶中,用水稀释至刻度,作为对照品溶液。按“2.3”项下的色谱条件,分别取供试品溶液及对照品溶液20 μL,注入液相色谱仪,记录色谱图,按外标法计算回收率。结果3个浓度的回收率均在97% ~103%之间(表1),平均回收率为100.30%,RSD为1.34%,说明该方法的准确度较高。
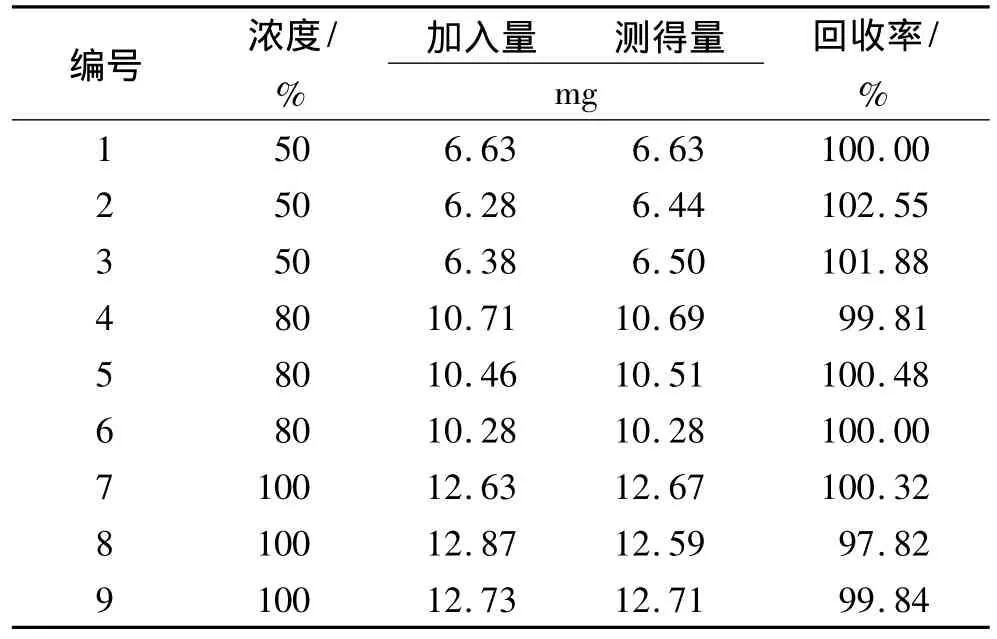
表1 氢溴酸高乌甲素溶出度回收实验结果Tab.1 Recovery of the dissolution of lappaconitine hydrobromide n=9
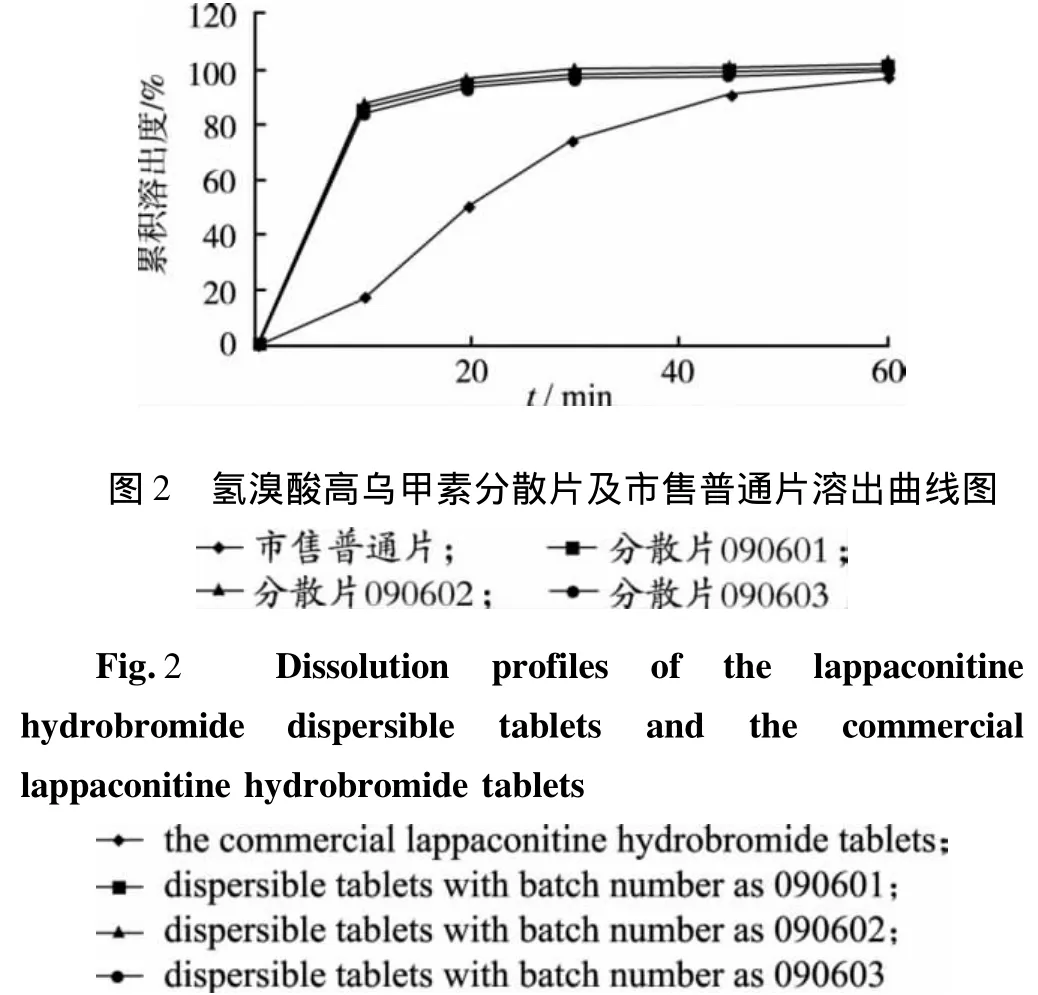
2.8 溶出均一性考察及与市售片比较 测定3批氢溴酸高乌甲素分散片中试样品溶出曲线,考察溶出均一性。采用小杯法,以 100mL水为溶剂,转速50 r·min-1。取样时间点设为10,20,30,45,60 min,分别计算累积溶出度。同法测定市售氢溴酸高乌甲素普通片的溶出曲线,与分散片进行比较。累积溶出曲线见图2。
3 讨论
氢溴酸高乌甲素片剂因规格较小(5 mg),质量标准[11](卫生部标准二部第5册)采用的溶出度测定方法为:“取本品数片(相当于氢溴酸高乌甲素50 mg),照溶出度测定法(《中华人民共和国药典》1995年版二部附录ⅩC第2法),加水800mL为溶剂,转速为100 r·min-1,经 45 min 时,吸取溶液 20mL,滤过,精密量取滤液10mL置于25mL量瓶中,照含量测定项下自……测定每片的溶出量。限度为标示量的80%”。按照此方法,一个溶出杯要放10片样品,实际上测得的是10片样品的平均值,不能真实反映出每片的溶出情况。分析原因,可能因为此标准制订较早,当时尚未普遍使用小杯法,故对规格较小的氢溴酸高乌甲素片剂采取了以上方法。
因此,采用小杯法进行氢溴酸高乌甲素分散片溶出方法研究,结果3批氢溴酸高乌甲素分散片溶出度均一性好,10 min内累积溶出度>80%,而普通片40 min时溶出度才达到80%,说明分散片的释药速度较普通片快,提示氢溴酸高乌甲素分散片的吸收可能比普通片快,因此有望达到迅速镇痛的目的。
[1]唐希灿,朱梅英,冯洁,等.刺乌头碱氢溴酸盐的药理作用研究[J].药学学报,1983,18(8):579-584.
[2]安一明,戴建平,陈力,等.高乌甲素贴片治疗癌症疼痛的临床研究[J].中国肿瘤临床与康复,1997,4(2):86-87.
[3]阙铁生,钟进才,周晓敏.高乌甲素透皮贴剂治疗中重度癌痛[J].中国临床康复,2005,9(2):211.
[4]杨涛,王利利,王均炉.氯诺昔康和高乌甲素用于老年人中上腹部手术后自控镇痛的效果比较[J].医药导报,2005,24(9):782-783.
[5]孙烁.高乌甲素复合舒芬太尼用于术后镇痛的临床观察[J].现代中西医结合杂志,2010,19(32):4185-4186.
[6]胡兆春,叶香芳.高乌甲素伍用吗啡用于硬膜外持续镇痛的临床观察[J].海峡药学,2010,22(6):195-196.
[7]王井泉.高乌甲素治疗56例胆道术后患者疼痛的临床疗效分析[J].中国临床药理学与治疗学,2010,15(5):551-554.
[8]戴秀琴,方韬.高乌甲素合用芬太尼在术后静脉镇痛中的应用[J].中国医院药学杂志,2009,29(5):402-404.
[9]胡雪莲,余涛,邢茂,等.HPLC法测定氢溴酸高乌甲素的含量和有关物质[J].医药导报,2011,30(2):249-251.
[10]王鸿,高建青,李新平.超声波对氢溴酸高乌甲素透皮吸收的影响[J].医药导报,2009,28(3):295-296.
[11]中华人民共和国卫生部药品标准(二部)第5册[S].1996:53.

