糖化血红蛋白水平与终末期肾病风险
瑟沃诺 等
引言
糖尿病是终末期肾病(ESRD)的首要原因。糖尿病护理的主要目的是通过对高血糖的管理来预防大血管和微血管并发症。据以前的研究报告,强化血糖控制可降低1型和2型糖尿病患者的微血管病变风险。虽然对大血管并发症的影响仍不明朗,但是一致认为,强化血糖控制和微血管并发症(尤其是肾病)之间存在相关性。
然而,就血糖控制在降低糖尿病患者的肾小球滤过率(GFR)或终末期肾病发病率的有效性问题,以往的试验结果相互矛盾。在UKPDS(英国前瞻性糖尿病研究)试验,强化控制组的2型糖尿病患者在9年时间内的血清肌酐增倍风险减少67%。一项试验(Epidemiology of Diabetes Interventions and Complications/Diabetes Control and Complications Trial)结果显示,强化治疗组患者的血清肌酐水平显著降低(P=0.004)。与此相反,VADT(Veterans Affairs Diabetes Trial)试验结果显示,平均随访5.6年后,无论蛋白尿进展情况,强化血糖控制组患者的血清肌酐增倍风险并没有显著降低(P=0.99)。ACCORD(Action to Control Cardiovascular Risk in Diabetes Study Group)试验也有类似的结果,该试验显示,ESRD结局在强化治疗组和常规治疗组之间没有显著差异性(P = 0.7126)。
因此,防止糖尿病患者ESRD进展的最佳糖化血红蛋白水平阈值,仍不清楚。此外,很少有试验把“血糖控制对ESRD进展的效果”作为研究的主要终点进行评估。此外,强化血糖控制对终末期CKD(慢性肾病)效果的数据也很少。KDOQI(Kidney Disease Outcomes Quality Initiative)指南建议糖化血红蛋白(HbA1c)降低至7.0%以下,可能有利于延缓肾功能减退;然而,证据水平不强。因此,本研究旨在评估糖尿病患者在怎样的糖化血红蛋白水平,可最大限度减少ESRD和全因死亡率。对于终末期CKD的糖尿病患者,我们还分析了严格血糖控制和ESRD发病率之间的相关性。
材料和方法
患者
从韩国首尔国立大学盆唐医院肾内科的2004年数据库检索出符合条件的糖尿病患者,年龄25岁或以上,已开始使用药物(包括口服降糖药和胰岛素)治疗。
统计学分析
我们比较了组间参数的差异。所有分析均采用SPSS(15.0版,SPSS,IL,USA)。连续变量或分类变量频率的数据采用平均值±标准偏差表示,连续变量的差异性采用双尾成对T检验或单向方差分析,分类变量的差异性采用卡方检验。我们比较了组间ESRD和全因死亡累积的发生率。为了确定基线糖化血红蛋白水平是否和我们指定的事件发生率独立相关,我们采用了Cox 比例风险模型进行对年龄、性别和其他风险因素的调整。双边检验的P值<0.05具有统计学意义。
结果
患者特征
共纳入4,474名患者,平均年龄66.21±11.60岁,其中52.5%为男性,糖尿病病程平均为8.56年,其中1,751名(39.1%)患者有高血压,1,605名(35.9%)患者有心血管疾病既往史(见表1)。
根据基线糖化血红蛋白(HbA1c)水平,我们把患者分为3组。①HbA1c<6.50%为第1组,平均HbA1c值为5.90%;②HbA1c 6.50%~7.49%为第2组,平均HbA1c值为6.92%;③HbA1c≥7.50%为第3组,平均HbA1c值为8.91%。第3组患者最年轻。第1组患者的糖尿病病程最短。血清总胆固醇和空腹血糖水平,3组组间有显著性差异。第1组患者的血清胆固醇水平最低。
在药物使用情况方面,第3组患者使用ACEI或ARB、OHA和胰岛素的频率最高;第1组患者的高血压和CVA事件最频繁。然而,各组间在CAD、CVD和癌症没有显著差异性(见表1)。
HbA1c数据分析
在研究随访期间,Post-index HbA1c值下降至7.27%±1.15%。各组的Post-index HbA1c值在组间显示存在显著性差异:第1组为6.32%,第2组为7.05%,第3组为8.10%。根据Post-index HbA1c值重新对患者进行分组发现,大多数患者仍然被分到以前的组别(见表2)。
结果分析
我们观察了5.29±1.22年后ESRD事件发生率,还观察了4.42±0.92年后的死亡率。结果发现,有90名(2.0%)患者进展为ESRD。ESRD患者占组内的比例,第1组为1.3%,第2组为1.8%,第3组为2.7%(P=0.017)。组间的全因死亡率没有显著差异性,整体有439名(9.8%)患者死亡:第1组为9.4%,第2组为9.0%,第3组为10.8%(P=0.199)。根据Kaplan - Meier生存曲线,在随访期间,第1组的ESRD事件发生率最低(log-rank检验,P=0.003)(图1A)。3组组间的全因死亡率没有显著差异性(log - rank检验,P=0.199)(图1B)。
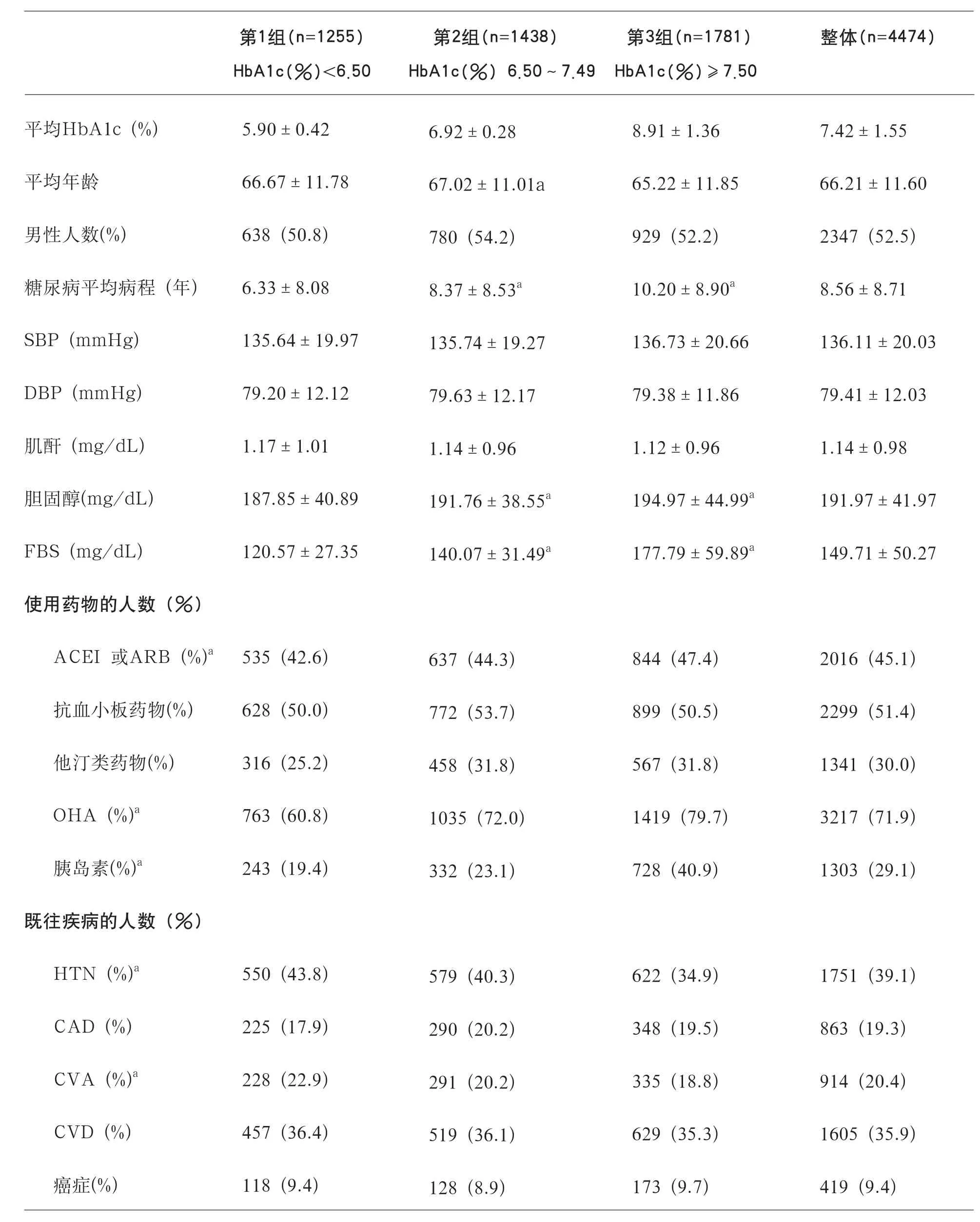
表1 各组患者的基线特征

表2 Post-index HbA1c数据分析
采用Cox 比例风险模型分析ESRD显示,经调整年龄、糖尿病病程和单因素危险因素后,和第1组相比,第2组的ESRD风险增加2.915倍(95%CI 1.172~7.252,P=0.021),第3组的ESRD风险增加4.219倍(95%CI 1.745~10.201,P=0.001)。和女性相比,男性的预后较差(HR,1.868;95%CI 1.112~3.139,P=0.018)。和GFR>60mL/min/1.73m2的患者相比,GFR<60 mL/min/1.73m2的患者的ESRD风险增加1.978倍(95%CI 1.080~3.623,P=0.027)(见表3)。
终末期CKD和HbA1c的关系
GFR<60mL/min/1.73m2的患者有799人。平均年龄为77.12±9.75岁,其中45.4%为男性,糖尿病平均病程为12.87年。在随访期间,有22名(2.8%)患者进展为ESRD。ESRD事件发生率,在基线HbA1c <6.50%组为1.3%,在基线HbA1c在6.50%~6.99%组为1.7%,在基线HbA1c在7.00%~7.99%组为2.3%,在基线HbA1c≥8.00%组为5.4%(P=0.043)。
根据GFR和基线HbA1c水平,我们把患者分为四组。①组A(HbA1c<6.50%+GFR≥60 mL/min/1.73 m2)的基线平均HbA1c水平为5.89%,②组B(HbA1c <6.50%+GFR<60 mL/min/1.73m2)的基线平均HbA1c水平为5.91%,③组C(HbA1c≥6.50%+GFR≥60 mL/min/1.73 m2)的基线平均HbA1c水平为8.03%,④组D(HbA1c≥6.50%+GFR<60 mL/min/1.73 m2)的基线平均HbA1c水平为7.99%。就ESRD事件的发生率而言,组A为1.1%,组B为1.3%,组C为2.9%,组D为3.4%(P=0.019)(图2)。经调整年龄、性别、糖尿病病程和单因素危险因素后,和组A相比,组C的ESRD风险增加3.692倍(95%CI 1.309~10.409,P=0.014),组D的ESRD风险增加7.428倍(95%CI 2.369~23.290,P=0.001)。然而,组B和组A之间并没有显示出类似的显著相关性(P=0.368)。
年龄、糖尿病病程、心血管危险因素和HbA1c的关系
年龄在80岁以上亚组(N=489)人群中,就各组进展为ESRD的比例而言,第1组为3.8%,第2组为0.7%,第3组为0.5%(P=0.034)。全因死亡在3组组间没有显著差异性(P=0.822 )。
糖尿病病程超过10年亚组(N=1346)人群中,共有24人(1.8%)进展为ESRD,就各组而言,第1组为1.2%,第2组为0.7%,第3组为2.6%。第2组的ESRD发病率较低(P=0.047)。3组组间的全因死亡率没有显著差异性(P=0.929 )。
共有1,592名患者有CVD既往史。在这一亚组人群中,整体的ESRD发病率为1.8%:第1组为1.1%,第2组为1.2%,第3组为2.7%(P=0.063)。3组组间的全因死亡率没有显著差异性(P=0.587)。

图1 ESRD发病率和全因死亡率
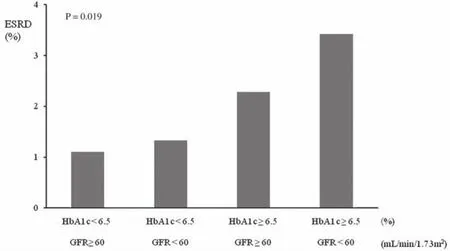
图2 各组ESRD的发病率
讨论
我们已经表明,HbA1c水平低于6.50%和ESRD事件发生率的降低有关,在HbA1c≥6.50%的条件下,不良事件风险随着HbA1c值的增加而增加。
就强化血糖控制对微量白蛋白尿的治疗效果而言,和以前的研究结果一致,但是就强化血糖控制和ESRD发病率之间的关系而言,研究结果却相互矛盾。此外,最近有研究结果显示,强化血糖控制组出现的风险超过了已获得的益处。ACCORD随机试验纳入的受试者特征包括:①CVD(35%)既往史或显著CVD风险,②年老(平均年龄62岁),③相对较长的糖尿病病程(平均糖尿病病程,10年)。该试验在随访3.5年后,因强化血糖控制组死亡率增加而被迫终止。最近发表的一项回顾性队列研究结果显示,偏低和偏高的HbA1c均值,都和全因死亡以及心脏原因死亡增加相关。
相比之下,强化血糖控制,可延缓1型糖尿病年轻患者的微血管并发症的发生发展。同样,强化血糖控制,可降低新诊2型糖尿病患者(平均年龄54岁)的微血管并发症风险。UKPDS的10年后续随访结果发现,强化血糖控制,可降低突发心肌梗死和全因死亡风险,还有降低微血管并发症风险。根据这些研究结果,ADA(美国糖尿病协会)指南建议,HbA1c的目标值应≤7.0%,以预防微血管和大血管并发症,强化血糖控制可使一部分患者(糖尿病病程短的或没有显性CVD的患者)的预期寿命得到延长。
然而,在ADVANCE试验,受试者的特征尽管包括年老(平均年龄为66岁)和伴有CVD高风险因素,结果显示,强化血糖控制组使大血管和微血管事件的复合终点发生率降低了10%。根据ADA指南,这些结果被归因于较短的糖尿病病程(平均8年)和较低的基线HbA1c水平(平均7.48%)。此外,ACCORD试验亚组分析结果表明,基线HbA1c<8%且没有CVD既往史的患者的主要CVD事件发生率偏低。VADT试验亚组分析结果显示,强化血糖控制使糖尿病病程<12年的患者在CVD方面获益。
我们的研究结果支持ADVANCE试验结果。我们研究的患者也有类似ADVANCE试验的基线特征,包括年龄、CVD风险和糖尿病病程。虽然ADVANCE试验没有显示强化血糖控制对肌酐倍增的治疗效果,但是可能有利于降低肾病原因死亡或肾病替代治疗的需求;我们的研究结果表明,第1组的ESRD发病率显著降低。就基线血清肌酐水平而言,我们的研究(100±86μmol/L)比ADVANCE试验(86±24μmol/L)要高,这也许可以用来解释,为什么我们的研究在随访5.29年后ESRD的发病率会增加。我们的研究结果显示,全因死亡率在3组组间之间没有显著差异性。这一结果和ADVANCE试验结果一致。
然而,对年龄在80岁或以上的亚组进行分析表明,ESRD发病率在第1组最高。此外,对糖尿病病程超过10年的亚组进行分析表明,ESRD发病率在第2组最低。在第1组,年龄较大或糖尿病病程较长的患者在ESRD进展方面没有显示获益。对于存在CVD既往史和CVD风险因素的患者,ESRD发病率显著降低(P=0.036)。以上这些结果表明,强化治疗的重点应放在年龄和糖尿病病程上,而不是CVD风险因素上。到目前为止,合并CKD的糖尿病患者应保持的HbA1c水平,仍不清楚。我们的研究结果表明,HbA1c目标值<6.5%,对于GFR<60 mL/min/1.73 m2的糖尿病患者,可降低ESRD的进展,而且全因死亡率没有增加倾向。即使在合并终末期CKD的糖尿病患者,强化血糖控制在延缓ESRD的进展方面也有显著影响。
最近,国际专家小组认为,在西方国家,HbA1c值在6.5%,在确定糖尿病患者有肾病进展风险方面表现灵敏。相反,在亚洲,日本的研究结果认为HbA1c阈值为6.1%,中国的研究结果认为HbA1c阈值为6.3%。在我们的研究,基线HbA1c水平比其他研究结果都低,而且认为强化血糖控制对于降低ESRD发病率是合适的;族裔的差异性可能会影响到研究的结果。
总之,我们的研究结果显示,在糖尿病患者,HbA1c值<6.50%可降低ESRD风险,同时不增加全因死亡率;对于年龄≥80岁、糖尿病病程超过10年的患者,临床HbA1c目标值建议可是适当放宽。另外,HbA1c值<6.50%还可以使合并终末期CKD的糖尿病患者在ESRD进展方面获益。

