美洛西林与四种常用输液的配伍稳定性考察
臧治满,李晨晨,谭爱萍*
美洛西林钠是临床上常用的一种半合成青霉素类抗生素,常用于革兰阴性菌中敏感菌属所致的感染[1]。该药说明书中未说明是否能与0.9%氯化钠注射液配伍使用,仅说明与5%葡萄糖氯化钠注射液或5%、10%葡萄糖注射液配伍使用。但在临床上,糖尿病患者因病情需要,不能使用葡萄糖注射液。而且临床曾发生过几例美洛西林钠与氯化钠注射液配伍后出现沉淀的案例。因此,本文模仿临床用药条件,考察美洛西林钠与4种常用输液的配伍稳定性,为临床用药提供参考。
1 材料与方法
1.1 材料
1.1.1 仪器 Lc-2010C HT高效液相色谱仪:日本岛津公司制造;HYPERSIL BDS-C18色谱柱(250mm ×4.6mm,5μm):大连依利特有限公司制造;万分之一分析天平:中德合资SARTORIOUS公司生产;DelTA320PH计:梅特勒-托利上海有限公司。
1.1.2 试药 注射用美洛西林钠,1 g/瓶,瑞阳制药有限公司生产,批号:10073001;0.9%氯化钠注射液,250mL/瓶,大连泰华药业有限公司生产,批号:810081821;5%葡萄糖注射液,250mL/瓶,大连泰华药业有限公司生产,批号:810060512;10%葡萄糖注射液,250mL/瓶,大连泰华药业有限公司生产,批号:809091212;5%葡萄糖+0.9%氯化钠注射液,250mL/瓶,大连泰华药业有限公司生产,批号:8090992711;蒸馏水:自制(经0.22μm微孔滤膜滤过);磷酸二氢钾(分析纯),沈阳市新西试剂厂生产,批号:2007年05月20日;磷酸氢二钾(分析纯),天津市博迪化工有限公司生产,批号:2007年6月7日;甲醇(色谱纯),天津科密欧化学试剂有限公司生产,批号:20090210。
1.2 方法
1.2.1 色谱条件 色谱柱:BDS-C18(250mm×4.6mm,5μm);流动相:磷酸盐缓冲溶液(pH 值为5.8)∶甲醇 =60∶40;检测波长:210 nm;流速:
1.2 mL/min;进样量:1μL;柱温为30℃。
1.2.2 溶液的配置 流动相的配制:精密称取磷酸二氢钾8.3409 g与磷酸氢二钾0.8700 g,加水溶解定容至1000mL,超声振荡10min,用孔径为0.22μm的微孔滤膜过滤。
对照品溶液的配制:取1 g注射用美洛西林钠,将其溶于10mL注射用水中,摇匀,使其充分溶解。
样品溶液的配制:按临床常用剂量,分别将2 g注射用美洛西林钠加入到0.9%氯化钠注射液、5%葡萄糖注射液、10%葡萄糖注射液、5%葡萄糖+0.9%氯化钠注射液中,制成样品溶液。
1.3 方法学考察
1.3.1 专属性考察 取对照品溶液1mL,将其稀释至 8 mg/mL,取 1μL 进样,再分别取 1μL 0.9%氯化钠注射液、1μL 5%葡萄糖注射液、1μL 10%葡萄糖注射液、1μL 5%葡萄糖+0.9%氯化钠注射液进样,比较所得色谱图。
1.3.2 标准曲线的绘制 取对照品溶液1mL,用流动相稀释至 1、2、4、8、12 mg/mL,在上述色谱条件下进行测定,记录峰面积,以色谱峰面积(Y)对美洛西林钠浓度(C)进行线性回归。
1.3.3 精密度考察 取对照品溶液1mL,将其稀释至8 mg/mL,连续进样5次,进样量1μL,记录峰面积,计算变异系数。
1.4 配伍稳定性考察 首先,测定5%葡萄糖注射液、10%葡萄糖注射液、0.9%氯化钠注射液、5%葡萄糖氯化钠注射液的pH值,将2 g美洛西林钠溶于上述4种输液中,再分别测定4种溶液的pH 值,作为 0 h 的 pH 值,然后于 0、0.5、1、2、3、4、5、6 h分别测定pH值及含量,同时记录配伍液外观变化。
2 结果
2.1 专属性考察结果 见图1~图5。可见4种输液对美洛西林钠的测定无影响,表明所建立的分析方法的专属性好。

图1 美洛西林钠色谱图

图2 5%葡萄糖注射液色谱图

图3 10%葡萄糖注射液色谱图

图4 0.9%氯化钠注射液色谱图

图5 5%葡萄糖+0.9%氯化钠注射液
2.2 标准曲线 美洛西林钠的线性回归方程:Y=2694317.7361 C+173722.5053,r=0.9999,结果表明,美洛西林钠在1~12 mg/mL范围内,浓度与面积呈良好的线性关系。见图6。
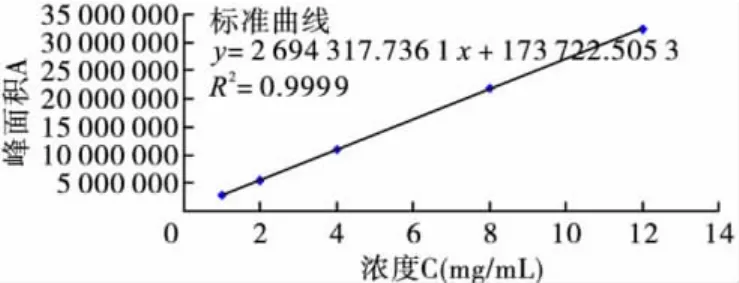
图6 标准曲线
2.3 精密度考察结果 见表1。

表1 美洛西林钠日内精密度考察结果
2.4 样品配伍后稳定性考察 见表2~表5。结果表明,美洛西林钠与4种输液配伍后,样品峰面积变化小于2%,表明配伍溶液在6 h内稳定。

表2 美洛西林钠与5%葡萄糖注射液配伍的稳定性考察

表3 美洛西林钠与10%葡萄糖注射液配伍的稳定性考察

表4 美洛西林钠与5%葡萄糖+0.9%氯化钠注射液配伍的稳定性考察

表5 美洛西林钠与0.9%氯化钠注射液配伍的稳定性考察
3 讨论
3.1 流动相的选择 由于美洛西林钠偏碱性,且当pH值为5.5~7.5时较稳定,因此,本文选择了磷酸盐缓冲液(pH 5.8)∶甲醇为流动相。有报道对美洛西林钠的测定采用磷酸盐缓冲液-乙腈(80∶20)为流动相[2]。由于甲醇和乙腈极性相似,且价格便宜,所以,在本研究中,将乙腈换为甲醇。在预实验过程中,笔者发现,当磷酸盐缓冲液∶甲醇为80∶20,保留时间过长,因此,调整了磷酸盐缓冲液与甲醇的比例。经过反复优化,最终确定以磷酸盐缓冲液∶甲醇(60∶40)为流动相,实现了主峰与杂质的良好分离,且保留时间短,缩短了实验时间。
3.2 测定波长的选择 于200~400 nm处对美洛西林钠样品溶液进行扫描,发现美洛西林钠的吸收峰在210 nm处[3],且在预实验中发现,氯化钠溶液、葡萄糖溶液、葡萄糖氯化钠溶液在210 nm处无吸收峰,对美洛西林钠的测定无影响,因此,选择210 nm作为美洛西林钠的检测波长。
3.3 在绘制标准曲线的过程中发现,载样量过大时,美洛西林钠峰形不呈正态分布,因此,若采用本实验所建立的色谱条件对美洛西林钠进行分析测定,样品溶液的适用浓度范围应在1~12 mg/mL。
3.4 本研究表明,美洛西林钠与氯化钠溶液配伍前后pH值无明显变化,而与葡萄糖溶液、葡萄糖氯化钠溶液配伍后,溶液的pH值变化较大,这可能是因为美洛西林钠偏碱性,实验中测得的氯化钠溶液pH值约为5.36,配伍后美洛西林钠对氯化钠的pH值影响不大。实验中测得5%葡萄糖溶液的pH值为4.32,10%葡萄糖溶液的 pH值为3.81,5%葡萄糖+0.9%氯化钠注射液的pH值为3.58,这3种溶液均偏酸性,美洛西林钠对配伍后的pH值影响较大,因此,配伍后溶液的pH值变化较大。
3.5 美洛西林钠在pH值为5.5~7.5时较稳定,pH值<4.5时会有沉淀发生,pH值<4.0及>8.0效价下降较快。葡萄糖注射液的pH值为3.2~5.5,葡萄糖氯化钠注射液的pH值为3.5~5.5,且在实际应用中,发现两者pH值经常低于4.5。若考虑pH值的影响,则美洛西林钠在葡萄糖注射液和葡萄糖氯化钠注射液中应当不稳定,但本实验结果显示,二者配伍后能稳定存在,这可能说明美洛西林钠与葡萄糖氯化钠注射液和葡萄糖注射液配伍后稳定存在的pH值范围较宽,因此,虽然配伍后二者的pH值偏低,美洛西林钠仍能稳定存在。0.9%氯化钠注射液的pH值为4.5~7.0。因此,理论上美洛西林钠在0.9%氯化钠注射液中稳定,且本实验结果证实了这一推测。但美洛西林钠说明书的用法中,没有说明可以与0.9%氯化钠注射液配伍使用,且在临床曾发生过用0.9%氯化钠注射液配伍后出现沉淀的案例。推测其可能与以下几个方面有关:①配伍浓度。临床上根据病情的需要,常会增加美洛西林钠的用量,若剂量过大,当超过了美洛西林钠与0.9%氯化钠注射液的配伍浓度时,就会有沉淀析出。②温度。温度是影响药物稳定的一个重要因素,若温度过高,药物稳定性下降,可能会有沉淀析出。③配制配伍液时,氯化钠注射液的pH值不符合质量标准,超出了美洛西林钠稳定存在的pH值范围,美洛西林钠不能稳定存在,因而在使用过程中有沉淀析出。目前,关于美洛西林钠与0.9%氯化钠注射液配伍后出现沉淀的原因尚未明确。
3.6 目前,糖尿病患者数量不断增长,如果在输液时,使用葡萄糖注射液或葡萄糖氯化钠注射液作为溶媒,会增加其血糖浓度,加重患者的用药负担。为减轻糖尿病患者的负担,临床上糖尿病患者应尽量避免使用葡萄糖注射液液。本实验结果表明,美洛西林钠与氯化钠注射液配伍后稳定性好,临床上可以配伍使用。
3.7 配置样品的过程中,由于操作手法不专业,药物有所损失,存在人为误差,因此,我们以0 h的峰面积为100,以峰面积比代替峰面积,从而消除了人为误差的影响。
本实验结果表明,美洛西林钠与0.9%氯化钠注射液、10%葡萄糖注射液、5%葡萄糖注射液以及5%葡萄糖+0.9%氯化钠注射液配伍后稳定,临床上可配伍使用。
[1]谢映姿,谢奕如,江晓梅.美洛西林不良反应20例临床分析[J].中国医药,2008,3(9):526-527.
[2]黄汉清,秦斌.HPLC法测定注射用美洛西林钠的含量[J].中国药师,2002,5(2):98-99.
[3]胡伟,张礼菊.美洛西林钠注射液在6种输液中的稳定性[J].安徽药学,2003,7(2):92-93.

