新型壳聚糖衍生物吸附剂对Ni2+的吸附行为
唐雪娇,杨 丽,吴丰鹏,高 敏,沈伯雄
新型壳聚糖衍生物吸附剂对Ni2+的吸附行为
唐雪娇,杨 丽,吴丰鹏,高 敏,沈伯雄
(南开大学环境科学与工程学院,天津 300071)
利用Ni2+印迹法,通过交联和胺化反应自制新型多胺化球形Ni2+模板交联壳聚糖吸附剂(P-C-CTS(Ni)),研究吸附剂对Ni2+的吸附行为,通过模型拟合和吸附动力学对吸附过程和方式进行讨论.通过扫描电镜表征,P-CCTS(Ni)呈球体,内部具多孔结构.室温下对不同浓度Ni2+溶液进行吸附研究,吸附数据与Freundlich 模型和BET模型拟合较好,证明该吸附剂呈多孔结构,吸附性能好,吸附过程为多层分子吸附. 吸附动力学研究表明该吸附剂在不同温度下对Ni2+吸附过程均包括3个阶段,即外表面扩散吸附、内表面扩散吸附和平衡吸附. 30 ℃条件下,吸附数据对二级扩散方程拟合较好,二级速率常数k为8.119×10-3g/(mg·min),说明该吸附剂对Ni2+吸附机理以化学吸附为主,受化学吸附控制.
壳聚糖衍生物吸附剂;吸附等温模型;吸附动力学;扩散方程拟合
壳聚糖(chitosan,CTS)是甲壳素脱乙酰基产物,是一种天然氨基多糖,具有特殊的分子结构和良好的理化特性,近几年壳聚糖的开发利用受到越来越广泛的关注[1-6].壳聚糖为基质制备的生物吸附剂具有原材料丰富、成本低廉、吸附选择性高和可生物降解等优点,在环境修复领域具有更为广阔的应用前景[7-11].
壳聚糖在稀酸中主链会缓慢水解[12]等缺点严重制约其应用,而单一交联法会大大降低壳聚糖吸附性能[13-14].笔者前期研究中通过印迹法和交联-胺化法相结合,合成新型多胺化Ni2+模板改性壳聚糖吸附剂,改善了壳聚糖的抗酸性和机械强度,提高了重复利用性能,同时基体上引入大量胺基,吸附能力大大提高,模板化和胺化使其吸附容量由1.072,mmol/g提高到2.746, mmol/g,增加156%[15-16].
笔者重点考察多胺化球形Ni2+模板交联壳聚糖吸附剂(P-C-CTS(Ni))对Ni2+的吸附动力学特性,探讨其吸附行为和规律,为其工业应用提供基础数据.
1 材料和方法
1.1 仪器与材料
主要仪器有722分光光度计、DDHZ-300台式恒温振荡器、DHSJ-4A型实验室酸度计和日本SHIMADZU SS-550 扫描电子显微镜.
主要材料有壳聚糖粉末(脱乙酰度大于92%),四乙烯五胺(TEPA)、环氧氯丙烷(ECH)及其他试剂均为分析纯,水为去离子水.
1.2 吸附剂制备和表征
取一定量NiSO4·6H2O及壳聚糖粉末,Ni2+含量为25,mg/g,置于4%乙酸溶液中,搅拌均匀,溶胀12 h.用注射器将壳聚糖乙酸溶液注入稀碱液中,制成直径约2.0,mm小球.放置24 h后水洗至中性,得Ni-CTS,湿态保存.
称取10.0,g,Ni-CTS(湿重),加入50,mL水和1.5,mL的交联剂ECH,80,℃恒温水浴5,h进行交联.完成后用水洗至中性,得C-Ni-CTS,再加入30,mL胺化剂TEPA和等体积的水,60,℃恒温水浴中胺化5,h.水洗至中性,得P-C-Ni-CTS.将P-C-Ni-CTS加入稀H2SO4进行振荡解吸,水洗至无Ni2+检出,最后置于稀碱液中碱化1,h,水洗至中性,得P-CCTS(Ni),湿态保存,待用[15-16].
对50 ℃真空干燥至恒重的P-C-CTS(Ni)外观及剖面进行扫描电镜(SEM)分析.
1.3 吸附量测定方法
溶液中Ni2+浓度由丁二酮肟分光光度法测定.吸附剂对溶液中Ni2+的吸附量为

式中:Qt为吸附t时间后的吸附量,mg/g;0ρ为溶液中Ni2+的初始质量浓度,mg/L;tρ为吸附t时间后溶液中Ni2+的质量浓度,mg/L;m为吸附剂质量(干重),g.
1.4 平衡吸附量和动力学数据获取
吸附剂平衡吸附量测定方法:称取一定量P-CCTS(Ni),加入初始质量浓度范围在0.1~2.0,g/L的Ni2+溶液25.0,mL,室温下振荡平衡24,h,测定溶液中Ni2+浓度(即平衡浓度ρe),由式(1)计算得到平衡吸附量Qe.
吸附剂在不同温度(30,℃、40,℃、50,℃)下的吸附动力学数据的获取:平行取6份P-C-CTS(Ni)于不同温度下进行动力学实验,其中Ni2+初始质量浓度0ρ=100,mg/L,溶液体积V=25.0,mL,同一振荡条件下,1~8,h内定期同时取样测定各溶液中Ni2+的质量浓度tρ,根据式(1)计算时间t内的吸附量Qt.
2 结果与讨论
2.1 SEM分析
50,℃真空干燥至恒重的P-C-CTS(Ni)外观及剖面SEM照片分别如图1和图2所示.
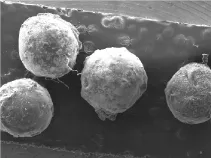
图1 P-C-CTS(Ni)外观SEM照片Fig.1 SEM photogragh for appearances of P-C-CTS(Ni)

图2 P-C-CTS(Ni)内部剖面SEM照片Fig.2 SEM photogragh for internal cross-section of P-C-CTS(Ni)
由图1可知,制备的P-C-CTS(Ni)经过50,℃真空干燥后,仍呈球体,大小均匀,直径为1.0,mm左右.
由图2可知,P-C-CTS(Ni)内部呈很多孔结构.这些孔结构影响着吸附剂的吸附方式和规律.2.2 吸附等温线拟合
图3为P-C-CTS(Ni)对Ni2+平衡吸附量Qe随溶液中Ni2+平衡的质量浓度ρe的变化曲线,溶液pH为5.0~5.5,室温.由图3可知,随着溶液中Ni2+平衡浓度ρe的增加,平衡吸附量Qe也相应增大,吸附属于Ⅴ型吸附[17],是典型的“S”型等温线[18].在较低的平衡浓度时,溶剂相对溶质有强烈的竞争吸附;当平衡浓度增大时,等温线有一较快上升阶段,这是被吸附的溶质分子对液相中溶质分子吸引的结果.然后又出现平缓阶段,说明发生多层吸附;随浓度增大发生与气体吸附相类似的毛细凝结现象,也可说明该吸附剂具备多孔结构.
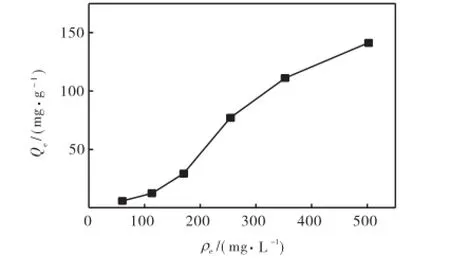
图3 平衡吸附量Qe与Ni2+平衡质量浓度ρe的关系曲线Fig.3 Relationship between adsorption capacities Qeand ρe
用Langmuir和Freundlich 模型描述吸附等温线.以ρe/Qe-ρe和lg Qe-lg ρe分别作图,见图4.
Langmuir等温方程为

式中:Qe为不同平衡浓度下的平衡吸附量,mg/g;Qm为吸附容量,mg/g;ρe为吸附后Ni2+的平衡质量浓度,mg/L;a、K和n均为常数.
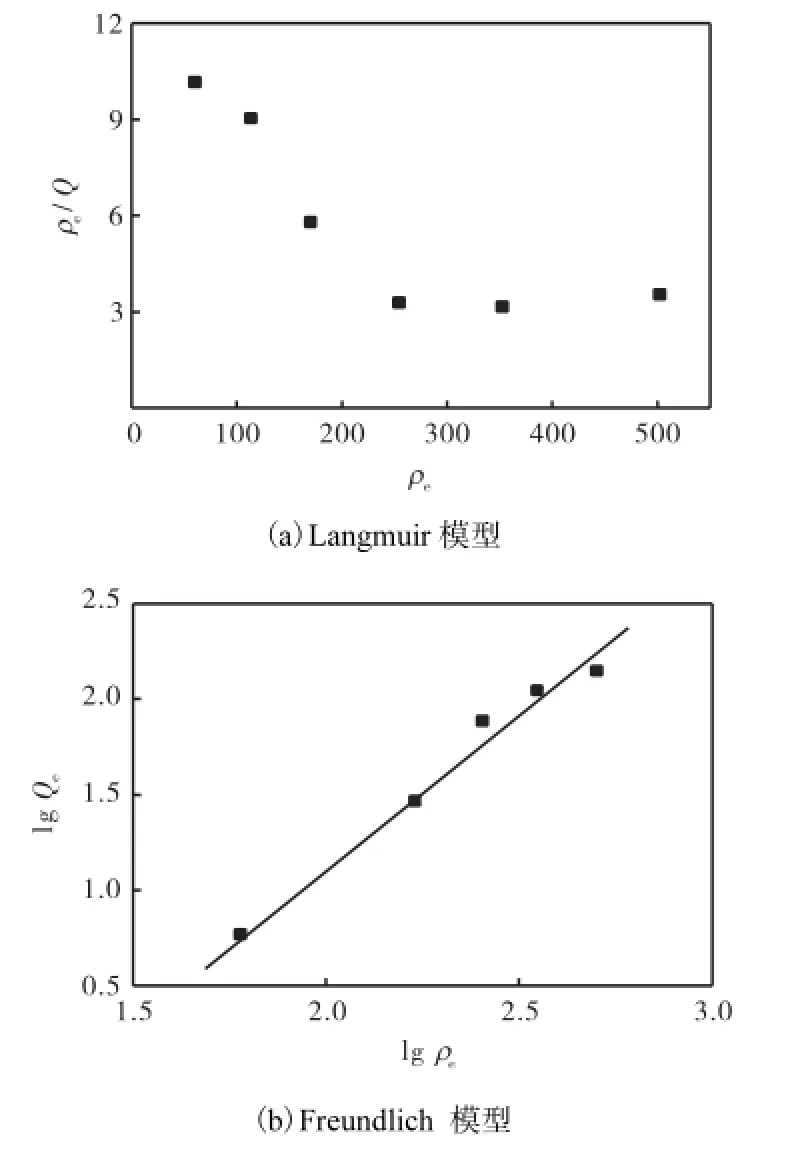
图4 吸附剂的吸附等温线拟合Fig.4 Adsorption isotherm of sorbent
图4 (a)曲线与Langmuir方程不符,图4(b)曲线与Freundlich方程的标准偏差为0.083,5,符合较好,说明该吸附剂对Ni2+的吸附方式为多分子层吸附,固体表面是呈多孔不均匀的.与上述结论是一致的.
以ρe/(Qe(ρs-ρe))-ρe/ ρs作图,见图5.
BET 吸附等温方程为
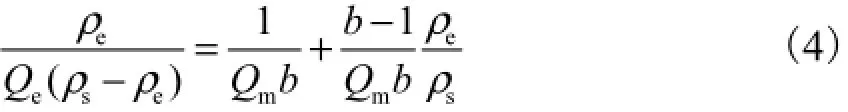
式中:Cs为金属离子的饱和质量浓度,mg/L;b为常数.
由图5可知,当溶液中Ni2+初始质量浓度大于0.5,g/L,ρe/(Qe(ρs-ρe))- ρe/ρs线性相关性良好,R2= 0.998 3,符合BET吸附模型.说明在较高Ni2+初始浓度溶液中,吸附剂表面实现多层分子吸附.
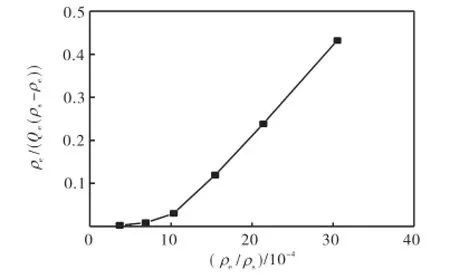
图5 吸附剂的BET吸附等温线Fig.5 BET adsorption isotherm of sorbent
2.3 吸附动力学
通过动力学实验,得1~8,h吸附动力学曲线(见图6).由图6(a)可知,不同温度下的吸附规律一致:在开始阶段,Qt随t的增加显著增大;之后,随反应时间的增长,Qt的增加速度逐渐减小;大约240,min后Qt基本不变.相应的吸附过程为3个阶段:首先Ni2+主要被吸附在吸附剂外表面;达到饱和后,Ni2+开始沿吸附剂表层孔径向内部扩散,同时内表面吸附发生;最后经过一段时间达到吸附平衡.
由于图6(a)中,1~2,h内吸附过程比较复杂,为便于观察,将图6(a)中虚线内曲线(1~2,h)单独作图,见图6(b).由图6(b)可知,不同温度下3个曲线都存在一个短暂的吸附平衡阶段,此阶段是吸附剂外表面对Ni2+吸附达到瞬间平衡后溶液沿吸附剂表层孔径向内部开始扩散的过程,此时在内部表面Ni2+吸附还未发生,所以溶液中的Ni2+含量未发生变化;之后Ni2+在孔径内开始发生吸附而使溶液中的Ni2+含量降低,但Ni2+在内孔扩散和吸附速率相对较慢.此吸附现象也证明吸附剂具有多孔结构,与吸附等温线所得结论一致.
由图6(b)可知,不同温度下,短暂平衡开始时刻不同,即外表面达到吸附平衡后含Ni2+溶液向孔径内扩散的开始时间不同.30,℃时吸附40,min后开始进入短暂平衡阶段;40,℃时吸附30,min后开始进入短暂平衡阶段;而50,℃时仅吸附20,min就开始.由此可知,温度越高,Ni2+在吸附剂外表面达到吸附平衡所需时间越短,并且吸附量Qt越大,说明该吸附机制为化学吸附.这也与该吸附剂的制备路线吻合.通过胺化,吸附剂表面引入大量活性氨基,包括壳聚糖分子中的酰胺基都是吸附Ni2+的活性位点,通过胺基上氮原子的孤对电子对Ni2+发生螯合实现吸附.
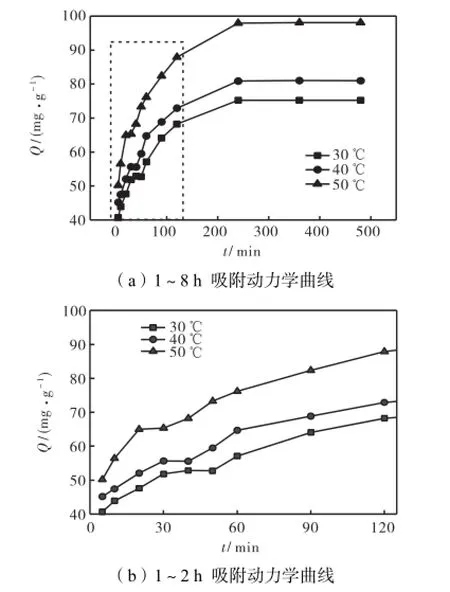
图6 不同温度下P-C-CTS(Ni)对Ni2+的吸附量随时间变化曲线Fig.6 Relationships of adsorption quantities of Ni2+to P-CCTS(Ni)and time at different temperatures
假设Ni2+在吸附剂外表面达到短暂吸附平衡时接近单层吸附饱和,以各个温度下表面吸附短暂平衡时间内t/Qt-t作图,得3条直线,如图7所示.其吸附动力学方程为

式中k为表观吸附速率常数.由斜率和截距可分别求得Qe和k值,结果列于表1中.
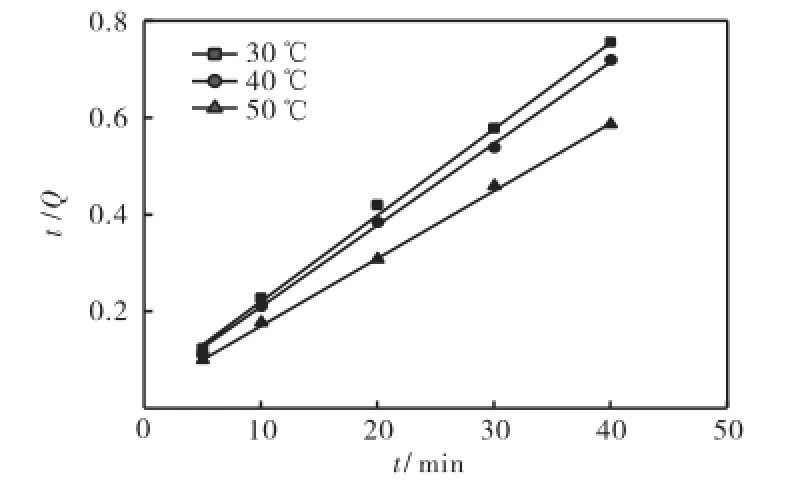
图7 P-C-CTS(Ni)对Ni2+的吸附动力学曲线Fig.7 Adsorption kinetic curves for adsorptions of Ni2+to P-C-CTS(Ni)
由Arrhenius方程k=Ae-Ea/RT,得lg k=-E/2.303RT +alg A.由表1可知,lg,k与1/T并不呈线性关系,表明温度对吸附速率的影响不服从Arrhenius方程.研究传质、化学反应等吸附过程的控制机制,常用一级、二级和内部扩散方程来测定试验参数.
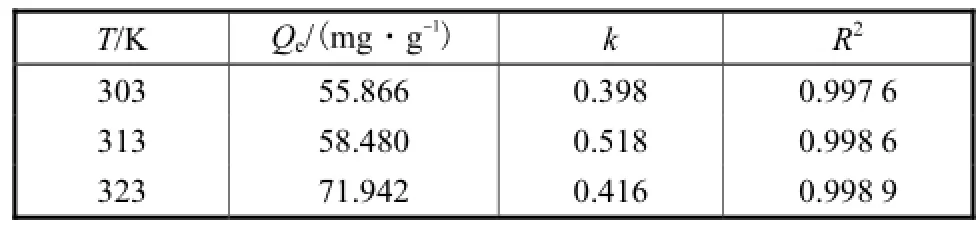
表1 不同温度下的吸附动力学参数Tab.1 Adsorption kinetic parameters at different temperatures
一级动力模型为
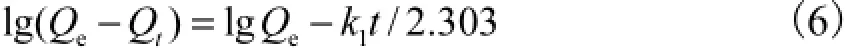
式中k1为一级吸附速率常数,min-1.通过lg(Qe-Qt)-t直线图可得Ni2+在不同浓度范围内速率常数k1和相关系数.
二级动力模型为

式中k2为二级吸附速率常数,g/(mg·min).通过t/Qt-t直线图可得到速率参数k2和相关系数R22.
内部扩散模型为

式中ki为内部扩散速率,mg/(g·min0.5).ki为Qt-t0.5直线的斜率,相关系数为R32.
对30 ℃时吸附动力学曲线进行一级、二级和内部扩散方程拟合,得P-C-CTS(Ni)对Ni2+吸附动力学参数,结果列于表2中.

表2 30,℃条件下吸附剂在前30 min内对Ni2+吸附动力学参数Tab.2 Kinetic parameters for Ni2+adsorption at 30,℃ for the first period of 30,min
二级模型以化学吸附为速控步骤.依据相关系数,用二级方程表示P-C-CTS(Ni)对Ni2+的吸附行为较好,可得二级吸附速率常数k2为8.119×10-3g/(mg·min),说明该吸附过程以化学吸附为主,受化学吸附控制.
3 结 语
自制多胺化球形Ni2+模板交联壳聚糖吸附剂(PC-CTS(Ni)),研究该吸附剂对Ni2+的吸附行为.在pH 5.0~5.5、室温下吸附剂对Ni2+的等温吸附为典型的“S”型,等温吸附线与Freundlich模型吻合较好,说明该吸附剂对Ni2+的吸附方式为多分子层吸附,固体表面是呈多孔不均匀的;在较高Ni2+质量浓度(>0.5,g/L)时,等温吸附与BET模型吻合很好,验证了吸附剂表面为多层分子吸附;吸附动力学研究表明该吸附剂在不同温度(30,℃、40,℃和50,℃)下对Ni2+吸附过程均包括3个阶段(外表面扩散吸附、内表面扩散吸附和平衡吸附);对30,℃吸附动力学曲线分别进行一级、二级和内部扩散方程拟合,结果表明,吸附数据对二级扩散方程拟合较好,二级速率常数k为8.119×10-3,g/(mg·min),表明吸附剂对Ni2+吸附以化学吸附为主.
[1] Schiffman J D,Schauer C L. Cross-linking chitosan nanofibers[J]. Biomacromolecules,2007,8(2):594-601.
[2] Monvisade P,Siriphannon P. Chitosan intercalated montmorillonite:Preparation,characterization and cationic dye adsorption[J]. Applied Clay Science,2009,42(3/4):427-431.
[3] Sahin M,Kocak N,Arslan G,et al. Synthesis of crosslinked chitosan with epichlorohydrin possessing two novel polymeric ligands and its use in metal removal[J]. Journal of Inorganic and Organometallic Polymers and Materials,2011,21(1):69-80.
[4] Chiou Shaohua,Wu Wenteng. Immobilization of candida rugosa lipase on chitosan with activation of the hydroxyl groups[J]. Biomaterials,2004,25(2):197-204.
[5] Park S,Lee S J,Chung H,et al. Cellular uptake pathway and drug release characteristics of drugencapsulated glycol chitosan nanoparticles in live cells[J]. Microscopy Research and Technique,2010,73(9):857-865.
[6] Fajardo P,Martins J T,Fucinos C,et al. Evaluation of a chitosan-based edible film as carrier of natamycin to improve the storability of saloio cheese[J]. Journal of Food Engineering,2010,101(4):349-356.
[7] Zonoozi M H,Moghaddam M R A,Arami M. Study on the removal of acid dyes suing chitosan as a natural coagulant/coagulant aid[J]. Water Science and Technology,2011,63(3):403-409.
[8] Fu H T,Kobayashi T. Self-assembly functionalized membranes with chitosan microsphere/polyacrylic acid layers and its application for metal ion removal[J]. Journal of Materials Science,2010,45(24):6694-6700.
[9] Saitoh T,Asano K,Hiraide M. Removal of phenols in water using chitosan-conjugated thermo-responsive polymers[J]. Journal of Hazardous Meterials,2011,185(2/3):1369-1373.
[10] Cao Jie,Tan Yebang,Che Yuju,et al. Novel complex gel beads composed of hydrolyzed polyacrylamide and chitosan:An effective adsorbent for the removal of heavy metal from aqueous solution[J]. Bioresource Technology,2010,101(7):2558-2561.
[11] Liu Tingyi,Zhao Lin,Sun Desheng,et al. Entrapment of nanoscale zero-valent iron in chitosan beads for hexavalent chromium removal from wastewater[J]. Journal of Hazardous Materials,2010,184(1/2/3):724-730.
[12] 黄金明,金鑫荣. 天然高分子壳聚糖作为吸附剂的吸附特性研究[J]. 高等学校化学学报,1992,13(4):535-536.
Huang Jinming,Jin Xinrong. A study of adsorption property of natural polymer chitosan as adsorption[J]. Chemical Research in Chinese Universities,1992,13(4):535-536(in Chinese).
[13] Koyama Y,Taniguchi A. Studies on chitin X. homogeneus crosslinking of chitosan for enhanced ion adsorption[J]. Journal of Applied Polymer Science,1986,31(7):1951-1954.
[14] Hsien Tzu-Yang,Rorrer G L. Heterogeneous crosslinking of chitosan gel beads:Kinetics,modeling and influence on cadmium ion adsorption capacity[J]. Industrial and Engineering Chemistry Research,1997,36(9):3631-3638.
[15] 张宝贵,唐雪娇,曹 梦,等. 一种新型壳聚糖衍生物吸附剂的制备及应用:CN,CN101007264[P]. 2008-11-12.
Zhang Baogui,Tang Xuejiao,Cao Meng,et al. The Synthesis and Application of a Novel Chitosan Derivatives Adsorbent:CN,CN101007264[P]. 2008-11-12 (in Chinese).
[16] 唐雪娇,曹 梦,毕成良,等. 新型吸附剂的合成、表征及其对Ni(Ⅱ)的吸附研究[J]. 化学学报,2007,65(23):2771-2775.
Tang Xuejiao,Cao Meng,Bi Chengliang,et al. Study on the synthesis and characterization of a novel adsorbent and adsorption property to Ni(Ⅱ)[J]. Acta Chimica Sinica,2007,65(23):2771-2775(in Chinese).
[17] 颜肖慈,罗明道. 界面化学[M]. 北京:化学工业出版社,2005.
Yan Xiaoci,Luo Mingdao. Intersurface Chemstry[M]. Beijing:Chemical Industry Press,2005(in Chinese).
[18] 朱 瑶,赵振国. 界面化学基础[M]. 北京:化学工业出版社,1996.
Zhu Yao,Zhao Zhenguo. Intersurface Chemstry Fundamentals[M]. Beijing:Chemical Industry Press,1996(in Chinese).
Adsorption Behavior of Ni2+onto New Chitosan Derivative Sorbent
TANG Xue-jiao,YANG Li,WU Feng-peng,GAO Min,SHEN Bo-xiong
(School of Environmental Science and Engineering,Nankai University,Tianjin 300071,China)
A new chitosan derivative sorbent (P-C-CTS(Ni)) was prepared by crosslinking and amination reactions with Ni2+imprinting method. The adsorption behaviors of P-C-CTS(Ni) were investigated by model-fitting and kinetics studies. The appearance and porous structure of P-C-CTS(Ni)were characterized by SEM. Under varied concentration of Ni2+at room temperature, the isotherm adsorptions were fitting both Freundlich model and BET model,indicating that the sorbent had porous structure and carried out a multilayer molecule adsorption process. The results show that there are three steps for Ni2+adsorption at different temperatures (surface diffusion adsorption, internalsurface diffusion adsorption and balance adsorption). The data at 303 K correlate well with the second-order kinetic model,the sorption rate constant being 8.119×10-3g/(mg·min), which indicates that chemical sorption is the main sorption mechanism and controls the adsorption procedures.
chitosan derivative sorbent;adsorption isotherm;adsorption kinetics;diffusion equation fitting
Q539
A
0493-2137(2011)11-0979-05
2011-03-30;
2011-05-17.
国家自然科学基金资助项目(50976050);中央高校基本科研业务费专项资金资助项目(65010451).
唐雪娇(1980— ),女,博士,讲师.
唐雪娇,tangxuejiao@nankai.edu.cn.
- 天津大学学报(自然科学与工程技术版)的其它文章
- 三U型填充真空集热管热性能理论分析
- 表面活性剂在同时脱硫脱氮中的应用
- 镍基单晶高温合金DD3强流脉冲电子束的表面改性
- 专家点评

