升麻及其炮制品的HPLC指纹图谱研究
王 冰, 张振秋, 孙艳涛, 李 力, 邓雪男(辽宁中医药大学药学院,辽宁大连 116600)
升麻及其炮制品的HPLC指纹图谱研究
王 冰, 张振秋*, 孙艳涛, 李 力, 邓雪男(辽宁中医药大学药学院,辽宁大连 116600)
目的 RP-HPLC法建立升麻指纹图谱。方法 采用Phenomsil BDS C18(250 mm×4.6 mm,5 μm)色谱柱;流动相为乙腈(A)-0.1%磷酸水溶液(B)梯度洗脱,0~5 min(88%A ∶12%B),25 min(80%A ∶20%B),45 min(70%A ∶30%B),60min(60%A∶40%B),检测波长316 nm,柱温40℃;体积流量1.0 mL/min;进样量10 μL。结果 建立了升麻的HPLC指纹图谱,标定出15个共有指纹峰。结论 升麻药材的指纹图谱可用于升麻的定性鉴别,为升麻药材的质量控制提供参考依据。
升麻;指纹图谱
升麻为毛茛科植物大三叶升麻Cimicifuga heracleifoliaKom.、兴 安 升 麻Cimicifugadahurica(Turcz.)Maxim.或升麻Cimicifuga foetidaL.的干燥茎。始载于《神农本草经》,列为上品。其味辛、微甘,性微寒。归肺、脾、胃、大肠经。具有发表透疹、清热解毒、升举阳气的功效。用于风热头痛,齿痛,口疮,咽喉肿痛,麻疹不透,阳毒发斑;脱肛,子宫脱垂[1]。升麻中含有有机酸、糖苷、色原酮、挥发油、甾醇等多种类型的化学成分[2]。当前对中药指纹图谱的研究较多[3-4],主要有 GC[5-6]和 HPLC 法[7-8]。对升麻的研究主要集中于定量测定[9]和成分分析[10]方面。本实验采用RP-HPLC法建立并分析升麻的指纹图谱[11],为升麻药材及其炮制品的质量评价提供参考。
1 仪器与试药
1.1 仪器 Agilent1100高效液相色谱仪(仪器编号:20041191 DE43607375),配置四元梯度泵,在线脱气机,VWD检测器;Phenomsil BDS C18(250 mm×4.6 mm,5 μm)色谱柱;METTLER AB135-S 十万分之一电子分析天平(瑞士);AR2140电子分析天平(上海奥豪斯公司)。
1.2 试药 异阿魏酸(中国药品生物制品检定所,批号111698-200602)。升麻药材经辽宁中医药大学李峰教授鉴定均为正品药材。样品编号依次为1~10;升麻炒炭品由北京商品地生品依药典方法自制,样品编号为11;蜜炙品购自上海,样品编号为12;来源、种类和收集时间见表1;水为重蒸馏水,甲醇、乙腈(天津市科密欧化学试剂有限公司,色谱纯),磷酸(天津市科密欧化学试剂有限公司,分析纯)。
2 方法与结果
2.1 色谱条件 Phenomsil BDS C18(250 mm×4.6 mm,5 μm)色谱柱;流动相:乙腈(A)-0.1% 磷酸水溶液(B)(13∶87);流动相梯度:0~5 min(88%A∶12%B),25 min(80%A ∶20%B),45 min(70%A∶30%B),60 min(60%A ∶40%B),检测波长为 316 nm;柱温:40 ℃;体积流量:1.0 mL/min。
2.2 参照物溶液的制备 取异阿魏酸对照品适量,精密称定,置棕色量瓶中,加10%乙醇制成每1 mL含异阿魏酸202.8 μg的溶液,即得。
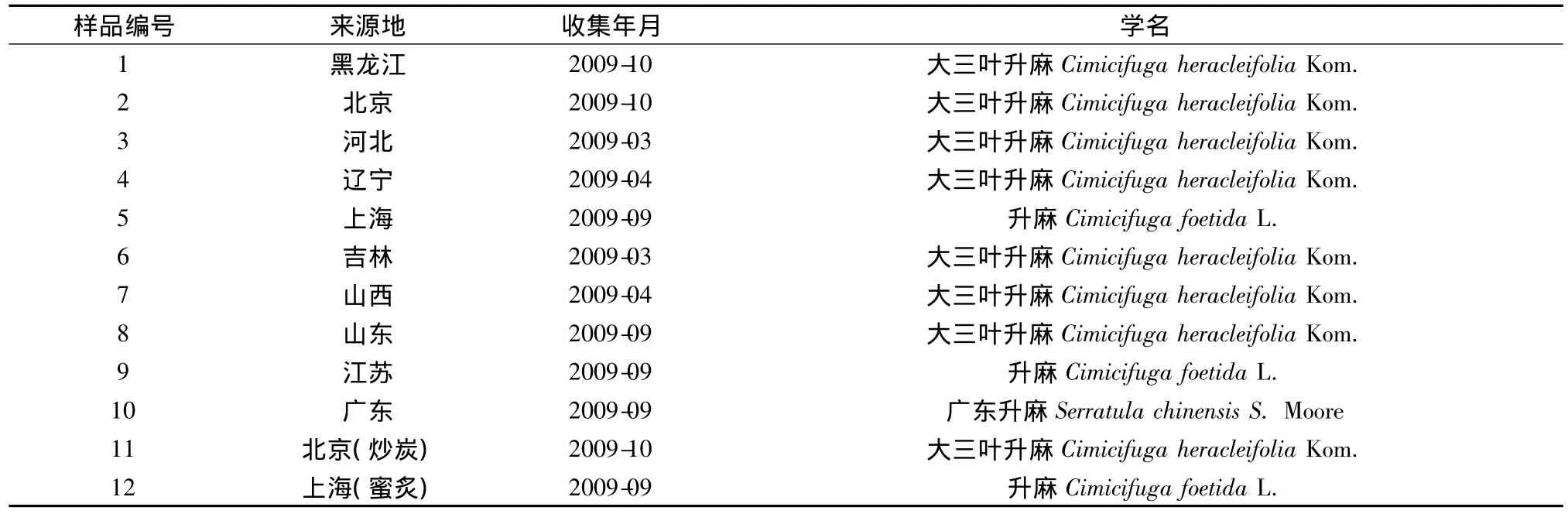
表1 不同商品地升麻药材Tab.1 Cimicifuga from different resources
2.3 供试品溶液的制备 分别称取1~12号药材粉末(过2号筛)约1 g,精密称定,置50 mL烧瓶中,加入30%乙醇20 mL,密塞,加热回流1.5 h,放冷,滤过,滤液置25 mL量瓶中,加30%乙醇稀释至刻度,摇匀,取续滤液,即得。
2.4 测定法 在2.1项色谱条件下,分别精密吸取参照物溶液和供试品溶液各10 μL,注入液相色谱仪,测定,记录色谱图,即得。参照物和样品指纹图谱见图1。
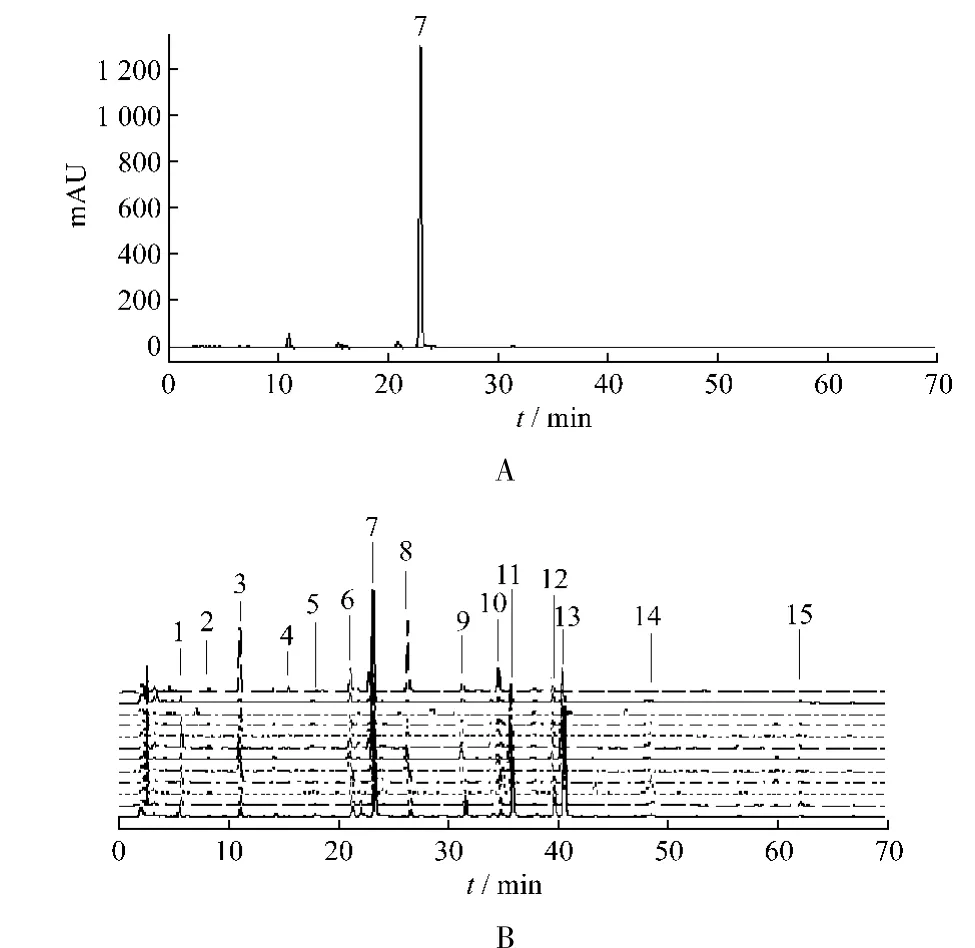
图1 对照品异阿魏酸(A)和样品(B)的HPLC色谱Fig.1 HPLC chromatograms of reference substances:iso-ferulate(A),sample(B)
2.5 精密度实验 取5号样品,按样品制备方法进行制备,在所建立的测定条件下,连续进样5次,以异阿魏酸峰位参照峰,实验结果得出色谱图中各特征峰相对保留时间的RSD<0.27%;相对峰面积(特征峰所占比例大于1%)的RSD<5%,表明精密度良好。
2.6 重复性实验 取5号样品5份,按样品制备方法进行制备,在所建立的测定条件下测定,以异阿魏酸峰位参照峰,实验结果得出色谱图中各特征峰相对保留时间的RSD<0.19%;相对峰面积(特征峰所占比例大于1%)的RSD<5%,表明方法的重复性良好。
2.7 稳定性实验 取5号样品,按样品制备方法进行制备,在所建立的测定条件下,分别在0、1、2、4、8、12 h进行测定,实验结果表明各特征峰相对保留时间的RSD<0.17%,相对峰面积(特征峰所占比例大于1%)的RSD<5%,表明样品的稳定性良好。
2.8 测定结果 取除10号样品外的11批升麻样品,按供试品制备方法,在2.1项色谱条件下,分别精密吸取10 μL,注入液相色谱仪,测定,11批样品出峰总数及共有峰所占的比例见表2。
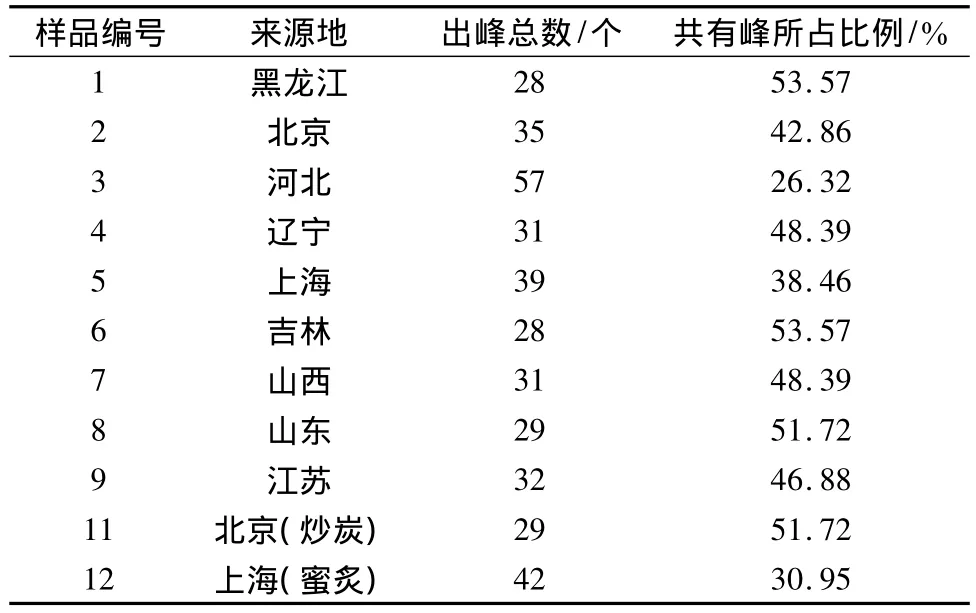
表2 各样品的出峰总数及其共有峰所占比例Tab.2 Numbers of sample peaks and proportion of common peaks
使用Excel 2003按照相关系数公式和夹角余弦公式[12]分析各个商品地及两种炮制品的保留时间和峰面积,计算相似度,结果见表3、表4。

表3 各峰相对保留时间的夹角余弦和相关系数计算结果Tab.3 The calculation result of cosine of the angle and correlation coefficient for relative retention times

表4 各峰相对峰面积的夹角余弦和相关系数计算结果Tab.4 The calculation result of cosine of the angle and correlation coefficient for relative peak areas
10 号样品的图谱中未出现参照物异阿魏酸峰,而在计算各峰相对保留时间和相对峰面积的夹角余弦和相关系数时,需要将样品中异阿魏酸峰的保留时间和峰面积作为1(作为分母),再将其他峰的保留时间和峰面积与之相比,得出相对保留时间和相对峰面积,利用得到的数据计算出夹角余弦和相关系数。所以10号样品无法根据异阿魏酸峰计算夹角余弦和相关系数。10号样品与其他样品比较(以1号样品为例),样品各峰的保留时间、与15个共有峰符合的峰数见表5。
3 讨论
3.1 根据中华人民共和国药典中指纹图谱测定方法,在选定的色谱条件下,建立了9个不同商品地升麻HPLC指纹图谱,标定出15个共有指纹峰;2个常用炮制品的HPLC指纹图谱,炒炭升麻具有15个共有特征峰;蜜炙升麻只具有13个共有特征峰。将炮制品与生品的指纹图谱相比较可知,升麻经炮制前后出峰总数和峰面积不完全相同,说明有效成分发生了变化。

表5 1号样品各峰的保留时间及其与10号样品共有峰数的比较Tab.5 The relative retention time of sample 1 and numbers of common peaks comparison between samples 1 and 10
3.2 实验通过紫外可见分光光度法测定供试品溶液,发现在316 nm处有较大吸收,所以选择316 nm为检测波长。
3.3 根据建立的指纹谱图,1~9批升麻药材的指纹图谱中15个共有峰相对保留时间符合程度较好,共有峰占总峰面积的90%以上;但各个峰的相对峰面积存在一定差异,说明不同来源的1~9批升麻药材质量是有差别的。
3.4 从表2可知,各样品的非共有峰数差异较大,说明不同来源的升麻所含有的成分存在差别,这可能与药材生长的地理位置、环境、气候、采收季节和时间等因素有关。
3.5 将北京和上海两地的生、炮制品进行比较:包括共有峰在内,蜜炙升麻中部分化学成分显著增加,异阿魏酸的峰面积有所减小;炒炭升麻中异阿魏酸的峰面积增加,而其他成分的峰面积显著减小甚至消失。说明炮制前后升麻所含的化学成分发生改变,可以从图谱中看出。
3.6 由广东商品地购买的升麻药材为菊科植物麻花头的根,主产于广东、福建等地,在当地习惯作升麻使用。其特征峰的数量以及所占的比例均小。本实验建立升麻的指纹图谱,而广东升麻与升麻不属于同种药材,所以在数据统计时未加入有关广东升麻(10号样品)的数据。根据实验建立的指纹图谱中特征峰种类和数目、共有峰相对保留时间差异等可对升麻进行定性鉴别、对同名不同物的药材加以区别。实验建立的指纹图谱可作为控制升麻及其炮制品内在质量的标准之一。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:68.
[2]张庆文,叶文才,赵守训,等.兴安升麻的化学成分研究[J].中草药,2002,(8):683-685.
[3]王 微,康云鹰.论中药指纹图谱利弊及其应用前景[J].现代中医药,2009,3(2):70-72.
[4]周 锐.现代中药质量标准体系与中药指纹图谱[J].中医中药,2007,7(4):221.
[5]康春珍,康志英,孔颜霜,等.沉香药材GC指纹图谱的研究[J].广东药学院学报,2006,22(6):610-623.
[6]李小妹,潭光华.石牌广藿香与海南广藿香挥发油的指纹图谱分析[J].广东药学院学报,2007,22(6):641-643.
[7]杨 瑛,王实强,蔡光先.蒲黄药材HPLC指纹图谱标准研究[J].中华中医药杂志,2008,23(5):444-446.
[8]陈 玉,郑 萍.川产葛根药材的HPLC指纹图谱[J].华西药学杂志,2008,23(2):217-218.
[9]王 冰,张振秋,孙艳涛.HPLC切换波长法同时测定升麻中5种成分的含量[J].药物分析杂志,2011,31(2):391-394.
[10]李从军,李英和.升麻中的三萜类成分[J].药学学报,1994,29(6):449-453.
[11]陈思妮,张振秋.广金钱草HPLC指纹图谱的研究[J].中成药,2008,30(9):1249-1252.
[12]苗爱东,孙殿甲.Excel 2002在中药指纹谱相似度计算中的应用[J].药学进展,2003,27(1):51-54.
WANG Bing, ZHANG Zheng-qiu*, SUN Yan-tao, LI Li, DENG Xue-nan
(College of Pharmacy,Liaoning Univesity of Traditional Chinese Medicine,Dalian 116600,China)
Cimicifuga;fingerprint
R284.1
A
1001-1528(2011)07-1106-04
2010-06-21
王 冰(1982—),女,硕士生,研究方向:药物分析。E-mail:wb20040312@163.com
*通信作者:张振秋,男,博士生导师,教授。Tel:(0411)87586058,E-mail:zhangzhenqiu@sina.com
HPLC fingerprint of Cimicifuga and its processed products

