利用聚钙黄绿素薄膜修饰电极测定黄嘌呤
周谷珍,唐倩倩,孙元喜
利用聚钙黄绿素薄膜修饰电极测定黄嘌呤
周谷珍,唐倩倩,孙元喜
(湖南文理学院 化学化工学院 湖南 常德 415000)
利用循环伏安法, 制备出具有良好催化活性的聚钙黄绿素薄膜修饰电极(PCALE). 利用PCALE对黄嘌呤(Xa)的电催化作用, 建立了对黄嘌呤含量定量分析的电分析方法. 在0.02 mol/L PBS(pH= 6.8)+ 0.2 mol/L KNO3体系中, 黄嘌呤的浓度在5.0×10-6~ 1.0×10-4mol/L范围内与峰电流呈良好的线性关系, 线性回归方程和线性相关系数分别为:p=-0.010 5-2.09,= 0.998 9, 检出限可达2×10-7mol/L. 利用该法对尿液中的黄嘌呤进行定量分析, 得到满意结果. 5次样品分析结果的相对标准偏差小于2%.
聚钙黄绿素; 修饰电极; 黄嘌呤; 电催化
黄瞟呤(Xanthine, 简称Xa)即2, 6-二羟基瞟呤, 存在于动物的血液、肝脏和尿中, 是嘌呤核苷酸分解代谢的中间产物, 其含量直接影响血液中尿酸的含量. 体液中Xa含量的测定对临床医学具有一定的实际意义. 目前, 文献报道测定Xa的电化学方法主要使用玻碳电极、热解石墨电极、碳糊电极等化学修饰电极[1-3]作为工作电极, 而用电聚合物薄膜修饰电极作为工作电极定量测定Xa的研究很少报道.
本文利用循环伏安法将生物染料钙黄绿素电聚合于玻碳电极表面, 制备出性能良好的聚钙黄绿素薄膜修饰电极; 利用该修饰电极对黄嘌呤的电催化作用, 建立了测定尿液中黄嘌呤的新方法.
1 实验部分
1.1 仪器与试剂
1.1.1 仪器
CHI660电化学工作站(上海辰华仪器公司); SB3200超声波清洗器(上海超声波仪器厂); 100 μL微量进样器(上海医用激光仪器厂); 实验过程采用三电极系统: 工作电极为玻碳电极(直径3 mm, 天津兰力科公司) 或聚钙黄绿素薄膜修饰电极(PCALE, 自制), 铂电极为辅助电极, 饱和甘汞电极为参比电极.
1.1.2 试剂
黄嘌呤(AR, 进口分装), 用磷酸配置成1.0× 10-3mol/L标准溶液; 钙黄绿素(简称CAL, AR, 湘中地质实验研究所), 配置成1.0×10-4mol/L 水溶液; 0.05 mol/L 磷酸盐缓冲溶液(pH=6.8, 简称PBS)等其余试液, 均采用分析纯试剂配制而成; 实验用水为2次石英蒸馏水, 实验过程无须通氮除氧且在室温下进行.
1.2 聚合物薄膜修饰电极的制备
1.2.1 基体玻碳电极的预处理
将玻碳电极(GC)在5#金相砂纸上打磨后, 在抛光机上抛光成镜面, 然后依次用1:1硝酸, 1:1乙醇, 蒸馏水超声清洗(每次约10 min).
将清洗后的电极在0.5 mol/L硫酸溶液中, 用循环伏安法在-0.5~1.4 V的电位范围内循环扫描至循环伏安图稳定止(约10周), 达到活化电极表面的效果.
1.2.2 PCALE的制备
在0.02 mol/L PBS (pH=6.86)+0.2 mol/L KNO3+ 1.0×10-4mol/L CAL聚合体系中, 采用循环伏安法, 控制扫描电位范围为:-1.4~1.8 V, 以50 mV/s的速率, 循环扫描电聚合20周, 即可制得性能稳定的PCALE.
1.3 实验方法
以PCALE为工作电极, 在含邻苯二酚的测试体系中, 控制电位范围为-0.3~0.7 V, 以100 mV/s的扫描速率进行循环伏安扫描, 根据CV图, 利用修饰电极对邻苯二酚的电催化作用, 考察修饰电极的性能. 以PCALE为工作电极, 在含Xa的体系中, 控制电位范围为0.5~1.2 V, 以100 mV/s的扫描速率进行CV扫描, 根据CV图上峰电流的大小, 进行Xa的定量分析.
2 结果与讨论
2.1 PCALE对黄嘌呤的电催化作用
2.1.1 Xa在PCALE上的循环伏安行为
将裸玻碳电极(GCE)和PCALE分别放入0.02 mol/L PBS (pH=6.8) +0.2 mol/L KNO3+ 1.0×10-5mol/L黄嘌呤的测试体系中, 记录循环伏安图(图1). 从图中可以看出: PCALE对Xa的氧化具有十分明显的电催化作用, 氧化峰电位为0.74 V.

测试体系: 0.02 mol/L PBS(pH=6.8)+0.2 mol/L KNO3+ 1.0×10-5mol/L Xa
扫描电位: 0.5 ~ 1.2 V 扫描速率: 100 mV/s
曲线1: GCE在测试体系中的CV曲线
曲线2: PCALE在测试体系中的CV曲线
图1 PCALE与GCE在测试体系中的循环伏安曲线
2.1.2 影响黄嘌呤氧化峰电流的因素
2.1.2.1 测试体系的选择
分别在0.02 mol/L PBS(pH=6.86)、0.10 mol/L CH3COOH-CH3COONa(pH=4.74)、0.10 mol/L HCl体系中加入等量的黄嘌呤, 在0.5~1.2 V电位范围内, 以100 mV/s的扫速进行循环伏安扫描. 通过实验发现: 在0.05 mol/L PBS(pH=6.8)缓冲体系中效果最好, 说明黄嘌呤在弱酸性条件下具有较好的电化学活性, 所以确定在弱酸性环境中对黄嘌呤进行分析.
2.1.2.2 测试体系pH选择
分别在pH=4.9、5.9、6.5、6.8、7.0、8.0的PBS介质中加入等量的黄嘌呤, 按实验方法进行测定, 结果表明: 在pH=6.8的PBS体系中峰形最好, 且在加入0.1~1.2 mL黄嘌呤时, 峰电流与浓度呈良好的线性关系, 所以最后选择的最佳测试条件为0.05 mol/L PBS(pH=6.8).
2.1.2.3 扫描速率对峰电流的影响
在0.05 mol/L PBS(pH=6.8)+0.2 mol/L KNO3+ 1.0×10-5mol/L Xa体系中, 分别以不同扫描速率进行扫描, 记录循环伏安图(见图2). 实验发现, 在低扫描速率下(≤ 100 mV/s), 氧化峰电流与扫描速率成正比; 在高扫描速率下(≥ 100 mV/s), 氧化峰电流与扫描速率的平方根成正比.
2.1.3 黄嘌呤的浓度与氧化峰电流的关系
在0.05 mol/L PBS(pH=6.8)+0.2 mol/L KNO3中, 用微量进样器精确量取50~1 000mL的黄嘌呤标准溶液于电解池中(总体积为10.0 mL), 按实验方法, 分别记录不同浓度黄嘌呤下的循环伏安图(见图3).

测试体系: 0.05 mol/L PBS(pH=6.8)+0.2 mol/L KNO3+ 1.0×10-5mol/L Xa
扫描速率(由内至外): 10 mV/s, 25 mV/s, 50 mV/s, 75 mV/s, 100 mV/s
扫描电位范围: 0.5~1.2 V
图2 PCALE在低扫描速率下的CV图

Xa浓度: 0.5×10-6mol/L, 1.0×10-5mol/L, 2.0×10-5mol/L, 4.0×10-5mol/L, 6.0×10-5mol/L;
扫描电位: 0~1.2 V; 扫描速率: 100 mV/s;
p=-0.010 5-2.09,= 0.998 9.
图3 PCALE在不同浓度Xa体系中的CV图
2.2 干扰试验
在最佳实验条件下, 当Xa浓度为1.0×10-5mol/L时, 对可能存在的共存物质进行了实验, 结果表明: 至少150倍的甘氨酸、50倍的DL-半胱氨酸、100倍的DL-丝氨酸、200倍的葡萄糖、170倍的乳酸等不干扰Xa的测定. 抗坏血酸和尿酸的电位分别在-0.1 V和0.3 V的位置上, 与Xa的电位相距较远, 因此也不干扰Xa的测定.
2.3 样品分析
2.3.1 尿样中Xa的测定
取新鲜尿样2 mL移至50 mL容量瓶中, 用pH= 5.3的磷酸缓冲溶液稀释至刻度, 摇匀后移取适量于电解池中, 其余步骤同实验方法, 用标准加入法进行定量分析, 分析结果列于表1.

表1 平行样品的测定结果
由表1可知: 样品测定结果的相对标准偏差为1.6%, 完全满足微量分析要求.
2.3.2回收率实验
本试验采用在样品中加入一定量的标准黄嘌呤溶液, 然后利用标准曲线法进行定量分析, 根据测定实验数据计算回收率, 结果列于表2中.
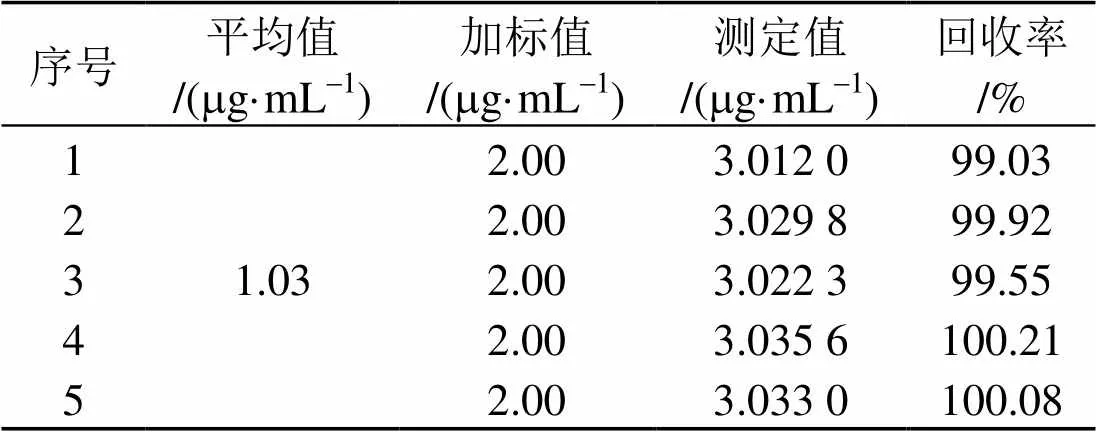
表2 样品回收率实验结果
由表2可知: 回收率在99.03%~100.21%之间.
3 结论
在0.05 mol/L PBS (pH=6.86) +0.2 mol/L KNO3聚合体系中, 利用循环伏安法电聚合制备出性能良好、电活性高, 并对Xa具有良好电催化作用的PCALE. 利用PCALE对Xa的电催化作用, 建立了对黄嘌呤含量进行定量分析的一种电分析方法, 并用于实际尿液样品中Xa的定量检测. 实验结果表明该定量分析方法的检出限较低, 工作曲线线性关系好, 相对标准偏差小, 完全满足微量分析的要求.
[1] 杨秋霞李国宝.刘祥兵等.聚灿烂甲酚蓝修饰电极的制备及电催化作用[J]. 济南大学学报: 自然科学版, 2005, 19(3): 211-214.
[2] 周谷珍. 苯胺掺杂聚茜素红薄膜修饰电极的研制及应用[J]. 湖南文理学院学报: 自然科学版, 2006, 18(2): 28-30.
[3] 孙元喜. 聚茜素红薄膜修饰电极对硫酸庆大霉素的电催化作用[J]. 分析测试技术与仪器, 2005, 11(1): 13-16.
Determination of xanthine using poly(calcein) film modified eletrodes
ZHOU Gu-zhen, TANG Qian-qian, SUN Yuan-xi
(College of Chemistry, Hunan University of Arts and Science, Changde 415000, China)
The preparation method of Poly(Calcein) film modified electrode was studied by the circulation voltammetry in the polymerization system of 0.02 mol/L PBS(pH=6.86)+0.2 mol/L KNO3+ 1.0×10-4mol/L(CAL). Using the electrocatalytic action of PCALE on the xanthine (Xa), the electroanalytic method of determining content of Xa was set up. In 0.02 mol/L PBS(pH=6.8)+0.2 mol/L KNO3, the concentration of Xa had a good linear relations in 5.0×10-6~ 1.0×10-4mol/L with the peak current, detection limit reached 2×10-7mol/L. The linear regress equation wasp=-0.010 5-2.09 and the linear correlation coffcient was 0.998 9. By the quantitative method to the Xa sample, the satisfactory result was obtained. The relative standard deviation of five samples analysis results was less than 2%, it completely satisfies the request of micro analysis.
poly(calcein); modified electrode; xanthine; electrocatalyse
10.3969/j.issn.1672-6146.2011.03.018
O 657.1
1672-6146(2011)03-0065-03
2011-04-12
周谷珍(1956-), 女, 教授, 研究方向为无机化学及电分析化学. E-mail:
(责任编校: 谭长贵)

