腹腔镜右半肝切除术1例报告
徐 钧, 董永红, 张宇红, 董秀山, 李卫斌 (山西省人民医院普外科, 太原 030012)
在微创外科快速发展的今天,腹腔镜在肝脏外科中应用由开始简单的肝囊肿开窗、局部肿物切除等发展到肝叶不规则和规则性切除。但由于肝脏的复杂管道系统和丰富的血供,开腹切肝技术在腹腔镜下难以应用,以及地域间医疗技术水平差异较大,使得腹腔镜肝切除的发展较为缓慢,尤其是腔镜下右半肝切除术的开展。本文就我院腹腔镜下右半肝切除术1例报告如下。
1 病例资料
1.1 一般资料 患者,男性,28岁,身高168 cm,体重104 kg。主因“乙型肝炎14年,发现肝占位7 d余”于2011-04-06入院。患者于14年前患有乙型肝炎,曾给予干扰素、中药等抗病毒治疗1年多,转氨酶正常后无任何治疗。今年因腹部不适行彩超检查,结果提示肝弥漫性疾病改变,肝右叶实质性低回声团伴周围多发小结节,大小约3.8 cm×2.4 cm。增强CT检查(图1)提示:肝右叶后段可见类圆形低密度影,边界尚清,大小约2.4 cm×2.7 cm,增强后,动脉期病灶不均匀强化,静脉期病灶减弱,延迟期病灶密度低于周期肝组织,提示肝右叶后段占位性病变(肝癌征象)。入院检查甲胎蛋白(AFP)正常,查体无明显阳性体征。术前诊断:肝占位、乙型肝炎。经积极的术前准备,在全麻下行腹腔镜右半肝切除术。

图1 术前腹部CT检查
1.2 手术步骤 采用气管插管全身麻醉,患者仰卧、头高脚低,双下肢分开。术者位于患者左侧,一助位于术者对侧,二助扶镜位于两腿之间。脐部穿刺建立气腹,腹内压维持12 mmHg,由此孔插入10 mm套管针,置入腹腔镜探查肝脏及邻近脏器,根据探查情况在腹部置入其他套管针,主操作孔尽可能接近病变部位取剑突下,副操作孔须与主操作孔及镜头保持一定距离,采用右锁骨中线肋缘下。
术中探查见肝脏右前叶近肝缘处有一肿物,镜下观察大小约4 cm×4 cm(图2)。术中行超声检查(图3)示:于肝右叶被膜下可见一实性低回声肿物,约4.5 cm ×3.0 cm,边界尚清,内部回声不均质,可见小片状液性暗区,后方回声稍有增强,肿物内可见粗大穿支动脉血管,另于右肝内还可见多个小的低回声结节,多数分布于肿物周围,少部分结节呈“牛眼样”改变,其中一个大小约6.6 mm ×4.2 mm,位于Ⅴ、Ⅷ段交界近肝正中裂2 cm处。其余肝实质回声粗,分布不均,门脉右支部分小分支腔内未见血流充盈。印象:肝脏回声异常,肝右叶实性占位,肝内多发小结节,门脉右支部分分支管腔栓塞。根据术中彩超结果,决定行腹腔镜下右半肝切除术。首先游离肝右三角韧带、右冠状韧带。仔细解剖第1肝门(图4、5),游离胆囊动脉、胆囊管、胆总管、肝总管,夹闭并切断胆囊动脉和胆囊管;游离并确定肝动脉的左右支,门静脉左右支及右前支和右后支;使用钛夹分别夹闭肝动脉右支、门静脉右前支和右后支,选择性阻断入肝血流,阻断后可清楚看到左右半肝的界限,即预切线。沿肝下下腔静脉向上仔细解剖第3肝门(图6),钛夹夹闭并切断部分肝短静脉。切断肝镰状韧带,肝脏膈面下移,解剖第2肝门(图7),由于患者过于肥胖,未能暴露肝右静脉。最后使用超声刀断离肝组织,肝断面管道用钛夹、Hem-olok夹夹闭,断面使用氩气刀止血并喷洒生物胶。切除肝脏放入标本袋内,于右侧肋下斜切口取出。术后病理报告为:肝细胞肝癌(高分化),周围肝组织脂肪变性显著,间质纤维增生。
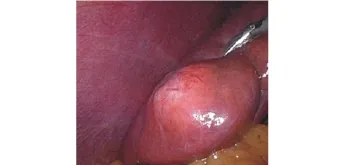
图2 肝脏肿物位于右前叶近肝缘处,呈圆形,大小约4 cm×4 cm
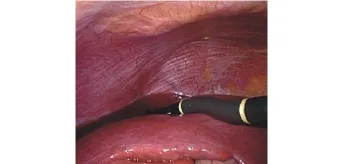
图3 术中腹腔镜下行彩超检查,以进一步明确肿物的大小、肿物和重要管道的毗邻关系、肝脏其他部位的病变
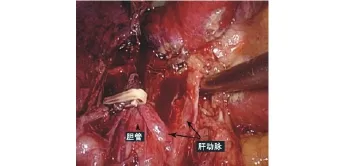
图4 解剖第1肝门正面观,可见胆管和肝动脉及其分支

图5 解剖第1肝门侧面观,自前向后分别为肝动脉右支、胆管、门静脉
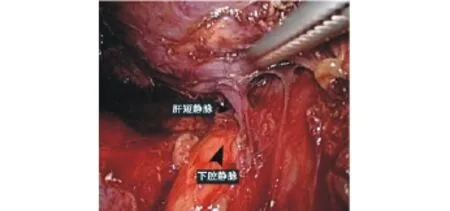
图6 解剖第3肝门,可见肝下下腔静脉和肝短静脉
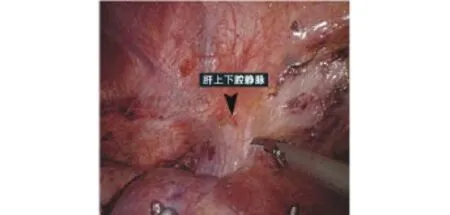
图7 解剖第2肝门,可见肝上下腔静脉
1.3 术后治疗 术后3 d给予甲基强的松龙40 mg,给予保肝治疗(还原性谷胱甘肽,门冬氨酸鸟氨酸,多烯磷脂酰胆碱),以及对症营养支持治疗,患者恢复良好,无胆漏、出血和肝功能衰竭等并发症发生,痊愈出院。
2 讨论
随着腹腔镜技术的提高和经验的积累,腹腔镜肝切除的范围己由肝缘浅表病变的局部切除扩大到半肝的规则性切除。除尾状叶外,只要肿瘤局限于一侧肝叶,肿瘤较小,无门静脉及胆管内癌栓和转移,无其他开腹肝切除术禁忌证者,均可行腹腔镜解剖性肝叶切除术[1]。国内外多中心报告腹腔镜可安全、有效地完成肝切除手术,而且初步的临床经验显示腹腔镜肝切除近期疗效明显优于开腹手术,治疗肿瘤的远期疗效与开腹手术相当[2,3]。
本例患者采用术中腹腔镜下彩超定位肿瘤的位置和边界,有效避免肿瘤的不全切除,同时也明确了肿瘤毗邻肝内血管及胆道的走向和关系,减少镜下出现难以控制大出血的风险。在游离肝脏周围韧带时,先游离右三角韧带和冠状韧带,解剖第1肝门和第3肝门之后再离断镰状韧带,这样镰状韧带可保持向上提拉肝脏,有利于暴露第1肝门和第3肝门。在阻断肝门血流时,采用肝门血流选择性阻断,这样可以彻底阻断预切除肝叶的入肝血流,与常规非选择性肝门阻断相比,可以明显减少肝脏切缘的渗血,并且可以避免残肝的缺血再灌注损伤,减少术后肝功能障碍的发生[4]。腹腔镜下解剖第二肝门难度极大,本例患者由于肥胖和肝脂肪变性,第二肝门区域间隙较小,解剖困难,为了手术安全,未勉强解剖。
虽然,腹腔镜下肝切除存在较多优点,但也存在耗时长、难度高、风险大以及费用高等问题,必须要求术者具有娴熟的腹腔镜外科操作技巧和丰富的肝脏外科经验,且能够将两者有机地结合起来。此外,在临床中选择适当的病例,严格遵守肿瘤的无瘤原则,积极有效预防并发症发生,必要时果断中转开腹,在此前提下,腹腔镜肝切除将能够得到长足的发展。
[1] 蔡秀军,王一帆.腹腔镜解剖性肝切除术[J].肝胆外科杂志,2009,17(1):11 -12.
[2] Chung CD,Lau LL,Ko KL,et al.Laparoscopic liver resection for hepatocellular carcinoma[J].Asian J Surg,2010,33(4):168 -72.
[3] 刘荣,胡明根,赵向前,等.完全腹腔镜肝切除的临床应用价值(附123例经验总结)[J].腹腔镜外科杂志,2006,11(6):479-481.
[4] Skums AV,Vitiuk RV,Lytvyn OI,et al.Laparoscopic resection of the liver[J].Klin Khir,2010,(11 -12):93 - 97.

