虾酱酶法模拟加工过程中的细菌学分析
谢主兰,何晓丽,雷晓凌,王美华
(广东海洋大学食品科技学院,广东 湛江 524088)
虾酱酶法模拟加工过程中的细菌学分析
谢主兰,何晓丽,雷晓凌,王美华
(广东海洋大学食品科技学院,广东 湛江 524088)
对虾酱酶法加工过程中各工序的细菌总数、大肠菌群数、副溶血性弧菌和沙门氏菌进行检验。结果表明:鲜虾原料的细菌总数为3.4×104CFU/g,冰水清洗后明显降低为3.0×103CFU/g,50℃酶解3h后的细菌总数显著增加至3.7×104CFU/g,加入食盐能抑制细菌的生长;采用100℃杀菌30min,能有效杀死虾酱中的细菌,成品虾酱的细菌总数为2.6×104CFU/g。鲜虾原料的大肠菌群数为15MPN/g,冰水清洗后明显降低至3.6MPN/g,酶解作用对大肠菌群的生长影响不大,加盐、保温、杀菌能明显消除大肠菌群的污染,成品虾酱的大肠菌群数小于3.0MPN/g。虾酱加工过程中均未检出副溶血性弧菌和沙门氏菌。由此可见,冰水清洗、加盐、杀菌等工艺条件是虾酱酶法加工过程中控制细菌总数和大肠菌群数的关键工序。
虾酱;酶解;细菌总数;大肠菌群;副溶血性弧菌
虾酱,是我国沿海居民传统的一种发酵型海洋食品。虾酱味道鲜香,且营养丰富,富含蛋白质、多种维生素及矿物质。虾酱中的蛋白质为完全蛋白质,氨基酸种类齐全,比例合适,吸收率高达98%。虾酱中的磷主要以卵磷脂和脑磷脂的活性形式存在,因此被誉为“健康食品”[1-2]。
然而,采用传统发酵法加工的虾酱,发酵时间长,含盐量高达25%~30%[1],不易被微生物污染,耐贮性比较好,但食用品质比较差,大多数情况下只能用作调味品,用量不多,限制了虾酱的食用范围,且高盐量容易导致高血压等心血管疾病,因此,高盐虾酱已不再受消费者的欢迎。考虑到消费者趋向低盐和方便即用的消费需求,酶法加工的低盐虾酱逐渐引起重视,国内外已有大量的研究报道[3-5]。纂翠华等[1]报道过虾酱的酶法制备及其应用,刘树青等[6]利用酶法制备低盐虾酱进行了工艺研究,分析了用酶、温度、盐对虾酱理化品质的影响。酶法加工的低盐虾酱是利用蛋白酶加速蛋白质的分解转化,可以大大缩短发酵时间,明显降低含盐量(18%左右),品质优良,滋味鲜美,扩大了食用范围,备受消费者的青睐,但是盐分含量较低,食盐的抑菌作用减弱,若加工过程不严格控制微生物污染,则产品耐贮性降低,甚至出现微生物超标导致的虾酱卫生安全问题。而目前,对虾酱酶法加工过程中的微生物污染情况的研究尚未见报道。
本实验对虾酱模拟酶法加工过程中的细菌总数、大肠菌群数、副溶血性弧菌和沙门氏菌进行检测,分析从鲜虾原料、冰水清洗、酶解、加盐、保温、杀菌到虾酱成品等各工序中的微生物变化情况,初步探讨加工过程中的关键工序,为进一步建立低盐虾酱制品酶法加工的关键控制点提供参考。
1 材料与方法
1.1 材料与试剂
鲜虾为市售,产地为湛江市东海岛海域。
胰蛋白酶 山东济南亚康力诺有限公司;蔗糖琼脂、胰蛋白胨大豆肉汤、三糖铁琼脂、V-P半固体琼脂、硫代硫酸钠、柠檬酸钠、胆盐、氯化钠、革兰氏染色剂、食盐等。
1.2 仪器与设备
101-3-BS-Ⅱ电热恒温鼓风干燥箱、SPX-250B型生化培养箱 上海跃进医疗器械厂;YS100双目电光生物显微镜 日本尼康公司;SW-CJ-1F洁净工作台、HH-6数显恒温水浴箱、YXQ-SG46-280SA不锈钢手提压力蒸气灭菌器 上海博迅实业有限公司医疗设备厂;SIEMENZ SCD-222电冰箱 安徽博西华制冷有限公司;XK97-A菌落计数器 上海华岩仪器设备有限公司;99K-5多功能混合搅拌器 佛山市顺德区辉马家用电器制造有限公司。
1.3 培养基
月桂基硫酸盐胰蛋白胨培养基(LST)、煌绿乳糖胆盐培养基(BGLB)、EC肉汤培养基、伊红美蓝琼脂培养基(EMB)、四硫磺酸盐煌绿增菌液(TTB)、亚硫酸铋琼脂培养基(BS)、TCBS琼脂培养基(硫代硫酸钠、柠檬酸钠、胆盐、蔗糖)、靛基质实验用培养基、氨基酸实验用培养基 北京陆桥技术有限责任公司。
1.4 方法
1.4.1 样品采集与预处理
实验用鲜虾均在湛江临东市场的一个固定销售点购买,时间为9~11月,每月采样不少于3批次,用保鲜袋装好,采集好的样品统一放入泡沫采样箱于0~6℃冷藏,然后在1h内运至广东海洋大学水产品加工实验室和食品微生物检验技术实验室进行实验,剩余样品采用无菌保鲜袋密封后,放入冰箱0~4℃冷藏,24h内加工。
1.4.2 虾酱酶法制备工艺流程
鲜虾→冰水清洗→沥水→粉碎→50℃酶解3h→过滤→加盐(18%)→保温3d→装瓶→杀菌(100℃,30min)→冷却→成品
1.4.3 样品制备
实验过程采用无菌操作的方法,根据检测目的,准确称取25.0g样品,捣碎后放入225mL无菌生理盐水中,稀释成1:10的样液,再以10倍递增,进一步稀释为1:100、1:1000的稀释液。这些稀释样液用于测定细菌总数、大肠菌群数、沙门氏菌。
另外,在无菌操作下称取样品50g,充分捣碎,放入30g/L NaCl溶液450mL,制成1:10的稀释液,并充分振荡;用1mL灭菌吸管吸取1:10的稀释液1mL,注入装有9mL 30g/L NaCl溶液试管里,制成1:100的稀释液;用同样的方法制成1:1000的稀释液,用于副溶血性弧菌的检测。
1.4.4 指标检测
1.4.4.1 细菌学检验
在虾酱加工的各个工序步骤中,分别检验细菌总数、大肠菌群数、沙门氏菌、副溶血性弧菌。细菌总数采用国家标准GB/T 4789.2—2008《食品卫生微生物学检验:菌落总数测定》中的平板菌落计数法检测;大肠菌群数采用GB/T 4789.3—2008《食品卫生微生物学检验:大肠菌群计数》中的MPN计数法检测[7];副溶血性弧菌检测采用SN 0173—92《出口食品副溶血性弧菌检验方法》[8];沙门氏菌采用SN 0170—92《出口食品沙门氏菌属(包括亚利桑那菌)检验方法》检测[9]。
1.4.4.2 加工过程中的细菌学分析
称取150.0g的鲜虾,用冰水反复清洗,沥干粉碎后,加入0.4g/100mL胰蛋白酶,在50℃恒温水浴锅中酶解3h,按质量分数18%的比例加入食盐,保温3d,在100℃条件下杀菌30min。检测虾酱制备过程中各工序及成品虾酱中的细菌总数、大肠菌群数、沙门氏菌及副溶血性弧菌。各做3次平行实验,取其平均值。
2 结果与分析
2.1 不同采样月份鲜虾细菌总数变化情况
对在9~11月份的鲜虾未加工样品细菌总数进行了检测,结果显示细菌总数在9月份最高,达到3.4×104CFU/g,11月份最低为2.5×104CFU/g。
2.2 虾酱加工各工序的细菌学变化
由表1可知,虾酱加工过程中的各工序细菌总数变化波动。鲜虾原料的细菌总数为3.4×104CFU/g。冰水清洗后,细菌总数明显降低至3.0×103CFU/g,这说明冰水有抑制细菌生长繁殖的作用。建议在实际生产中,采用无污染的冰水对原料进行清洗。清洗后的虾进行沥水、粉碎,再加胰蛋白酶在50℃水解3h后,浆液的细菌总数增加至3.7×104CFU/g,与冰水清洗相比明显增多,这可能是因为浆液中含有的耐热菌数较多,在酶解过程中大量繁殖,酶解有利于耐热菌的生长繁殖。因此,在加工过程中应严格控制酶解温度与时间,既能让蛋白质充分水解,又能控制细菌的快速生长,确保虾酱的卫生安全。加盐、保温3d后,细菌总数降低为3.2×104CFU/g,即食盐有抑制细菌生长的作用。杀菌对虾酱的细菌总数影响很大,与鲜虾原料比,虾酱的细菌总数明显降低为2.6×104CFU/g,符合水产行业标准规定的细菌总数≤4×104CFU/g[10]。这说明采用100℃杀菌30min,能有效杀死虾酱中的细菌。
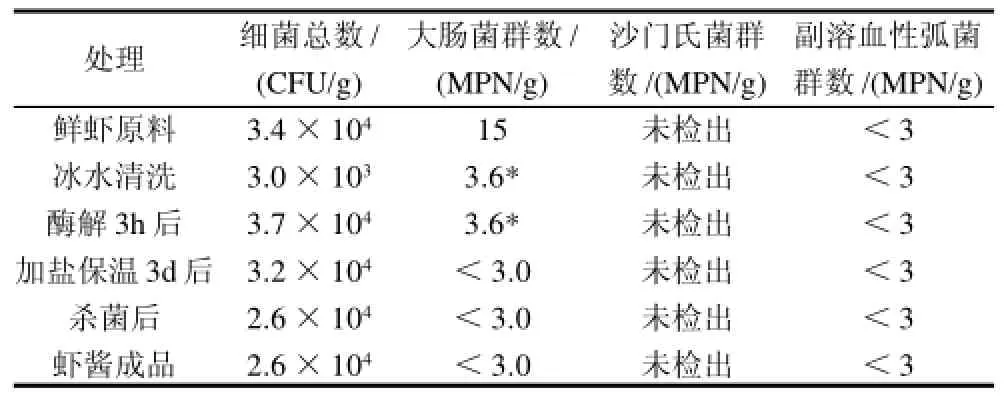
表1 虾酱加工过程中的细菌学检测结果Table 1 Bacterial test results during the processing of shrimp sauce
从表1可见,鲜虾原料的大肠菌群数为15MPN/g,冰水清洗后,大肠菌群数明显降低至3.6MPN/g,与鲜虾原料相比差异显著(P<0.05),但不符合食品卫生国内标准规定的大肠菌群数和相关国际标准的规定(大肠菌群数≤30MPN/100g)[10-12]。原料沥水、粉碎、加胰蛋白酶在50℃水解3h后,虾浆液的大肠菌群数为3.6MPN/g,与鲜虾原料相比差异明显,但与冰水清洗后的虾相比没有差异,即酶解温度与时间对大肠菌群的生长影响不大。加盐、保温3d、杀菌后,虾浆液中的大肠菌群数的检验结果均小于3MPN/g,即大肠菌群阴性。符合食品卫生国内标准和相关国际标准的规定[10-12]。
副溶血性弧菌(Vibrio parahaemolyticus)是沿海国家和地区的导致食物中毒的重要病原菌,在我国部分沿海地区,细菌性食物中毒中副溶血性弧菌食物中毒占首位[13]。副溶血性弧菌是一种耐盐性细菌,是导致海产品肠道传染病的主要致病菌,该菌是在夏秋季容易引起感染人群的食物中毒[14-15]。因此,对鲜虾原料及虾酱中副溶血性弧菌的检测很有必要。由表1可知,鲜虾原料、冰水清洗、沥水、粉碎、酶解、加盐、保温、杀菌等虾酱加工过程中,各个工序的副溶血性弧菌的检验结果均小于3MPN/g,符合食品卫生国内标准和相关国际标准规定(副溶血性弧菌群数<3MPN/g)[10-12]。虾酱酶解加工过程中均未检出沙门氏菌。
3 结 论
3.1 通过对虾酱酶法模拟加工过程中各工序的细菌学分析,结果显示加工过程中的细菌总数受清洗用水、酶解及杀菌等工序的影响。杀菌工艺条件直接影响虾酱的风味品质与细菌学品质。因此,冰水清洗和杀菌是控制虾酱中细菌总数变化的关键工序。
3.2 鲜虾原料大肠菌群数明显超标,不符合相关国内与国际标准的规定,这说明湛江近海养殖水质污染严重。在实际生产中,必须对近海水质加强监控,减少污染源,以确保海产品卫生质量与安全性。加工过程中,加入一定量的食盐及杀菌工艺是消除大肠菌群的重要环节,也是避免肠道致病菌危害卫生健康的关键工艺。
3.3 虾酱酶解加工过程中及成品虾酱,都未检出副溶血性弧菌和沙门氏菌,因此,符合致病菌不得检出的要求。
[1] 纂翠华, 张伟, 王元秀, 等. 虾酱的酶法制备及其应用[J]. 食品工业, 2007(4): 19-20.
[2] 杜云建, 赵玉巧, 马晨艳. 虾酱的研究[J]. 中国调味品, 2009, 34(8): 81-84.
[3] HEU M S, KIM J S, SHAHIDI F, et al. Characteristics of protease from shrimp processing discards[J]. Journal of Food Biochemistry, 2003, 27 (3): 221-236.
[4] CAKLI S, KILINC B, CADUN A, et al. Effects of using slurry ice on the microbiological, chemical and sensory assessments of aquacultured sea bass (Dicentrarchus labrax) stored at 4 ℃[J]. Eur Food Res Technol, 2006, 222(1/2): 130-138.
[5] CHAWLA S P, CHANDER R. Microbiological safety of shelf-stable meatproducts prepared by employing hurdle technology[J]. Food Control, 2004, 15(7): 559-563.
[6] 刘树青, 林洪. 酶法制备低盐虾酱的研究[J]. 海洋科学, 2003, 27(3): 57-60.
[7] GB/T 4789—2008 食品卫生微生物学检验国家标准[S].
[8] SN 0173—92 出口食品中副溶血性弧菌检验方法[S].
[9] SN 0170—92 出口食品中沙门氏菌检验方法[S].
[10] SC/T 3602—2002 中华人民共和国水产行业标准 虾酱[S].
[11] 吕志平. 国内外技术法规和标准中食品微生物限量[M]. 北京: 中国标准出版社, 2002.
[12] 罗雪云, 刘宏道. 食品卫生微生物检验标准手册[M]. 北京: 中国标准出版社, 1995.
[13] 张宏伟, 付建荣. 弧菌科细菌致急性腹泻的流行病学调查[J]. 中华医学检验杂志, 1996, 19(1): 45.
[14] SU Yicheng, LIU Chengchu. Vibrio parahaemolyticus: a concern of seafood safety[J]. Food Microbiol, 2007, 24(6): 549-558.
[15] SERICHANTALERGS O, BHUIYAN N A, NAIR G B, et al. The dominance of pandemic serovars of Vibrio parahaemolyticus in expatriates and sporadic cases of diarrhoea in Thailand, and a new emergent serovar(O3:K46)with pandemic traits[J]. J Med Microbiol, 2007, 56(5): 608-613.
Bacteriological Analysis in Mimic Enzymatic Processing of Shrimp Sauce
XIE Zhu-lan,HE Xiao-li,LEI Xiao-ling,WANG Mei-hua
(College of Food Science and Technology, Guangdong Ocean University, Zhanjiang 524088, China)
Total viable bacteria, coliforms, Vibrio parahaemolyticus and Salmonella were counted at various stages of enzymatic processing of shrimp sauce. The results indicated that the total bacterial count in fresh shrimps was 3.4×104CFU/g, and a lower value of 3.0 × 103CFU/g was observed after washing with ice water. However, the number of total bacteria in shrimps after enzymatic hydrolysis at 50 ℃ for 3 h was increased to 3.7 × 104CFU/g. Salt addition could obviously inhibit bacterial growth. Sterilization at 100 ℃ for 30 min could effectively kill bacteria in shrimp sauce and the sterilized shrimp sauce showed a total bacterial count of 2.6 × 104CFU/g. Washing with ice water could cause the coliform count in fresh shrimps to obviously decline from 15 to 3.6 MPN/g. However, enzymatic hydrolysis did not affect coliform count. Salt addition, constant temperature and sterilization could significantly decrease the pollution from coliforms and coliforms in shrimp sauce products were counted to be less than 3.0 MPN/g. Neither Vibrio parahaemolyticus nor Salmonella were detected during the processing of shrimp sauce. Therefore, ice water washing, salt addition and sterilization are critical for the control of total bacteria and coliform counts.
shrimp sauce;enzymatic hydrolysis;total bacteria;coliform;Vibrio parahaemolyticus
TS254.9;R155.1
A
1002-6630(2011)07-0279-03
2010-08-15
广东海洋大学自然科学基金项目(1012120)
谢主兰(1966—),女,副教授,硕士,主要从事食品微生物与水产品质量安全研究。E-mail:xiezhulan66@163.com

