吡格列酮对糖耐量异常患者的干预作用
徐寒松 雷闽湘 孔德明 向 慧 谢晓云 (贵阳中医学院第二附属医院内分泌科,贵州 贵阳 550003)
糖耐量异常(IGT)属于糖尿病前期,如不加干预,约 60%以上的患者 5年后会发展为糖尿病。老年IGT者患高血压、缺血性心脏病、动脉粥样硬化的危险性是正常糖耐量人群的1.5~2倍,早期发现和诊断 IGT患者,并对其进行干预治疗,已成为糖尿病一级和二级预防,减少微血管和大血管并发症的一个重要环节,由于生活方式干预在具体实践中有一定困难,因此药物干预成为有效干预手段。本研究采用吡格列酮干预老年 IGT患者,并进行临床效果观察。
1 对象与方法
1.1 研究对象 选择在中南大学湘雅医院和贵阳中医学院第二附属医院内分泌门诊或体检时发现FPG在6.1~7.0 mmol/L之间,强化生活方式干预 1个月后,OGTT(采用 75 g无水葡萄糖负荷)检查 2h PG仍在 7.8~11.1 mmol/L之间的患者。排除继发性血糖升高;严重的微血管并发症,严重的心、肝、肾疾病,其他严重器质性疾病。共 119例患者入选,经签署知情同意书后进入干预治疗,男 61例,女 58例,年龄 47~76岁,平均(66.4±8.5)岁,平均病程(5.36±3.54)年。根据随机原则分为吡格列酮组(60例)和安慰剂对照组(59例)。吡格列酮组与对照组性别构成、平均年龄、体重指数、腰臀比、总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)、空腹血糖(FPG)、葡萄糖耐量试验(OGTT)后 2 h血糖(2 h PG)、空腹胰岛素(FINS)、OGTT后 2 h胰岛素(PINS)、胰岛素敏感指数(ISI)、胰岛素抵抗指数(Homa-IR)均相匹配。两组指标均具有可比性(P>0.05)。
1.2 方法
1.2.1 治疗方法 两组入选对象在强化生活方式干预的基础上,吡格列酮组给予盐酸吡格列酮片(卡司平,杭州中美华东制药有限公司生产,批号 20050500,每片 15 mg),每日早餐前30 min服用 30mg,对照组给予安慰剂,每日早餐前 30 min服用2片,疗程均为 1年。盐酸吡格列酮片与安慰剂片均由杭州中美华东制药有限公司提供,按随机双盲双模拟分装,安慰剂外观、大小、颜色、气味、包装与盐酸吡格列酮片一致。
1.2.2 观察指标和方法 用药前及用药后 12、24、48 w各随访 1次,观察临床表现及有无不良反应,测定空腹及 75 g无水葡萄糖负荷后 2 h PG、PINS、血脂等指标。FPG用葡萄糖氧化酶法测定,FINS用放免法测定(试剂盒为天津德普生物技术有限公司生产)。稳态模型(Homa模型)的 Homa-IR=(FPG×FINS)/22.5,ISI=1/(FINS×FPG)。
2 结 果
2.1 两组治疗前后各项指标变化比较 两组老年 IGT人群初访时体重指数、腰臀比、血压与治疗前差异均无统计学意义(P>0.05)。吡格列酮组 FPG、2hPG、FINS、PINS、Homa-IR均较治疗前显著下降,ISI升高(P<0.05,P<0.01);对照组 FPG较治疗前下降(P<0.05),2 h PG、Homa-IR、ISI、FINS、PINS水平均无改变(P>0.05);见表 1。
2.2 糖尿病发病率比较 两组老年IGT人群 48 w后随访,安慰剂组糖耐量转为正常者 25例(42.4%),仍为 IGT者 29例(49.2%),转为糖尿病者 5例(8.5%);吡格列酮组糖耐量转为正常者 50例(83.3%),仍为 IGT者 8例(13.3%),转为糖尿病者 2例(3.3%)。
表1 两组治疗前后各项指标的变化(±s)
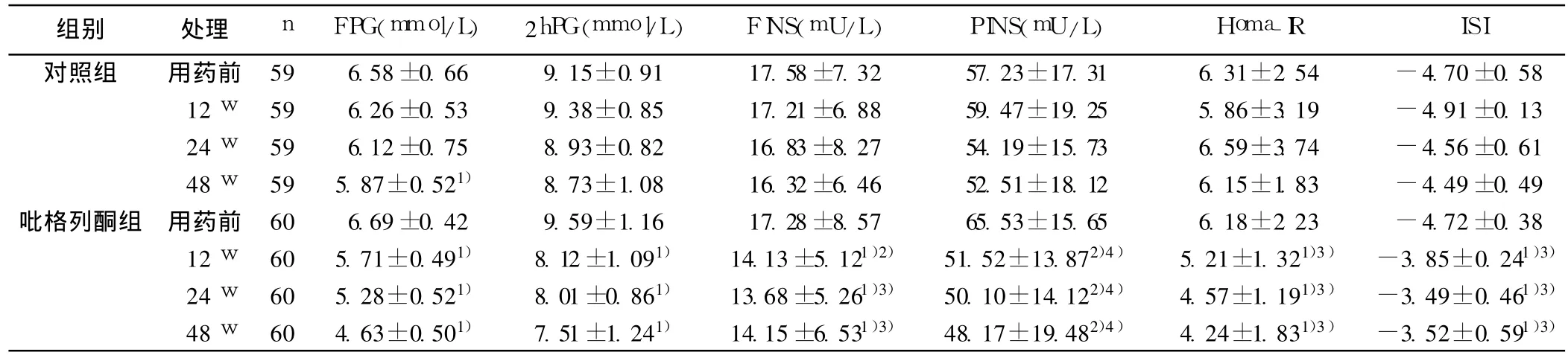
表1 两组治疗前后各项指标的变化(±s)
与同组治疗前比较:1)P<0.05,2)P<0.01;在同一治疗时间与对照组比较:3)P<0.05,4)P<0.01;下表同
组别 处理 n FPG(mmol/L)2hPG(mmol/L) FINS(mU/L) PINS(mU/L) Homa-IR ISI对照组 用药前 59 6.58±0.66 9.15±0.91 17.58±7.32 57.23±17.31 6.31±2.54 -4.70±0.58 12 w 59 6.26±0.53 9.38±0.85 17.21±6.88 59.47±19.25 5.86±3.19 -4.91±0.13 24 w 59 6.12±0.75 8.93±0.82 16.83±8.27 54.19±15.73 6.59±3.74 -4.56±0.61 48 w 59 5.87±0.521) 8.73±1.08 16.32±6.46 52.51±18.12 6.15±1.83 -4.49±0.49吡格列酮组 用药前 60 6.69±0.42 9.59±1.16 17.28±8.57 65.53±15.65 6.18±2.23 -4.72±0.38 12 w 60 5.71±0.491) 8.12±1.091) 14.13±5.121)2) 51.52±13.872)4) 5.21±1.321)3) -3.85±0.241)3)24 w 60 5.28±0.521) 8.01±0.861) 13.68±5.261)3) 50.10±14.122)4) 4.57±1.191)3) -3.49±0.461)3)48 w 60 4.63±0.501) 7.51±1.241) 14.15±6.531)3) 48.17±19.482)4) 4.24±1.831)3) -3.52±0.591)3)
2.3 初访时及干预治疗 48 w末血脂的变化 吡格列酮组与治疗前及对照组治疗后比较,TG明显下降,HDL升高(P<0.05),而 TC及 LDL水平无明显变化(P>0.05);对照组血脂水平均无改变(P>0.05),见表 2。
表2 两组患者血脂的变化(±s)
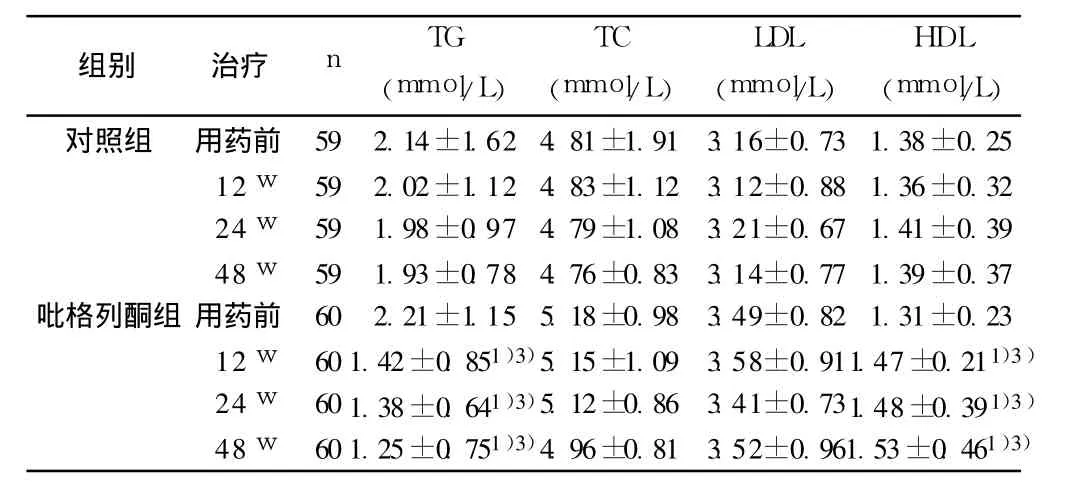
表2 两组患者血脂的变化(±s)
对照组 用药前 59 2.14±1.62 4.81±1.91 3.16±0.73 1.38±0.25 12 w 59 2.02±1.12 4.83±1.12 3.12±0.88 1.36±0.32 24 w 59 1.98±0.97 4.79±1.08 3.21±0.67 1.41±0.39 48 w 59 1.93±0.78 4.76±0.83 3.14±0.77 1.39±0.37吡格列酮组 用药前 60 2.21±1.15 5.18±0.98 3.49±0.82 1.31±0.23 12 w 60 1.42±0.851)3)5.15±1.09 3.58±0.911.47±0.211)3)24 w 60 1.38±0.641)3)5.12±0.86 3.41±0.731.48±0.391)3)48 w 60 1.25±0.751)3)4.96±0.81 3.52±0.961.53±0.461)3)
3 讨 论
IGT的危害不仅表现在可转变成糖尿病,而且表现在 IGT人群较糖耐量正常者有发生心血管疾病的更高危险性,尤其是老年患者,在IGT阶段就可能发生血管病变。因此对老年 IGT患者应积极进行干预,有效的治疗可延缓或防止冠心病及其他大血管病变的发生、发展,在 IGT阶段即进行干预是最合理的糖尿病防治措施。目前针对 IGT的干预措施主要有行为干预和药物干预两大类。美国的理想膳食模式(DDP)研究证实,强化生活方式干预可降低 IGT人群发生糖尿病相对风险 58%,并且具有简便、经济的特点,然而对于老年IGT人群来说,改变长期形成的生活方式并非易事,长期坚持更为困难,而且对于 IR较严重的老年 IGT人群,生活方式干预效果并不理想,因此药物干预是最重要与最主要的干预方式。吡格列酮属噻唑烷二酮类,是过氧化物酶增殖物激活受体γ(PPAR-γ)的高度选择性及强力的激动剂〔1〕,PPAR-γ属于激素核受体超家族,为调控基因转录的因子。人类的 PPAR-γ在胰岛素作用的关键靶组织如脂肪、肌肉、肝脏中表达。PPAR-γ被激活后调控与胰岛素效应有关的多种基因的转录,这些基因的功能涉及葡萄糖的产生、转运、利用以及脂肪代谢的调节。吡格列酮通过与PPAR-γ结合并使之活化,可以改善胰岛素的外周效应,增加外周组织对糖的摄取,降低血糖并改善脂质代谢紊乱,同时不刺激胰岛 B细胞分泌胰岛素,而是增加胰岛素敏感性,减少IR。最近还有研究〔2〕显示吡格列酮可以减轻氧化应激导致的脂肪细胞IR,改善胰岛素信号传导。有研究提示,老年 2型糖尿病患者在诊断时就有 50%合并并发症,提示糖尿病的治疗和干预应当更加积极,开展更早。本研究采用吡格列酮对 IGT的干预作用进行观察,结果显示,在饮食控制和运动的基础上使用吡格列酮,在体重没有任何改变的情况下,1年后观察到吡格列酮组FPG、INS水平及IR明显下降,INS敏感性增加,与对照组比较差异显著。严重的脂质代谢异常是 IR和糖尿病发生发展的主要因素,本研究对血脂影响进行观察,结果显示吡格列酮能降低TG,提高HDL,明显改善IGT患者的脂质代谢,此结果与国内外近期报道一致〔3,4〕,提示 TG可能是脂代谢异常引起 IR发生发展的主要因素;1年后随访对糖尿病发病率进行比较,安慰剂组转为糖尿病者 5例(8.5%);吡格列酮组转为糖尿病者 2例(3.3%)。两组糖尿病发病率均明显低于大庆研究中 IGT人群平均每年15.7%的糖尿病自然转归率〔5〕。提示强化生活方式干预及药物干预均能明显降低IGT患者糖尿病发病率,而两者配合能达到最佳干预效果。
近年来有很多有关该类药物安全性的报道,包括肝脏毒性,体重增加和水潴留。本研究结果显示,使用吡格列酮干预治疗 1年中,生命体征、实验室检查指标均未见有临床意义的变化,提示吡格列酮治疗安全性较好,但远期疗效、安全性等尚需进一步观察证实。
1 Chilcott J,Tappenden P,Jones ML,et al.A systematic review of the clinical effectivenessof pioglitazonein the treatment of type 2diabetesmellitus〔J〕.Clin Ther,2001;23(11):1792-823.
2 曾天舒,潘世秀,陈璐璐 .吡格列酮改善氧化应激导致的脂肪细胞胰岛素抵抗〔J〕.中国医院药学杂志,2007;27(11):1541-4.
3 Goldberg RB,Kendall DM,Deeg MA,et al.A comparison of lipid and glycemic effects of pioglitazone and rosiglitazone in patientswith type 2 diabetes and dyslipidemia〔J〕.Diabetes Care,2005;28(7):1547-54.
4 吴 坚,邹大进,吴文君 .国产吡格列酮对 2型糖尿病患者的疗效及安全性研究〔J〕.中国新药杂志,2002;11(5):399-400.
5 胡英华,李光伟,潘孝仁,等 .大庆糖尿病发病率调查及 21世纪我国糖尿病发病情况的预测〔J〕.中华内科杂志,1993;32(3):173-5.

