纳米四氧化三铁/离子载体修饰电极检测海水中痕量重金属铅
娄婷婷,潘大为,王元娥,宋德安,蒋 琳,秦 伟
(1.中国科学院 烟台海岸带研究所,中国科学院 山东省海岸带环境过程重点实验室,山东 烟台,264003;2.中国科学院 海洋研究所,山东 青岛,266071;3.中国科学院 研究生院,北京,100049;4.湖南大学 化学生物传感与计量学国家重点实验室,湖南 长沙,410082)
随着人类社会工业化的发展,重金属对海洋环境所造成的污染越来越严重。海水中生活的鱼类、贝类等海洋生物由于对重金属离子有富集累积作用,其体内重金属含量严重超标,这不仅会造成海洋渔业的巨大损失,还会危及人类健康,日本著名的水俣病和骨痛病就是典型的例子。因此,检测海水中特别是河口海岸带水体中重金属离子含量是非常必要的。
铅是一种高毒性重金属,可在生物体中蓄积,它对水生生物的安全浓度为0.16 mmol/L (0.7 μg/L)[1],超过此浓度水生生物将面临严重威胁。目前常用的铅离子检测方法有原子吸收光谱法(AAS)、原子发射光谱法(AES)、电感耦合等离子体-质谱联用法(ICP-MS)等,但是这些方法由于仪器昂贵笨重、操作复杂、携带不方便,因此仅适用于实验室分析。电化学溶出伏安法具有仪器装置简单、易于实现自动化、灵敏度高、适合现场监测等优点受到人们的关注[2-3],并已成功用于海水中多种重金属元素的快速测定;但是溶出伏安法选择性较差,海水中共存重金属离子常常干扰测定。
本文提出了一种新型纳米复合材料化学修饰电极,显著提高了溶出伏安法检测海水中铅离子的灵敏度和选择性。该复合材料包括纳米四氧化三铁(nano-Fe3O4)、离子载体(ionophore)以及导电聚合物Nafion等三种成分。纳米四氧化三铁粒径小、表面积大[4-6],能够使复合材料形成多孔结构,从而增强电极对铅离子的富集能力,提高检测的灵敏度。离子载体被广泛应用于电位型离子选择性电极领域,但是由于其导电性差,在伏安分析法中鲜有应用;离子载体含有仅供特定离子通过的空穴或者结合的位点,能够显著提高对特定离子检测的选择性[7-8]。Nafion是一种全氟磺酸树脂,具有良好的热稳定性和化学稳定性、阻抗小、水溶性小[9];作为一种导电载体修饰到电极上,它能够使纳米材料和离子载体更紧密的附着在电极的表面,同时提供阴离子位点,实现重金属阳离子萃取[10-12]。本文制备了纳米四氧化三铁/Nafion/铅离子载体修饰的玻碳电极,采用微分脉冲伏安法成功实现了海水中铅离子高灵敏、高选择性测定。
1 实验
1.1 试剂与仪器
硝酸铅、硝酸镉、硝酸铜、硝酸汞购于国药集团试剂有限公司(上海);N,N-二甲基酰胺(DMF)(高效液相色谱纯)购于天津科密欧公司;Nafion (质量分数5%,乙醇与水混合液)、氢氧化钠、冰醋酸、铅离子载体(Ⅳ)购于Sigma-Aldrich。所用试剂纯度为分析纯或者优级纯。所用纯水均由Pall Cascada实验室水系统制备。
CHI 660C电化学工作站购自上海辰华仪器公司;采用标准三电极体系:玻碳电极为工作电极(直径3 mm),铂电极为对电极,饱和甘汞电极为参比电极。所测电势均相对于参比电极。采用 JEOL JSM.6700 F场发射扫描电子显微镜(SEM)拍摄纳米粒子及电极表面形貌。
1.2 四氧化三铁的合成和修饰溶液的配制
将氯化铁、硫酸亚铁以摩尔比2 :3的比例混合加入到200 mL二次去离子水中溶解搅拌均匀,然后加入三颈烧瓶中,温度控制在 30 ℃左右。在通 N2情况下,加入15.6 mL质量分数为25%~28%的浓氨水,剧烈搅拌,并保持水温恒定,反应 30 min后结束。在外加磁场的作用下,用水洗涤至中性,倾去上层清液。所得沉淀物经 60℃恒温真空干燥,得到纳米四氧化三铁,经研钵研磨成粉末状保存在干燥器中备用。
取纳米Fe3O4粉末10 mg加入5 mL含有0.5%Nafion(质量分数 5 %)与 5 mmol铅离子载体(Ⅳ)的溶液(DMF为溶剂)中,超声 30 min以上,使其分散均匀,得到所需的修饰电极溶液。用同样的方法配制平行试验的电极修饰溶液,但不含有纳米Fe3O4和铅(Ⅳ)离子载体。
1.3 修饰电极的制备
首先在抛光布上分别用0.3、0.05 μm Al2O3粉末将玻碳电极(有效直径 3 mm)仔细打磨干净;冲洗干净后,置于超声波清洗器中震荡1 min,再用乙醇和纯水分别冲洗;最后在0.5 mol/L 的H2SO4溶液中用循环伏安法从-0.15 V扫描至1.3 V直到得到稳定的曲线。用超纯水将电极冲洗后,电吹风吹干;滴5 μL Fe3O4/ionophore的修饰液,并置于红外灯下烘烤;至有机溶剂挥发完毕后,再冷却至室温即得需要的修饰电极。此时,可以看出电极表面形成一层致密的膜。作为对比实验,分别取5 μL 0.5% Nafion溶液和5 μL 2 mg/mL Fe3O4、0.5% Nafion 溶液滴到玻碳电极制成修饰电极。
1.4 实验方法
将修饰后的电极浸入到含有一定标准浓度的Pb2+的 0.1 mol/L 醋酸/醋酸钠缓冲溶液(pH 4.5 )中,在搅拌的条件下富集 10 min。然后以修饰电极作为工作电极,铂电极、饱和甘汞电极分别作为对电极和参比电极,在通氮除氧10 min的醋酸/醋酸钠缓冲溶液(pH 4.5)中进行实验。首先施加-1.1 V的负电位30 s进行预电解,使吸附在电极表面的Pb2+还原为Pb0。静置2 s后,用微分脉冲伏安法以电位增量为5 mV、振幅0.05 V、脉冲宽度为0.01 s、脉冲周期为0.2 s 从-0.9 V正向扫描至到-0.5 V,记录阳极溶出曲线,得到Pb的氧化峰。该过程结束后,将电位保持在+0.0 V处30 s,除去电极表面未被氧化的铅。
2 结果与讨论
2.1 富集与溶出机理探讨
在开路电位下,修饰电极在 Pb2+溶液中富集,Pb2+吸附到电极表面的修饰膜中。施加-1.1 V电压预电解时,膜中的 Pb2+还原为 Pb0,沉积在修饰电极中。在从-0.9 V到-0.5 V的扫描过程中,Pb0被氧化成Pb2+而溶出。机理大致如下:

2.2 纳米四氧化三铁及Nano- Fe3O4/ionophore修饰后电极的表征

图1 所合成的纳米Fe3O4的扫描电镜图Fig.1 SEM image of nano- Fe3O4
图1为用化学共沉淀法所合成的四氧化三铁的扫描电镜照片,从图中可以看出该四氧化三铁颗粒直径在 30~40 nm,且比较均匀。纳米复合材料滴涂在电极表面则形成一层致密的膜覆盖在电极表面,如图2所示。由于纳米颗粒附着在电极表面,因而增大了电极的比表面积,更有利于铅离子的吸附。

图2 纳米Fe3O4/Nafion/ionophore修饰在电极表面SEM形貌图Fig.2 SEM image of the Nano-Fe3O4/Nafion/ionophore film on the modified electrode
2.3 条件选择
Fe3O4浓度、离子载体浓度、Nafion浓度和富集时间都会对电流响应信号产生显著的影响,本实验对各因素进行了条件优化,如图3所示。修饰液中四氧化三铁的浓度过高,会使背景电流过大,而浓度过低,则会降低吸附能力,因此本实验中浓度选择在 2 g/L。离子载体是不导电的高聚物,浓度过高会使电极表面的导电能力降低,背景电流增加;浓度过低,离子载体不能很好地发挥其特定选择性。实验表明,离子载体的浓度在 1 mmol/L时,铅离子的阳极溶出峰电流信号最大。Nafion的质量分数从0.1 %变化到0.5 %过程中,随着质量分数的增加,离子交换作用增加,电流值逐渐增加,在 0.5 %时到达最大。Nafion的质量分数继续增加,膜厚度随之增加,离子传递过程受阻,使离子难以到达电极表面,电流值有所下降。因而Nafion的质量分数选取0.5%。由于纳米材料的吸附能力随着时间的延长逐渐增加,直至达到饱和,实验表明 10 min后,峰电流增长缓慢。本实验选取富集时间为10 min。此外,滴到电极表面的溶液太少会使电极表面修饰不均匀,量太多,则使膜的厚度增加,导电能力下降,所以本实验选择 5 μL。
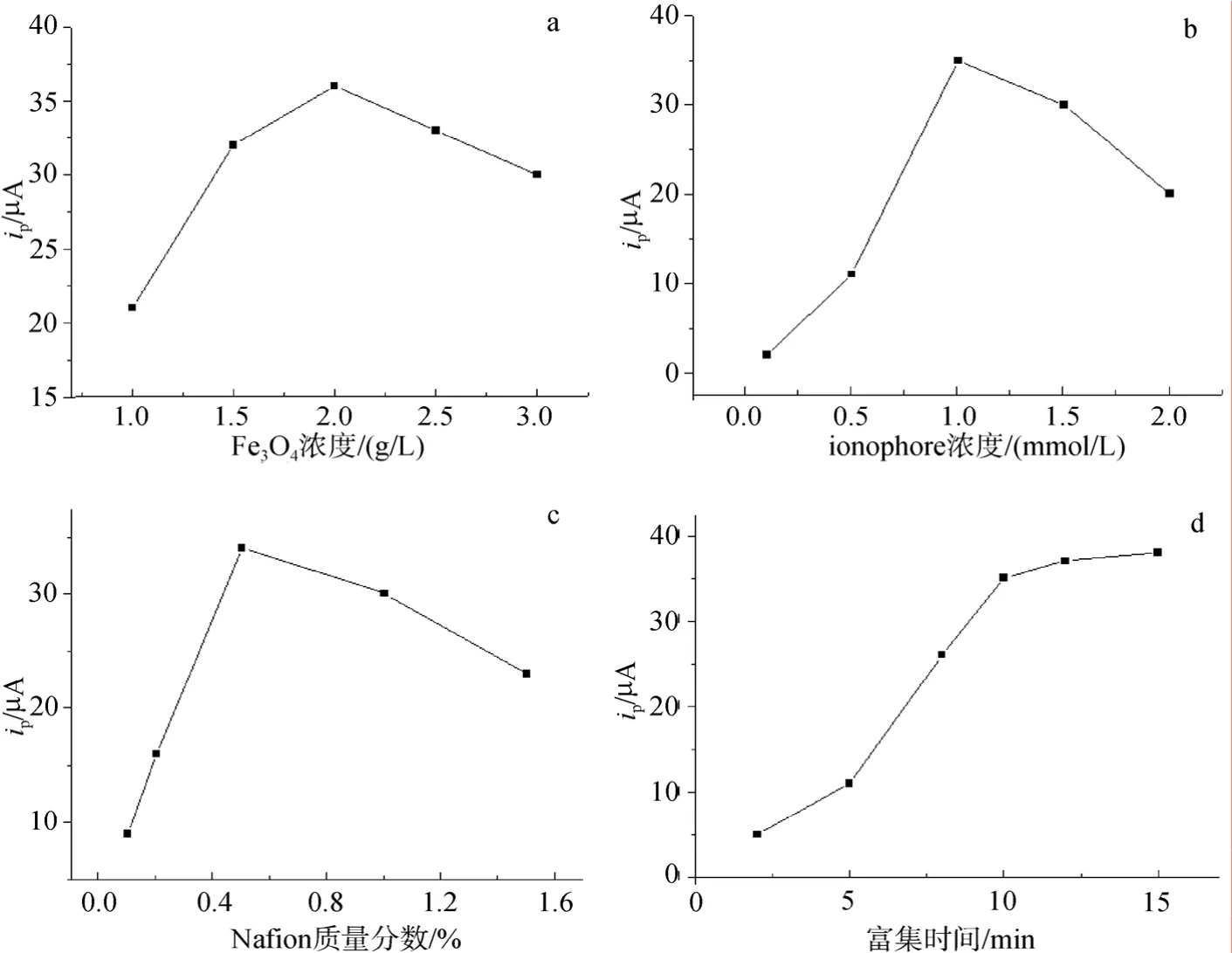
图3 Fe3O4浓度(a)、离子载体浓度(b)、Nafion浓度(c)和富集时间(d)对电流响应信号的影响Fig.3 Effect of Fe3O4 concentration (a),ionophore concentration (b),Nafion concentration (c) or deposition time (d) on the peak current
2.4 不同修饰电极电化学行为
为了更好地说明修饰电极的吸附能力,裸电极、Nafion修饰电极、Nano-Fe3O4/Nafion修饰电极、Nano-Fe3O4/Nafion/ionophore修饰电极,分别富集10 min Pb2+后,在-1.1V沉积后,用微分脉冲伏安法正向扫描得到不同的Pb2+氧化峰,如图4中所示。从图中可以看出,Nano-Fe3O4/Nafion/ionophore修饰电极产生的电流信号最大,Nano-Fe3O4/Nafion次之,Nafion修饰的电极也产生信号,是因为 Nafion本身为阳离子交换剂,可以交换溶液中的 Pb2+,因而会对Pb2+有所响应。Nano-Fe3O4/Nafion/ionophore修饰电极的峰电流信号与其他电极相比大大提高,这是因为纳米Fe3O4颗粒的超细颗粒结构,使得其比表面积增大,吸附重金属离子能力增强,因而在电极上产生较大的电流信号,提高了检测重金属离子的灵敏度。图中 Nano-Fe3O4/Nafion/ionophore修饰电极的铅的氧化峰D峰相对C峰的位置有所不同,偏向正电位,这可能是由于修饰电极膜中加入了ionophore后,ionophore和铅离子的特异性结合,使铅的溶出峰位置发生改变。
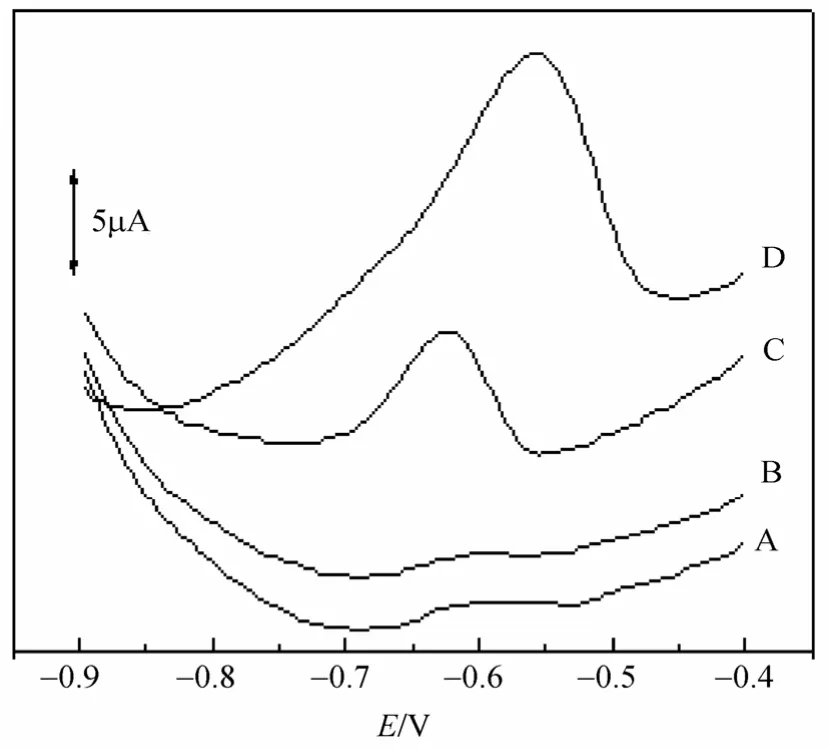
图4 不同修饰电极在10 nmol/L Pb2+溶液中的微分脉冲伏安图Fig.4 Differential pulse voltammograms of different electrodes in the solution of 10 nM lead ion.
2.5 标准曲线
将制备好的 Nano-Fe3O4/Nafion/ionophore修饰电极浸入到一系列Pb2+标准溶液中,富集10 min后,用微分脉冲伏安法进行扫描测定得到一系列氧化峰,然后把峰高对浓度绘制成ip-C图如图5。其线性回归方程为:ip=0.82C+ 1.61,相关系数为:R= 0.987。本方法对铅离子的最低检出限用C=3σ/S求出,其中,C表示最低检出限的浓度,σ为空白信号的相对标准偏差(σ=2.7×10-7),S为线性曲线的斜率(S=0.82 μA L/nmol),经计算最低检出限C为1.0×10-9mol/L。

图5 铅离子浓度从3~60 nmol/L的溶出伏安图Fig.5 Stripping voltammegrams of Pb ions from 3 to 60 nmol/L
2.6 共存离子的干扰实验
铅离子的溶出分析中容易受到其他重金属离子的干扰。而对于其他海水中的常见离子,1 000倍的Na+,K+,SO42-,Cl-等离子基本对测定没有干扰。本实验主要研究了3种主要重金属干扰离子Cu2+、Cd2+、Hg2+对铅离子测定的影响。在铅离子的溶出分析中,Cd2+能够占据电极表面铅离子的结合位点,而会降低铅离子的峰电流。Cu2+也因为会与铅离子形成金属共溶物沉积在电极表面而抑制铅离子的峰电流。Hg2+会在修饰电极表面形成汞膜而对铅离子的测定有很大的干扰。实验表明,当Pb2+浓度为50 nmol/L时,基于四氧化三铁/离子载体的修饰电极,100倍的Cd2+不干扰测定,20倍的Cu2+、Hg2+没有明显的干扰。而在不含离子载体的修饰电极上,10倍的Cu2+、20倍Cd2+对50 nmol/L Pb2+有明显抑制作用,而10倍的Hg2+会使铅离子的电流信号升高。这说明基于四氧化三铁/离子载体的修饰电极具有很好的选择性。因为本实验在开路电位下对 Pb2+进行富集,利用铅离子载体(ionophore)提供的仅与铅离子配合的位点或仅供铅离子通过的空穴,因而对 Pb2+进行选择性富集,有效阻止非目标离子在电极上的吸附与沉积,提高了目标离子Pb2+检测的选择性。
2.7 实际海水样品测量
取不同地点的近海岸海水样,经0.45 μm微孔膜过滤和紫外消解预处理后,利用标准加入法测出样品中铅离子的浓度。并将所得结果与用ICP-MS比较,分析结果见表1,从表中看出两者基本相吻合,表明该法有望用于海水样品中重金属离子的分析。
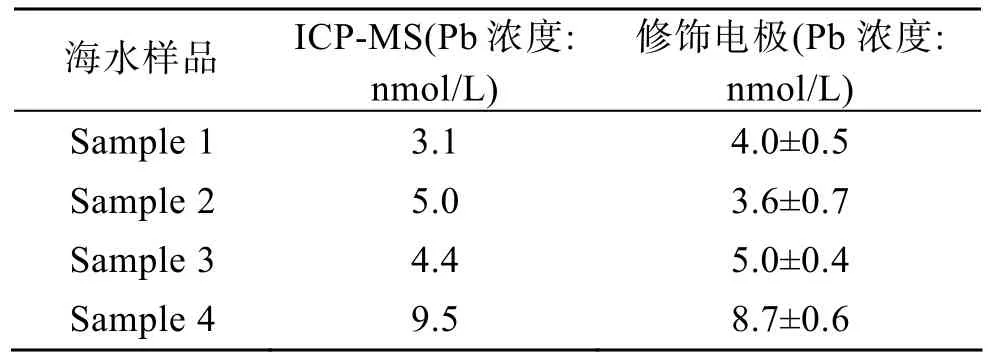
表1 实际海水样品测定结果比较Tab.1 Results of Pb determination in seawater samples
3 结论
利用纳米Fe3O4、Nafion导电聚合物以及具有良好选择性的离子载体混合物修饰玻碳电极,制成电化学传感器检测重金属离子 Pb2+的浓度。在所选实验条件下,峰电流与溶液浓度在 3~60 nmol/L范围内呈良好的线性关系。此法用于检测消解后的海水样品与ICP-MS法比较,表现出良好的吻合性,本试验为海水中重金属离子的检测提供了新的方法。
[1]奚旦立,孙裕生,刘秀英.环境监测[M].3版.北京:高等教育出版社,2004.
[2]Wang J.Stripping analysis:principles,instrumentation and applications [M].Deerfield Beach:VCH Publishers,1985.
[3]董绍俊,车广礼,谢远武.化学修饰电极[M].北京:科学出版社,1995.
[4]张立德,牟寄美.纳米材料和纳米结构[M].北京:科学出版社,2001:24-25.
[5]吕晓凤,殷平,胡玉才,等.无机吸附材料在处理含重金属离子肺水肿的应用进展[J].化学与生物工程,2007,24(6):8-11.
[6]Huang S H,Chen D H.Rapid removal of heavy metal cations and anions from aqueous solutions by an amino-functionalized magnetic nano-adsorbent [J].Hazard.Mater,2009,163 (1):174-179.
[7]Bodor S,Zook J M,Lindner E,et al.Chronopotentionmetric method for the assement of ionophore diffusion coefficients in solvent polymeric membranes[J].Solid state electrochem,2009,13:171-179.
[8]Hassan S S M,Saleh M B,Gaber A A A,et al.DDB liver drug as a novel ionophore for potentiometric barium(II)membrane sensor[J].Talanta,2003,59:161-166.
[9]华 秀,张志强.Nafion化学修饰电极富集和阳极溶出伏安法测定废水中铜[J].分析仪器,1997(1):33-36.
[10]Cao G X,Jimenez O,Zhou F M, et al.Nafion coated Bismuth film and Nafion coated Mercury film electrodes for anodic stripping voltammetry combined on line with ICP-MS spectrometry[J].J Am Soc Mass Spectrom,2006,17(7):945-952.
[11]杨丽珠,吴迪,叶筱琴,等.TZAAP-Nafion修饰电极溶出伏安法测定痕量铜[J].化学研究与应用,2007,12(19):1363-1366.
[12]Tsai Y C,Chen J M,Marken F.Simple cast-deposited multi-walled carbon nanotube/Nafion thin film electrodes for electrochemical stripping analysis[J].Microchimica Acta,2005,150:269-276.

