羧甲基纤维素-壳聚糖胶囊固定化蔗糖酶
杨 婷,侯文龙,牛少莉,刘晓敏,段志青,杨越冬
(河北科技师范学院理化学院,河北秦皇岛,066004)
固定化酶是指被局限在某一特定区域上的、并且保留了它们的催化活力、可以反复、连续使用的酶。与游离酶相比,固定化酶具有下列优点:固定化酶极易与底物、产物分开;可以在较长时间内进行反复分批反应和装柱连续反应;在大多数情况下,能够提高酶的稳定性;酶反应过程能够严格控制:产物溶液中没有酶的残留,简化了提纯工艺;较游离酶更适合于多酶反应;可以增加产物的收率,提高产物的质量;酶的使用效率提高,成本降低[1~7]。胶囊法固定化酶最接近自由酶的工作环境,能最大限度地保留酶的活性。在已有的胶囊法固定化酶技术中,利用聚阴离子电解质——海藻酸和聚阳离子电解质——壳聚糖、聚赖氨酸等间的静电作用形成多电解质络合物囊膜实现酶固定化的报道非常多[8~12]。羧甲基纤维素是非常廉价的聚阴离子电解质,也可与壳聚糖、聚赖氨酸等聚阳离子电解质形成多电解质络合膜实现酶的固定化,但以羧甲基纤维素和壳聚糖为原料进行胶囊法固定酶的研究未见报道。本试验以壳聚糖和羧甲基纤维素为原料制备羧甲基纤维素-壳聚糖胶囊并用其固定蔗糖酶,考察羧甲基纤维素-壳聚糖胶囊固定化蔗糖酶的可行性。
1 材料与方法
1.1 材料和药品
酵母;羧甲基纤维素钠(化学纯);壳聚糖(自制,脱乙酰度大于 80%);冰醋酸(分析纯);无水乙醇(分析纯);十二烷基硫酸钠(SDS);葡萄糖(分析纯);氢氧化钠(分析纯);3,5-二硝基水杨酸(化学纯);蔗糖(分析纯);醋酸钠(分析纯);丙三醇(分析纯)等。
1.2 试验方法
1.2.1 羧甲基纤维素-壳聚糖胶囊的制备 用 6号注射器的针头将壳聚糖溶液滴入到 100mL的 CMC溶液中,硬化24 h后滤出,用 pH 4.6醋酸缓冲溶液洗涤后得羧甲基纤维素-壳聚糖胶囊。实验中重点考察壳聚糖浓度、CMC浓度、硬化时间、固定化温度对胶囊形成效果的影响。
1.2.2 蔗糖酶的制备 SDS(十二烷基硫酸钠)抽提法[13]。称取酵母 10 g,加入 60 mL 0.3mmol/L的SDS溶解,40℃水浴 12 h后取出,4℃,12 000 r/min离心 15min,上清液即为粗制酶液。在粗制酶液中加入乙醇使其质量分数达 0.30,4℃放置过夜,然后在 4℃下 12 000 r/min离心 15min,取上清液,追加乙醇使其终质量分数达 0.50,4℃放置 1 h,在 4℃下 12 000 r/min离心 15m in,弃上清液,沉淀分为两部分,一部分干燥后测定沉淀中粗酶含量;另一部分用 pH 4.6醋酸缓冲溶液配制成含粗酶 0.3%的酶液,4℃保存备用。
1.2.3 羧甲基纤维素-壳聚糖胶囊固定化蔗糖酶的制备 取 1.2.2制备的粗酶液与 10.0 mL质量分数为 0.02的壳聚糖溶液充分混合,按 1.2.1相同的方法制备羧甲基纤维素-壳聚糖胶囊固定化蔗糖酶。固定化蔗糖酶在 pH 4.6的醋酸缓冲溶液中,4℃贮存备用。
1.2.4 羧甲基纤维素-壳聚糖胶囊的表征 ①羧甲基纤维素-壳聚糖胶囊形貌观察:将胶囊用刀片切开后平铺在载玻片上晾干,用 SEM观察胶囊表面形貌。②胶囊强度的测定:将胶囊置于离心管中,在 3 000转/min离心 30 min后观察胶囊的破碎或保持完整性情况来表征胶囊的膜强度。
1.2.5 酶和固定化酶活性的测定 以煮沸酶液作对照,以 1m in内催化释放 1μmol还原糖的酶量为 1个酶活单位(U)。取 2.0mL粗酶液与 2.0m L蔗糖溶液(0.2 g/L,pH 4.6醋酸溶液)混合均匀,于 37℃反应 15 min。用 DNS法测定反应液中还原糖的量[13~14]。固定化酶酶活测定同游离酶。取适量固定化酶与底物混合,均匀震荡 15min后,取上清液用 DNS法测反应液中还原糖的量。试验中重点考察缓冲溶液的 pH值、反应温度对游离酶和固化酶活性的影响。
游离酶和固定化酶的米氏常数通过 Lineweaver-Burk作图法(即双倒数作图法)测定。以 1/V对 1/[S]作图,根据直线在横轴上的截距(-1/Km)求出米氏常数 Km。
2 结果与分析
2.1 胶囊形貌
胶囊的形貌表面的微细结构见图1。从图 1可以看出,羧甲基纤维素-壳聚糖胶囊球形规整,分散性好,粒径均在 3mm左右(左上角 a为胶囊照片)。SEM观察可以看出,胶囊表面较均匀地分布许多孔径在 100~300 nm的微孔,这是反应底物和产物能有效迁移通过囊膜的基础。
2.2 影响胶囊形成的因素
2.2.1 壳聚糖和羧甲基纤维素浓度对胶囊形成的影响 将壳聚糖溶液和羧甲基纤维素溶液按不同的浓度组合制备胶囊,固化 24 h后观察成球情况;再经 3 000 r/m in离心半小时。当壳聚糖的质量分数为0.02,CMC的质量分数为 0.015时,制得的胶囊其成球性好,球形规则,机械强度最好,高于或低于此浓度时均不能得到理想的胶囊。
2.2.2 固定化时间对成球效果的影响 以质量分数为 0.02的壳聚糖溶液,质量分数为 0.015的 CMC溶液制备胶囊,在室温下固化不同时间,经 3 000 r/min离心半小时后观察胶囊的变形情况。试验中发现,随着固化时间的延长,囊膜强度逐渐增强,固定化时间为 24 h后的囊膜强度基本不再变化,处理过程中不再有皱缩或粘连的现象。
2.3 固定化酶的性质
2.3.1 pH值对固定化酶活性的影响 蔗糖酶在 pH 4.6时活性最大,试验中为考察固定化酶的耐酸碱性能,分别将游离酶和固定化酶在任意 pH值时的活性与各自在 pH 4.6时活性的比值的变化来表征游离酶或固定化酶活性受酸碱度的影响,测试温度 40℃(图2)。由图 2可知,游离蔗糖酶在 pH 4.6~5.0范围内活性最高,偏离这一 pH值范围其活性快速下降;当体系的 pH 5.5时游离蔗糖酶的活性仅为最高时的 18%,当 pH 3.6时其活性为最高时的 63%。而壳聚糖 -羧甲基纤维素胶囊固定化蔗糖酶的活性在 pH 4.6的偏酸性范围内随酸度增加,活性只是略有减低。当 pH值高于 5.0后固定化酶的活性才明显降低,但其幅度也明显低于游离酶,说明蔗糖酶固定化后其耐酸碱性能明显提高。
2.3.2 固定化酶的最适温度 体系的 pH 4.6时,蔗糖酶在 50℃表现出最高的催化活性。游离蔗糖酶和羧甲基纤维素-壳聚糖胶囊固定化蔗糖酶在不同温度时相对于各自在 50℃的活性如图 3所示。在低于 50℃时,体系的温度变化对游离蔗糖酶和固定化蔗糖酶的活性影响基本相同;高于 50℃时,随体系温度升高,游离酶的失活作用明显快于固定化酶,可见经羧甲基纤维素-壳聚糖胶囊包封后的蔗糖酶耐热性能有明显提高。
2.3.3 米氏常数(Km)与最大反应速度 分别以不同浓度蔗糖溶液在 37℃,pH 4.6下测定酶活力,以1 min时测定的酶活力代表酶促反应初速度,按 Lineweaver-Burk作图法作图(图 4)。根据直线在横轴上的截距(-1/Km)求出固定化酶的米氏常数(Km=54.11 mmol/L)较游离酶(Km=35.62mmol/L)大。这说明固定化酶对底物的亲和力相对较小,这与囊膜对底物和产物的扩散限制有关。也正是基于此原因,试验中固定化酶中还原糖的最大反应速度为 10.82mg/(m L·min),低于游离酶中的还原糖 Vmax=12.72 mg/(mL· min)。

图 1 羧甲基纤维素-壳聚糖胶囊表面的 SEM照片
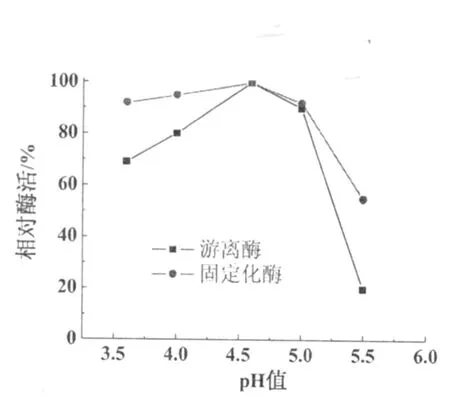
图 2 pH值对游离酶和固定化酶活力的影响
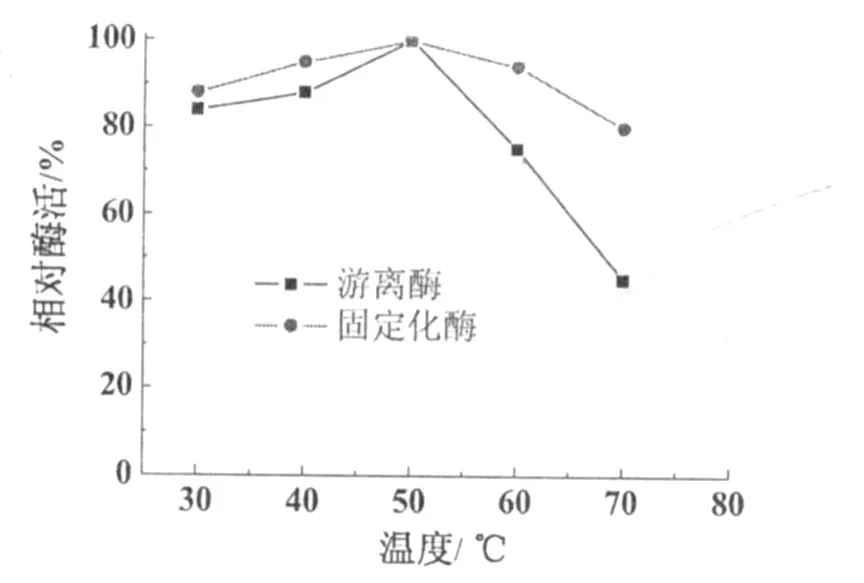
图 3 温度对游离酶和固定化酶活力的影响
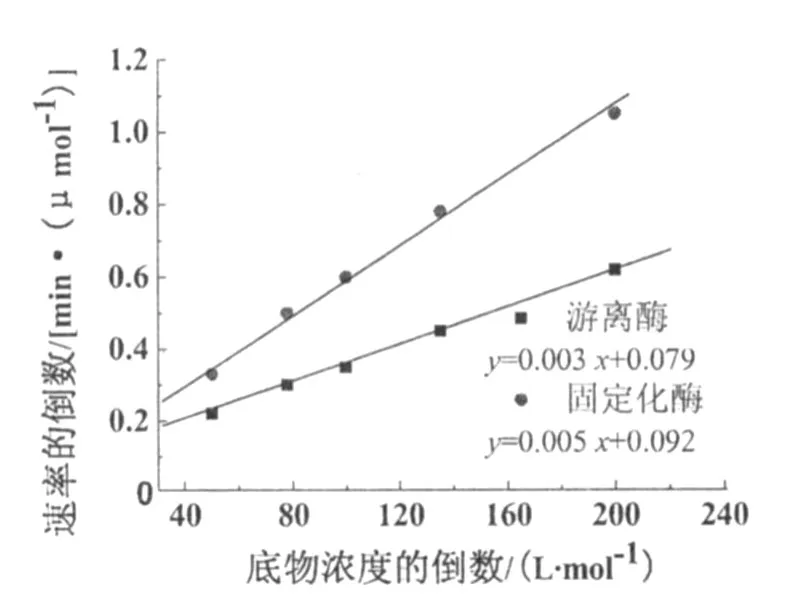
图 4 底物浓度与速率的关系
3 结 论
羧甲基纤维素-壳聚糖胶囊固定蔗糖酶耐酸性、耐热性明显增强,固定化酶的米氏常数(Km=54.11 mmol/L)大于游离酶的米氏常数(Km=35.62mmol/L);制备固定化酶的最佳工艺为:将酶溶于质量分数为 0.02的壳聚糖溶液中,滴入质量分数为 0.015的羧甲基纤维素溶液中固化 24 h。
[1] 郭勇.酶工程[M].北京:科学出版社,2004.
[2] 袁勤生,赵健.酶与酶工程[M].上海:华东理工大学出版社,2005.
[3] 孙志浩.生物催化工艺学[M].北京:化学工业出版社,2004.
[4] 郭勇.酶的生产与应用[M].北京:化学工业出版社,2003.
[5] 林章凛,李爽.工业酶一制备与应用[M].北京:化学工业出版社,2005.
[6] EMEL Emregul,SIBEL Sungur,URAL Akbu lut.Polyacrylam ide-gelatine carrier system used for invertase immobilization[J].Food Chemistry,2006,97(4):591-597.
[7] G Sanjay,SSugunan.Invertase immobilized on montmorillonite:reusability enhancement and reduction in leaching[J].Catalysis Communications,2005,6(1):81-86.
[8] 徐国英,朱启忠,董学卫,等.海藻酸钠-壳聚糖固定化漆酶的研究[J].西南师范大学学报:自然科学版,2008,33(3):90-94.
[9] 杨金水,刘葳.甲壳素/壳聚糖在酶固定化中的应用[J].生物技术,2006,16(2):89-91.
[10] 刘映薇,于炜婷,刘袖洞,等.海藻酸钠-壳聚糖-海藻酸钠(ACA)微胶囊的蛋白质通透性研究[J].中国生物医学工程学报,2006,25(3):370-373.
[11] 刘袖洞,于炜婷,王为,等.海藻酸钠和壳聚糖聚电解质微胶囊及其生物医学应用[J].化学进展,2008,20(1):126.
[12] 孙万成,蒋笃孝,宋龄瑛,等.壳聚糖/海藻酸钠微胶囊固定化磷脂酶 A 1的研究[J].食品科学,2004(11):14.
[13] 李楠,庄苏星,丁益.酵母蔗糖酶的提取方法[J].食品与生物技术学报,2007,26(4):83-87.
[14] 徐桦,陆珊华,孙爱民.酵母蔗糖酶 Km值的测定[J].南京医科大学学报,1999,17(4):329-330.
(责任编辑:石瑞珍)

