口服抗凝剂Edoxaban
口服抗凝剂Edoxaban
edoxaban;FXa抑制剂;抗凝作用;关节置换术;房颤
深静脉血栓(DVT)及相关并发症已成为影响公众健康的主要杀手之一。由于目前临床使用的抗凝疗法均存在局限性,人们正在积极开发强效稳定的新型口服小分子抗凝药。活化因子FXa为一种丝氨酸蛋白酶,可将凝血酶原转化为凝血酶,是一个极具价值的抗凝作用靶点,它在内源性和外源性两条凝血途径的会聚点发挥作用,现已成为开发新一代抗凝药物的主要靶点。一分子FXa可导致成千上万的凝血酶分子产生,而FXa抑制剂则可阻止凝血酶的突增,减少凝血酶诱导的凝血和血小板的激活,且无传统抗凝剂所具有的局限性。日本三共制药公司研发的新型口服抗凝剂edoxaban即为FXa的高特异性直接抑制剂,对其他丝氨酸蛋白酶无作用,其对FXa的选择性较对凝血酶(FⅡa)高10 000倍。
本品化学结构式:
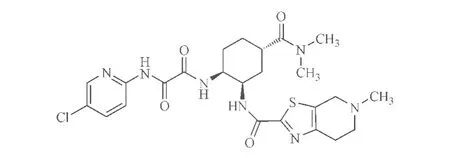
CAS:480448-29-1
药理作用 在抗凝血酶(AT)缺损小鼠中进行的试验显示,edoxaban的抗血栓作用不依赖于血浆AT水平。
大鼠和家兔静脉停滞模型试验显示,经口给予edoxaban,可显著抑制血栓形成。在铂丝诱导的大鼠静脉血栓模型试验中也获得相似结果,给予本品2.5mg◦kg-1,即可明显抑制血栓形成。在这些模型动物的血浆中,本品在激发抗血栓作用的同时,也致使凝血酶原时间(PT)延长和抗FXa活性提高。
在不同的实验动物模型中,研究者们比较了edoxaban与其他抗凝剂的抗血栓作用。不同大鼠模型实验显示,在相同剂量范围内,edoxaban可有效预防动脉和静脉血栓形成,而FXa间接抑制剂fondaparinux则需在较高剂量下方能抑制动脉血栓形成;分别静注edoxaban(0.3mg◦kg-1)或凝血酶抑制剂melagatran(2mg◦kg-1)均可有效抑制麻醉大鼠由组织因子诱导的高凝状态。
药动学 动物实验显示,edoxaban经口给药后1~2 h,其血药浓度即可达峰值,而一旦被吸收,主要经肾排泄,消除半衰期为9~11 h。本品(2.5和5mg◦kg-1)经口给予大鼠0.5 h后,对血浆中FXa活性的抑制作用达峰值,且抑制作用可维持达4 h。猴子试验显示,本品起效快:给药后4 h,抗FXa活性即达峰值(抑制率为93%),且在24 h时仍能保持11%的抑制率;在剂量为1mg◦kg-1时,本品的AUC和Cmax分别为(852±284)μg◦h◦L-1和(175± 74)μg◦L-1。人体试验显示,本品吸收快,血药浓度达峰时间(Tmax)中值为1.0~5.0 h,血浆半衰期为8~11 h;单剂量60 mg口服后1.5 h,血药浓度即可达峰值(240±16)μg◦L-1,而5 h后则降至(127± 6)μg◦L-1,12 h后降至(37±3)μg◦L-1。在高加索白种人和日本健康志愿者中进行的试验显示,在给药的同时摄取食物,对本品的AUC、Cmax以及肾清除率均无显著影响,只是进食状态下给药后的Tmax较空腹给药略有延迟。
安全性 诸多动物模型实验已表明,edoxaban诱发出血的剂量10倍于其呈现抗血栓活性的剂量,故本品较普通肝素或低分子肝素以及其他现用抗凝剂具有更为宽泛的安全剂量范围。在一项体内实验中,通过29号针头将0.1U胶原酶溶液注入大鼠纹状体,诱导脑内出血模型,再分别给模型大鼠使用edoxaban和melagatran,结果,测得二者对血栓形成的抑制率达50%时所需的剂量分别为0.045和0.14 mg◦kg-1◦h-1,并发现edoxaban发挥抗血栓作用与致脑内出血加重之间的安全剂量范围明显较melagatran更宽。而且,一系列的动物实验表明,重组FⅦa(rFⅦa)、rFⅧ、浓缩活化凝血酶原复合物Feiba和FⅨ可显著有效抑制edoxaban的抗凝作用,因此,一旦edoxaban导致严重出血,可用它们作为解药。
临床研究 在接受了选择性全膝关节置换术的523名日本患者中进行的一项随机、平行组、安慰剂对照、双盲、双模拟、多中心临床研究考察了edoxaban的疗效,结果显示,本品各剂量组(5~60mg◦d-1,持续11~14 d)受试者的静脉血栓栓塞(VTE)发生率均较安慰剂组显著降低(P<0.001),且此疗效呈剂量依赖性;各实验组受试者的临床出血事件发生率无显著差异,未见严重不良反应和肝酶水平变化。
在1 146名非瓣膜性房颤患者中进行的一项随机、平行组、多中心、多国、双盲、为期12周的Ⅱ期临床试验比较了不同剂量edoxaban(30 mg,qd或bid; 60mg,qd或bid)与华法林标准疗法的安全性,结果发现,edoxaban 30 mg(qd)和60mg(qd)剂量组中严重及不严重的临床出血事件发生率与华法林组相似,但30mg(bid)和6mg(bid)剂量组的此不良事件发生率却明显高于华法林组;各治疗组中肝酶水平持续升高的人数无显著差异,中风发生率也相当。表明,30mg(qd)和60mg(qd)edoxaban的安全性与华法林相似,且耐受性良好。
最近三共公司在奥兰多美国血液病学会(ASH)年会上披露了最新的edoxaban用于髋关节置换患者的Ⅲ期临床试验阳性结果,展现了该口服FXa抑制剂预防VTE的疗效要优于依诺肝素(Clexane/Lovenox,一种低分子肝素)。这项在日本进行的名为STARSJ-V的Ⅲ期临床试验中,接受全髋关节置换术的610名患者随机口服edoxaban (30mg,qd)或皮下注射依诺肝素(2 000 IU,bid),持续11~14 d,主要终点考察指标为症状性肺栓塞(PE)和DVT的发生率。结果,两组均未见PE发生,但edoxaban组的DVT发生率(2.4%)明显低于依诺肝素组(6.9%),相对风险降低65.7%(P= 0.016);两组严重及不严重的临床出血事件发生率无显著差异(2.6%vs 3.7%,P=0.475),且均未出现颅内出血和死亡病例;edoxaban组和依诺肝素组中转氨酶水平超过正常值上限3倍的受试者比例分别为2.6%和10.0%。
该公司也已完成另一项名为ENGAGE AFTIMI 48的全球性Ⅲ期临床试验的受试患者招募工作,这项试验将在全球1 400个中心的约21 000名患者中进行,比较30mg(qd)或60mg(qd)edoxaban与华法林用于房颤患者预防中风和系统栓塞的疗效。公司称,这是迄今最大规模的一项针对房颤患者的edoxaban临床试验。此外,一项在日本国内进行的将edoxaban用于PE和DVT患者VTE的急救和预防的Ⅲ期临床试验也正在开展受试患者的招募工作。
2010 年初,edoxaban已在日本首次递交上市申请,用于预防接受较大矫形外科手术(包括全膝置换术)患者的血栓形成。
R 973.2

