用于多发性硬化症的口服免疫调节剂Laquinimod
用于多发性硬化症的口服免疫调节剂Laquinimod
laquinimod;免疫调节剂;多发性硬化症
多发性硬化症(MS)是一种中枢神经系统(CNS)的炎性脱髓鞘疾病,其特征为局灶性白细胞炎症反应,并导致神经细胞功能障碍、肌无力、视觉障碍以及其他神经损伤症状(如轻度认知障碍、震颤、头晕、失聪、强直、疲劳、触痛、触觉丧失、对温度和疼痛敏感等)。MS的炎症发生在CNS的白质不规则区域,其所致脱髓鞘可减慢或完全阻断神经元传导,疤痕组织的硬化斑块取代髓鞘质,间或致神经纤维本身受损。据估计,全球约有250万MS患者,且频发于中青年人群,其中女性多于男性。但MS的病因尚不明确,其所致髓鞘质的破坏可能缘于休眠病毒或其他病原体引发的异常免疫反应。现已发现,6型疱疹病毒(HHV-6)、EB病毒(EBV)和肺炎衣原体可引发MS;环境因素也会导致MS的风险增加,如温暖的气候条件下MS具有高发率;而且,可能由某些相互作用基因(如ApoE-ε4、HLA-DR2和-DR53等位基因)突变产生的易感基因也参与了MS的病理过程。
目前的MS疗法主要是针对MS复发和发展的预防与治疗以及症状的控制,其疾病缓解药物包括抗炎、免疫调节和免疫抑制类药物,如重组干扰素(IFN)β1b和β1a、盐酸米托蒽醌以及醋酸glatiramer,但需频繁注射给药,且不能长效抑制病情,还会引发流感样副作用及注射部位炎症反应。不过,免疫调节似乎仍是最引人关注的MS治疗途径,而抑制攻击髓鞘的T细胞、B细胞和巨噬细胞活性,已成为用于治疗MS的免疫调节剂开发与研究的焦点。口服免疫调节剂三羧氨基喹啉(roquinimex,Linomide)在临床试验中可有效抑制MS,然而因不良反应发生率较高,且耐受性差,其Ⅲ期临床试验被终止,因此研究者们正积极研发更高效且具更少的免疫调节剂典型不良反应(如发热、肌肉和关节痛以及强直)的抗MS药。由Active Biotech公司开发的新型口服免疫调节剂laquinimod(ABR-215062)是在三羧氨基喹啉结构的基础上经化学修饰(包括在喹诺酮环上引入若干取代基,并延伸酰胺甲基链)而合成的新化学实体,与三羧氨基喹啉相比,它不仅具有独特的化学结构,且MS动物模型实验显示,它能更有效地抑制病情发展和CNS中炎症细胞浸润,安全性更好。
本品化学结构式:
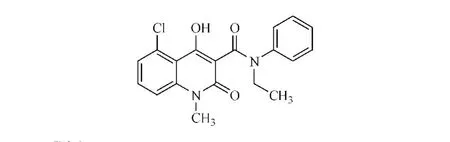
CAS:248281-84-7
药理作用 在一项动物实验中,研究人员给SJN/N小鼠接种C57BL/6小鼠脊髓匀浆,并注射百日咳毒素(PTX)诱导急性实验性自身免疫性脑脊髓炎(EAE)小鼠模型(即一种人MS的动物模型),且在小鼠接种后第3~7天和10~12天,经口给予laquinimod(0.04、0.2、1和5 mg◦kg-1◦d-1)。结果发现,本品能剂量依赖性抑制免疫小鼠发生急性EAE,且在最高剂量下可完全抑制EAE的发生;脑组织分析显示,1和10 mg◦kg-1◦d-1本品可分别显著减少和完全抑制CD45+白细胞浸润小鼠CNS;本品抗EAE活性较三羧氨基喹啉高20倍,后者对模型小鼠发生急性EAE的抑制剂量为0.2~25mg◦kg-1◦d-1,而二者均能抑制急性EAE所致小鼠体重的下降。另一项动物实验显示,本品还可显著抑制敲除IFN-β和野生型C57BL/6小鼠发生急性EAE,表明本品的作用不依赖于IFN-β的表达。
在一项体内研究中,通过免疫接种外周神经P0蛋白肽180-199和弗氏佐剂,诱导实验性自身免疫性神经炎(EAN)大鼠模型(即一种由CD4+T细胞介导的人脱髓鞘疾病格林-巴利综合征的动物模型),大鼠在免疫接种当日开始接受皮下注射laquinimod(1.6和16mg◦kg-1◦d-1),直至第35天。结果显示,与对照组相比,本品可显著地剂量依赖性地将EAN的发作推迟2~8 d,并降低了EAN的严重程度;本品还能抑制P0蛋白肽180-199特异性T细胞反应,减少外周神经的炎症和脱髓鞘作用;同时,本品可剂量依赖性减少淋巴结中炎症细胞因子IFN-γ和TNF-α,增加外周神经组织中抗炎症细胞因子IL-4。由此表明,本品的作用机制可能涉及对Th1/Th2细胞因子平衡的调节。
药动学 一项在SJL/N小鼠中进行的实验比较了laquinimod和三羧氨基喹啉的药动学特性,两药均为经口给予,剂量均为5 mg◦kg-1。结果显示,两给药组小鼠的总血药浓度相似,laquinimod组小鼠的Cmax和AUC分别为26μmol◦L-1和152μmol◦h◦L-1,而三羧氨基喹啉的两参数分别为30μmol◦L-1和125μmol◦h◦L-1;但两药的血浆蛋白结合率有较大差异,laquinimod和三羧氨基喹啉在血浆中的游离态百分率分别为2.2%和21.5%,游离三羧氨基喹啉的AUC值较游离laquinimod大8倍。
用小猎犬进行的试验显示,laquinimod在剂量达1.2mg◦kg-1◦d-1时仍耐受性良好,很少引发炎症副作用;在该剂量下,游离药物的AUCunb为2.9μmol◦h◦L-1,与5 mg◦d-1剂量下的人体实验值相似。急性EAE小鼠模型实验显示,本品0.1~1mg◦kg-1◦d-1剂量下的AUCunb为0.06~0.6μmol◦h◦L-1,与0.1~1 mg◦d-1剂量下的人体实验值相似。人体实验显示,本品在2.4~2.5 mg◦d-1剂量下可引起炎症副作用,表明人体对本品的敏感性超出动物模型实验所给出的预期。由此推测,本品用于MS患者的最初有效剂量可能为0.03 mg◦d-1,而在约0.3 mg◦d-1剂量下可获得最佳疗效。
临床研究 在MS患者中进行的Ⅰ期临床研究显示,laquinimod在2.4mg◦d-1剂量下方引起剂量限制性炎症反应,其最大耐受剂量(MTD)为1.2 mg◦d-1。一项在MS复发患者中进行的Ⅱ期临床试验显示,本品在0.3 mg◦d-1剂量下耐受性良好,且可有效抑制MS活动期病变;经该剂量本品的6个月治疗,受试者的MRI疾病活度检查值降低30%,而在治疗初期,受试者的疾病活度降低40%以上。
在涉及209名MS复发患者的一项双盲、随机、安慰剂对照临床试验中,与安慰组比较,laquinimod (0.1和0.3mg◦d-1,po,持续24周)能有效抑制MS活动期病变(由钆增强MRI脑部扫描测得),且对脑部至少已有一处MS活动期病变者尤为有效;在治疗期间和最后1次给药后8周进行的钆增强MRI扫描发现,与安慰剂组比较,本品0.3 mg◦d-1剂量组受试者脑部MS活动期病变的累积个数减少了44%,其中治疗前脑部至少已有一处病变者的病变累积个数减少了52%;本品各剂量组耐受性良好,仅可致轻度红细胞沉降率升高及肝功能异常,这些副作用通常为短暂性和无临床意义的;本品呈线性药动学特性,其清除率随受试者的EDSS评分(临床普遍使用的MS患者功能障碍等级评分)增加而下降;本品疗效与血药浓度成正相关,受试者体内血药浓度越高,其脑部病变发生率越低,因此在治疗窗口内,较高剂量的本品可产生较高疗效。
Active Biotech公司于2004年将laguinimod的全球市场(除了北欧和波罗的海国家)开发权转让给了Teva公司,最近两家公司宣布成功地完成了为期两年的laquinimod第1项Ⅲ期临床试验,这项名为ALLEGRO的试验涉及1 106名复发-缓解型MS (RRMS,一种常见型MS,其特点为不可预测的复发,伴有新症状出现,且已有症状加重)患者,达到了各项终点考察指标的预期,即与安慰剂组比较,RRMS受试者经本品1日1次口服治疗,其年复发率(主要考察指标)和病情恶化率(次级考察指标,采用EDSS评分测定)均明显降低,且本品耐受性良好,本品组受试者的感染总发生率与安慰剂组相似。但两家公司暂未披露该项试验详细数据,声称将会在2011年上半年的一次顶级科学会议上公布试验详情。目前,两家公司正期待于2011年3季度出台本品的第2项Ⅲ期临床试验报告,以便在欧美递交本品用于治疗RRMS的上市申请,该项为期2年、涉及1 332名受试患者、名为BRAVO的试验将比较本品与标准的注射用MS治疗药干扰素β-1a(Avonex)的疗效。
R 979.5

