碱金属离子交换Y型分子筛CO分子吸附量子化学研究*
, ,
(1.北京化工大学,教育部超重力工程研究中心,北京 100029;2.河北科技大学化学与制药工程学院)
碱金属离子(如Li+、Na+、K+)交换分子筛,由于其交换的碱金属存在,因而有着良好的催化性能和吸附性能。阳离子与不同客体分子之间相互作用的信息可通过检测探针分子与活化位之间形成络合物的性能来得到。CO分子是一种最常用的探针分子,能够很好地用来探测分子筛的吸附位、吸附性能及活化位的催化性能。CO分子与碱金属离子交换分子筛能形成不同的吸附情况,而之前的研究很少探讨CO在分子筛上的多分子吸附情况。
A.C.Otero等[1-2]研究Li-ZSM-5分子筛上CO分子吸附光谱时发现存在两个新的吸附带(2 193 cm-1和2 188 cm-1),而CO分子的振动峰在2 143 cm-1,很难从试验中分析这两种不同的振动峰存在的原因及详细信息。而量子化学能从微观角度详细准确地了解吸附位置、结构及其性能,因而被广泛应用于分子筛结构及性能的研究。前人[3-4]对碱金属离子交换分子筛的吸附试验和理论研究主要集中在Li-ZSM-5分子筛性能的研究,而对其他碱金属离子交换分子筛的研究则很少有报道,此外对于碱金属离子交换的Y型分子筛的研究鲜有报道。笔者应用量子化学方法,研究了碱金属离子交换Y型分子筛上CO多分子吸附行为,特别研究了其红外光谱和吸附催化性能。
1 计算模型和方法
在真实的Y型分子筛晶胞中截取一个含有5个Si四面体和1个Al四面体的6T簇模型(见图1),其由两个相互交叉的四元环组成,其中一个四元环位于六柱体中,另外一个位于方纳石笼中,面对Na-Y分子筛的超级笼。绝大部分的反应都发生在超级笼中,因而选取此6T簇模型作为计算起始模型,它能够模拟真实的碱金属离子交换的Y型分子筛的反应环境。S.A.Zygmunt等[5]通过量子化学计算研究认为,分子筛3T和1T簇模型中Al原子周围的氧原子缺失会导致理论计算尤其是能量计算的不准确,因而簇模型中的Si原子的悬挂键用H原子饱和,并且H原子沿着Si—O键的方向固定在晶格位置,保持结构的完整性,而对于Al原子则用羟基饱和,这样能更好地模拟Al原子附近的电子密度。

图1 从Y型分子筛晶胞中截取的6T簇模型
所有计算都应用密度泛函理论(DFT)的B3LYP方法[6],利用Gaussian 03[7]软件包计算完成。交换的碱金属离子(Li+、Na+、K+、Rb+、Cs+)的核电子用LANL2DZ有效核电势(Effective Core Potential,ECP)来表示,其价电子采用LANL2DZ基组,而其他原子均采用6-31+G(d,p)基组来计算。所有的稳态结构都用振动频率结果确认,红外光谱从频率分析中得出。
2 结果及讨论
2.1 碱金属交换分子筛结构
应用图1所示的6T簇模型作为碱金属离子交换的初始构型,优化所得的碱金属离子交换分子筛的稳态构型如图2所示,其结构参数列于表1。

图2 碱金属离子(M+)交换的Y型分子筛的稳态构型
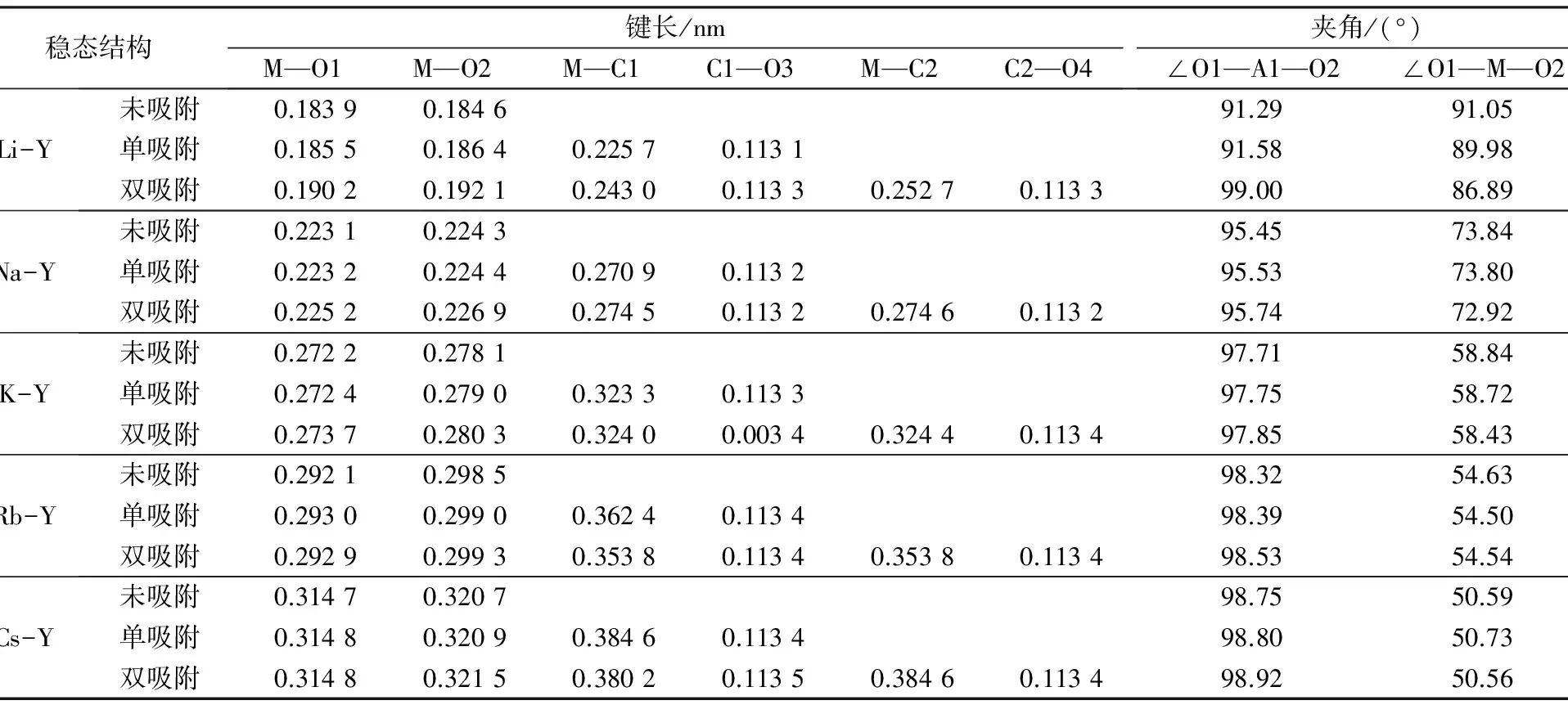
表1 优化的各态稳态结构参数
由图2及表1可以看出:碱金属离子与分子筛骨架上的氧原子O1、O2分别形成桥氧键;当Li+交换时,Li—O1和Li—O2的键长分别为0.183 9、0.184 6 nm;Al—O1的键长从未交换时的0.181 1 nm增加到0.184 2 nm,Al—O2的键长则由0.180 0 nm增加到0.183 6 nm;∠O1-Li-O2的角度为91.05°;Al—O的键长与Li—O的键长相差不大。这些都说明交换的碱金属离子与分子筛骨架相互作用,碱金属离子已与分子筛骨架相键合。其他碱金属离子Na+、K+、Rb+、Cs+的稳态结构与Li-Y分子筛的稳态结构类似。从表1还可以看出,随着原子半径的增加,M—O的键长逐渐增加。
2.2 CO单分子吸附
单个CO分子吸附在碱金属离子交换的Y型分子筛上的稳态结构如图3所示,其结构参数列于表1,Mulliken电荷参数列于表2。从图3及表1可以看出:单个CO分子吸附时,CO分子中的C原子会与碱金属离子弱相互作用,当CO分子吸附在Li-Y分子筛上时,Li—C的距离为0.225 7 nm,而Li—O1、Li—O2的键长分别增加到0.185 5、0.186 4 nm;C—O键长从自由分子时0.113 0 nm增加到0.113 1 nm。从表2可以看出,对于Li-Y分子筛,吸附态时CO分子的Mulliken电荷数增加到0.160,而Li+的Mulliken电荷数从0.590减少到0.492,说明吸附时电荷从Li+向CO转移,而分子筛结构参数变化很小,说明CO分子吸附时对分子筛结构的影响很小。当CO分子吸附在其他碱金属离子交换的分子筛时,其情况与Li-Y分子筛一致。随着碱金属原子半径的增加其M—C距离增加。但是值得注意的是,除Li-Y分子筛外,CO分子吸附在其他碱金属离子分子筛时,其电荷都是从CO分子向碱金属离子转移,而碱金属离子的电荷数变化不一,Na+、K+电荷减少,而Rb+、Cs+电荷增加。

图3 CO单分子吸附在碱金属离子(M+)交换Y型分子筛上的稳态结构
CO分子吸附时的热力学参数列于表2。从表2可以看出:当CO分子吸附在Li-Y分子筛时,其振动频率发生蓝移,出现在2 265 cm-1,高于未吸附时的CO峰值(2 202 cm-1,用相同方法计算所得);而CO分子吸附在Na-Y、K-Y、Rb-Y、Cs-Y分子筛上时,其振动频率分别为2 254、2 239、2 231、2 229 cm-1,都出现一定程度的蓝移。随着原子半径增加其振动频率逐渐减低。CO分子吸附时,与碱金属离子相互作用,放出热量,定义其相互作用能为:
Ebind=ECO-M-Y-EM-Y-nECO
式中:n为吸附的CO分子数。计算得CO吸附在Li-Y分子筛时,其结合能为26 kJ/mol。而随着原子半径增加,结合能迅速减低,吸附在Cs-Y分子筛时,其结合能仅为1 kJ/mol。其红外振动频率和结合能的变化说明,随着碱金属原子半径的增加,其与CO分子的相互作用逐渐减弱。

表2 Mulliken电荷及热力学参数
2.3 CO双分子吸附
计算发现,两个CO分子能稳定地吸附在碱金属离子交换的分子筛上,其吸附的稳态结构如图4所示。从图4可以看出,当第二个CO分子吸附时,其构型与单个CO分子吸附时相似,都是CO分子中的C原子与碱金属离子相结合。当CO分子吸附在Li-Y分子筛时,其Li—C1、Li—C2的键长分别增加到0.243 0 nm和0.252 7 nm。而C—O键长为0.113 3 nm,高于单个CO分子吸附时的键长。而∠O1-Li-O2、∠O1-Al-O2角度基本上未产生变化,说明吸附的CO分子未对分子筛骨架产生影响。双分子吸附时,Li+的Mulliken电荷数为0.646,说明双分子吸附时其电荷发生了转移。碱金属离子的Mulliken电荷数变化并不呈现规律性,但是吸附的两个CO分子的电荷变化量基本接近,但是都远低于相应的单个分子吸附时CO电荷的变化量。而两个CO分子吸附在其他碱金属离子交换分子筛时,其结构变化与Li-Y分子筛类似。
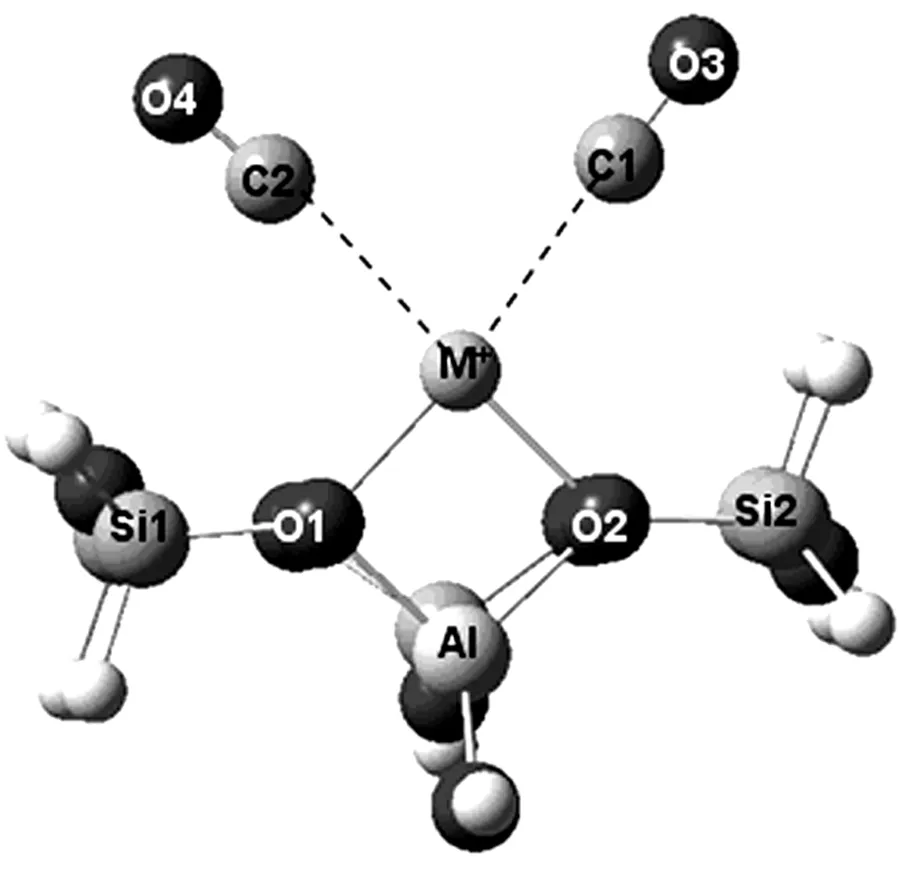
图4 CO双分子吸附在碱金属离子(M+)交换Y型分子筛上的稳态结构
双分子吸附时在Li-Y分子筛时,其CO振动频率会出现两个峰值,分别在 2 244 cm-1和2 239 cm-1。当双分子吸附时其CO振动频率比自由CO分子分别增加了42 cm-1和37 cm-1,而与单个CO分子吸附时则减少了21 cm-1和26 cm-1。这与A.C.Otero等[1-2]实验结果一致。从表2可以看出, Li-Y、Na-Y分子筛上双分子吸附时CO的振动频率与单分子吸附时有较大差别,而K-Y、Rb-Y、Cs-Y分子筛吸附时,其前后振动频率变化很小,且两个CO分子的振动频率很接近,大约相差1 cm-1。当第二个CO分子吸附在Li-Y分子筛上时,其结合能为-42 kJ/mol。而其吸附在Na-Y、K-Y、Rb-Y、Cs-Y的结合能分别为-26、-11、-5、-2 kJ/mol。双分子吸附的能量变化趋势与单分子吸附时类似。
3 结论
应用量子化学方法,从微观角度了解CO分子吸附在碱金属离子(Li+、Na+、K+、Rb+、Cs+)交换Y型分子筛上的机理,特别是对于CO吸附时红外光谱的变化做了详细研究。研究发现,CO能与碱金属离子发生多分子吸附,其吸附的结构及行为类似。计算所得CO单分子吸附在Li-Y、Na-Y、K-Y、Rb-Y、Cs-Y分子筛上时,其振动频率分别为2 265、2 254、2 239、2 231、2 229 cm-1,其红外光谱均会发生蓝移。当双分子吸附时,其红外光谱会出现两个新的吸附带,其频率比单个分子吸附时有所降低。Li-Y、Na-Y分子筛上双分子吸附时CO的振动频率与单分子吸附时有较大差别,而K-Y、Rb-Y、Cs-Y分子筛吸附时,其前后振动频率变化较小,且两个CO分子的振动频率很接近,大约相差1 cm-1。计算所得CO单分子吸附在Li-Y、Na-Y、K-Y、Rb-Y、Cs-Y的结合能分别为-26、-14、-6、-3、-1 kJ/mol,而双分子吸附时其结合能分别为-42、-26、-11、-5、-2 kJ/mol。能量计算结果显示CO分子吸附强度会随着离子半径的增加而减弱。
[1] Otero A C,Manoilova O V,Rodriguez D M,et al.Formation of several types of coordination complexes upon CO adsorption on the zeolite Li-ZSM-5[J].Phys.Chem.Chem.Phys.,2001,3:4187-4188.
[2] Otero A C,Rodriguez D M,Manoilova O V,et al.Linkage isomerism of carbonyl coordination complexes formed upon CO adsorption on the zeolite Li-ZSM-5:variable-temperature FT-IR studies[J].Chem.Phys.Lett.,2002,362(1/2):109-113.
[3] Millini R.Application of modeling in zeolite science[J].Catal.Today,1998,41:41-51.
[4] Bonelli B,Garrone E,Fubini B,et al.Two distinguishable lithium sites in the zeolite Li-ZSM-5 as revealed by adsorption of CO:an infrared spectroscopic and thermodynamic characterisation[J].Phys.Chem.Chem.Phys.,2003,5:2900-2905.
[5] Zygmunt S A,Curtiss L A,Zapol P,et al.Ab initio and density functional study of the activation barrier for ethane cracking in cluster models of zeolite H-ZSM-5[J].J.Phys.Chem.B,2000,104(9):1944-1949.
[6] 薛全民,张永春,宋伟杰.钴离子改性的Y型分子筛对低浓度NO吸附性能的研究[J].离子交换与吸附,2004,20(3):254-259.
[7] Naccache C M,Taarit Y B.Oxidizing and acidic properties of copper-exchange Y zeolite[J].J.Catal.,1971,22(2):171-181.

